真解(true solution)和胶体溶液(colloidal solution)的区别
真溶液和胶体溶液是两类性质不同的溶液。真实溶液和胶体溶液在许多性质上是不同的,比如颗粒大小、溶液外观、可过滤性和可见度。这主要是由于溶质颗粒大小的不同而引起的。真实溶液和胶体溶液的关键区别在于,真实溶液的性质是均匀的,而胶体溶液是一种非均匀混合物。
什么是真正的解决办法(a true solution)?
真正的溶液是含有溶解在溶剂中的两种或多种物质混合物的均质溶液。溶剂的粒径小于10-9m或1nm。一个简单的例子是糖在水中的溶液。真实溶液中的微粒肉眼看不见,而且这些微粒不能通过滤纸过滤。真正溶液中的粒子不会停留在原地,因为它们完全溶解在溶液中。因此,它们不能通过普通过滤分离。

什么是胶体溶液(a colloidal solution)?
胶体溶液是不均匀混合物,溶液中物质的粒径介于真溶液和悬浮液之间。它的范围从1纳米到1000纳米。火灾产生的烟雾是一个胶体系统的例子,其中微小的固体颗粒漂浮在空气中。与真实溶液类似,胶体溶液中的粒子肉眼看不见。但是,这些微粒大到可以被羊皮纸或动物膜挡住。

真解(true solution)和胶体溶液(colloidal solution)的区别
真溶液和胶体溶液的性质:
均质与非均质
真溶液:真实溶液含有两种或两种以上物质的均匀混合物。
胶体溶液:胶体溶液看起来像一个均匀的溶液,但它是一个不均匀的混合物。
粒子可见性:
真溶液:真溶液的溶质颗粒即使用显微镜也看不见。
胶体溶液:胶体溶液中的颗粒只有用强力显微镜才能看到。
粒径:
真溶液:真实溶液中粒子的大小约为10-10米。
胶体溶液:胶体溶液中溶质颗粒的大小在1-100nm之间。
物质分离:
真溶液:真实溶液中的成分不能通过过滤分离。
胶体溶液:胶体的成分不能通过过滤分离。然而,它们可以通过离心分离,然后用特殊的过滤器过滤。
廷德尔效应:
真正的解决方案:真正的解决方案不显示廷德尔效应。(不要散射光)
胶体溶液:胶体溶液表现出廷德尔效应。(也被称为“廷德尔散射”,是指胶体中的粒子或极细悬浮液中的粒子的光散射)
真溶液和胶体溶液示例:
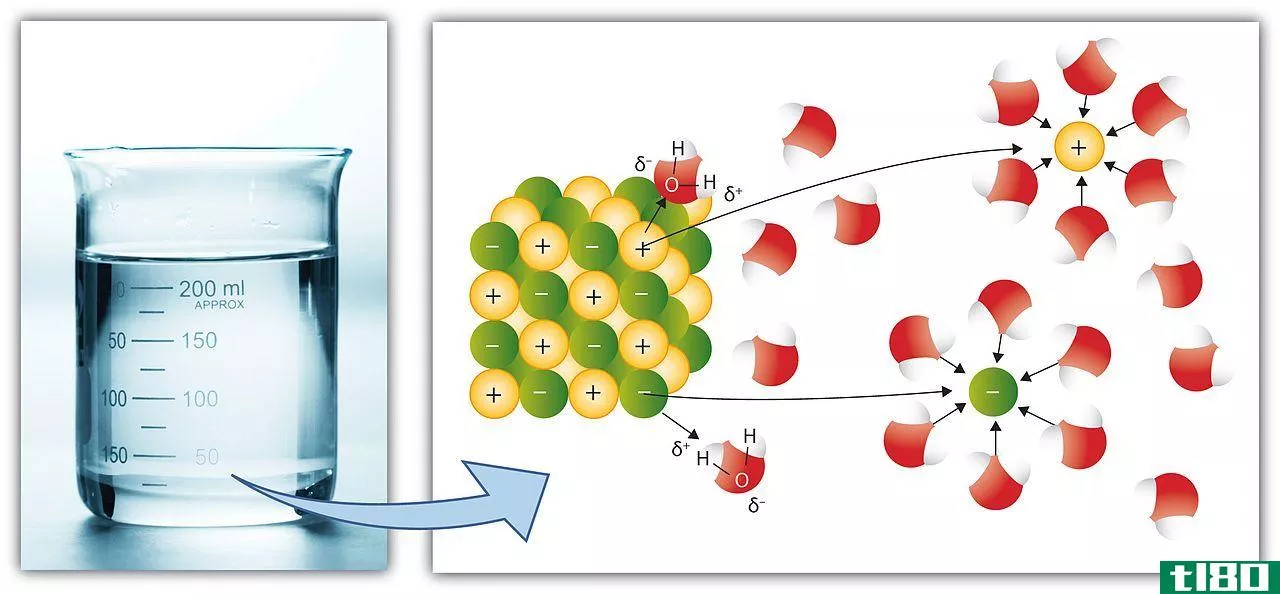
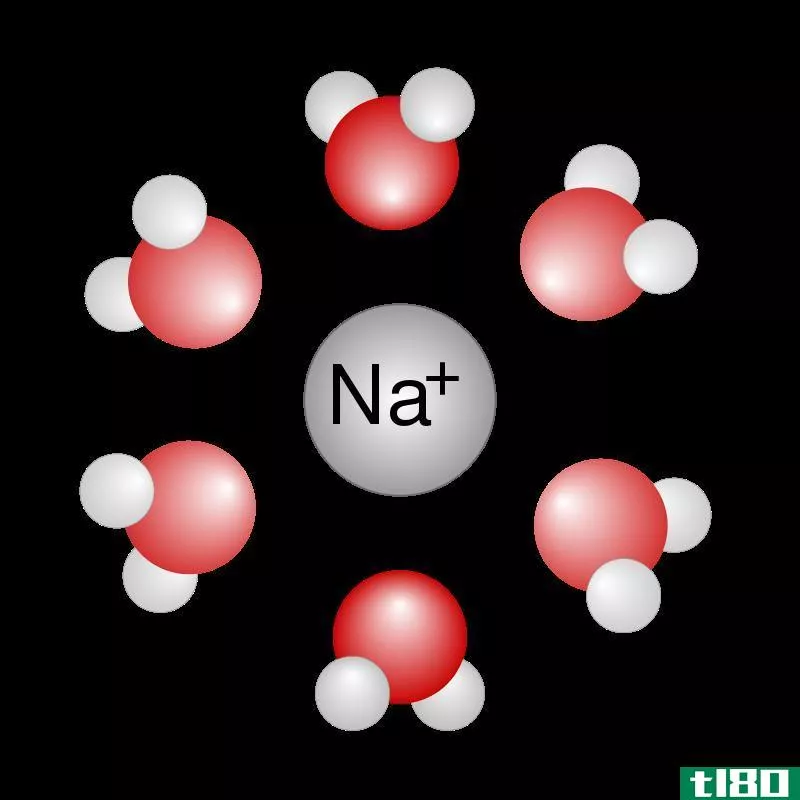
真正的解决方案:当我们把盐、糖等物质放入水中时,它们会完全溶解,形成均匀的溶液。换句话说,这些溶质分子在水中均匀分散。真实溶液中的粒子是分子大小的,它们是看不见的。此外,这些粒子不会停留在原地。真正的解决方案有:
- 普通盐在水中的溶液
- 糖水溶液
- 糖和明矾
胶体溶液:有些物质在溶液中完全可溶(糖溶于水),有些则完全不溶(沙子溶于水)。在这两种类型之间有一个中间类别;这些粒子比分子大,比悬浮粒子小。它们在强力显微镜下可见。胶体溶液的一些例子是,
- 水中淀粉
- 水中卵白蛋白
Image Courtesy:
1. Salt in water solution By Chris 73 / Wikimedia Comm***, [CC BY-SA 3.0], via Wikimedia Comm***