关键区别——sp3d2与d2sp3杂交
在电子所在的原子中有一种被称为轨道的假想结构。不同的科学发现为这些轨道提出了不同的形状。原子轨道可以经历一个称为杂交的过程。为了获得化学键合所需的合适形状,轨道杂交发生了。杂化是原子轨道的混合形成杂化轨道。sp3d2和d2sp3就是这样的混合轨道。sp3d2和d2sp3杂化的关键区别在于sp3d2杂化涉及同一电子壳层的原子轨道,而d2sp3杂化涉及两个电子壳层的原子轨道。
目录
1. 概述和主要区别
2. 什么是sp3d2杂交
3. 什么是d2sp3杂交
4. sp3d2与d2sp3杂交的相似性
5. 并列比较——sp3d2与d2sp3杂交的表格形式
6.摘要
什么是sp3d2杂交(sp3d2 hybridization)?
sp3d2杂化是将同一电子壳层的s,p,d原子轨道混合形成sp3d2杂化轨道。在那里,一个s原子轨道,三个p原子轨道和两个d原子轨道相互混合。这种混合导致六个大小和形状相同但方向不同的杂化轨道。
sp3d2杂化轨道以八面体排列。这些杂化轨道在八面体排列的两个轨道之间有90度角。八面体排列显示了一个正方形平面,其中有四个杂化轨道,其余两个轨道位于该方形平面的上方和下方(垂直于该平面)。
例子
让我们考虑一个例子来理解sp3d2杂交。例:SF6分子具有八面体形状,因为硫原子的3s、3p和3d原子轨道混合形成SP3D2杂化轨道。
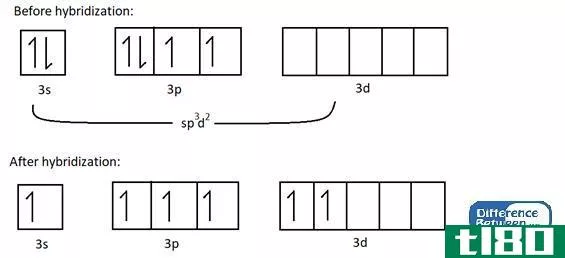
图01:杂化前后硫原子的电子结构。
如上图所示,杂化产生了六个不成对的电子,它们可以与六个氟原子进行化学键合。最重要的是,所有参与杂化的原子轨道都在同一个电子壳层中(在上面的例子中,它是n=3电子壳层)。
什么是d2sp3杂交(d2sp3 hybridization)?
d2sp3杂化是将同一电子壳层的s和p原子轨道与另一电子壳层的d轨道混合形成d2sp3杂化轨道。这种杂交产生了六个杂交轨道。这些杂化轨道以八面体几何排列。
最重要的是,在这种杂化中,d原子轨道来自不同的电子壳层(n-1电子壳层),而s和p原子轨道来自同一电子壳层。让我们考虑一个例子来理解这种杂交。大多数杂化的sp3是由杂化的金属配合物组成的。
例子
例如,以Co(NH3)3+络合物为例。
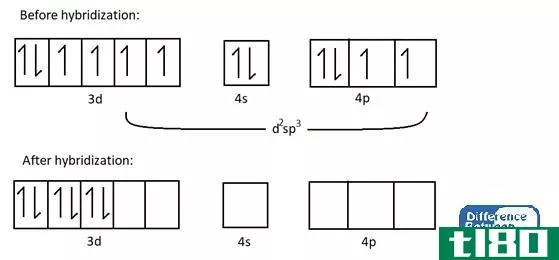
图02:杂化前后钴原子的电子结构。
如上图所示,杂化后钴原子中有六个空杂化轨道。这些空位轨道可以参与配位化学键的形成(这里氨配体=NH3)。
sp3d2型(sp3d2)和d2sp3杂交(d2sp3 hybridization)的共同点
- sp3d2和d2sp3杂交产生八面体几何。
- sp3d2和d2sp3杂化轨道之间的夹角均为90o。
- sp3d2和d2sp3杂交均产生6个杂交轨道。
sp3d2型(sp3d2)和d2sp3杂交(d2sp3 hybridization)的区别
| sp3d2与d2sp3杂交 | |
| sp3d2杂化是将同一电子壳层的s,p,d原子轨道混合形成sp3d2杂化轨道。 | 另一个电子壳层与spd的杂化轨道是d23的电子壳层杂化轨道。 |
| 命名法 | |
| sp3d2杂交形成sp3d2杂化轨道。 | d2sp3杂交d2sp3杂化轨道。 |
| 原子轨道类型 | |
| sp3d2杂化涉及同一电子壳层的原子轨道。 | d2sp3杂化涉及两个电子壳层的原子轨道。 |
| d轨道 | |
| sp3d2杂化涉及n电子壳层的d原子轨道。 | d2sp3杂化涉及n-1电子壳层的d原子轨道。 |
总结 - sp3d2型(sp3d2) vs. d2sp3杂交(d2sp3 hybridization)
sp3d2杂交和d2sp3杂交是混淆的术语,大多数情况下,它们被错误地交替使用。这些在很多方面是不同的。sp3d2和d2sp3杂化的关键区别在于,sp3d2杂化涉及同一电子壳层的原子轨道,而d2sp3杂化涉及两个电子壳层的原子轨道。
下载sp3d2与d2sp3杂交的pdf版本
你可以下载这篇文章的PDF版本,并根据引文说明离线使用。请在这里下载PDF版本:sp3d2和d2sp3杂交的区别