d块元素(d block elements)和过渡元素(transition elements)的区别
D块元素和过渡元素之间的区别是相当混乱的。这两个词可以互换使用,很多人用“过渡元素”来表示d块元素。D块元素和过渡元素的关键区别在于,虽然所有的转换元素都是D块元素,但并非所有D块元素都是转换元素。很明显,d块元素在d亚壳层中有d电子。过渡元素是形成具有不完全填充d轨道的稳定离子的元素。例如,锌和钪是d块元素,但不是过渡元素。
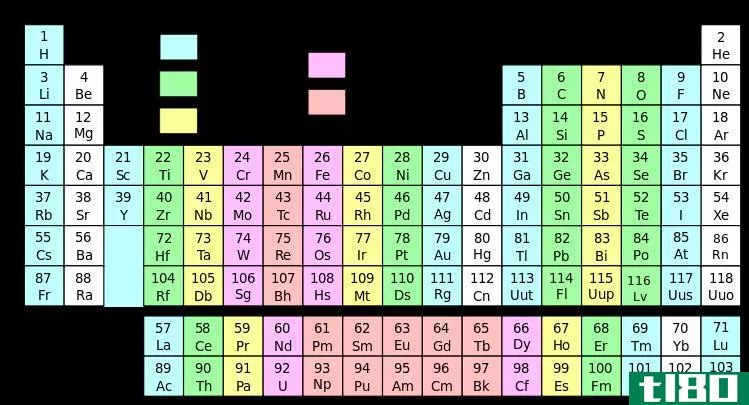
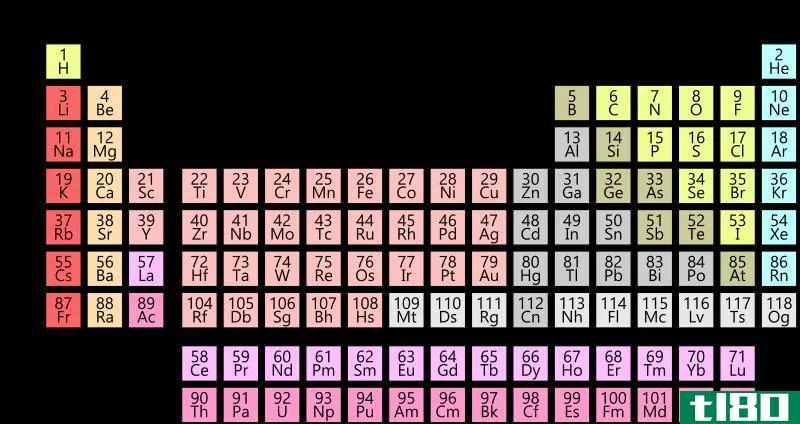
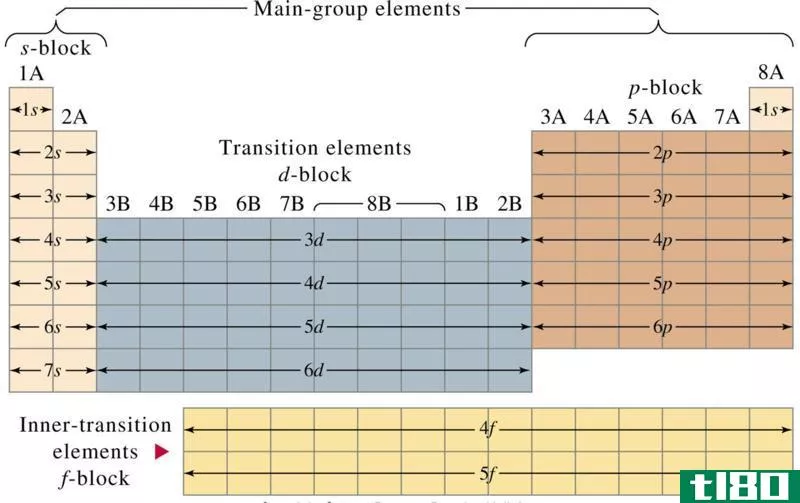
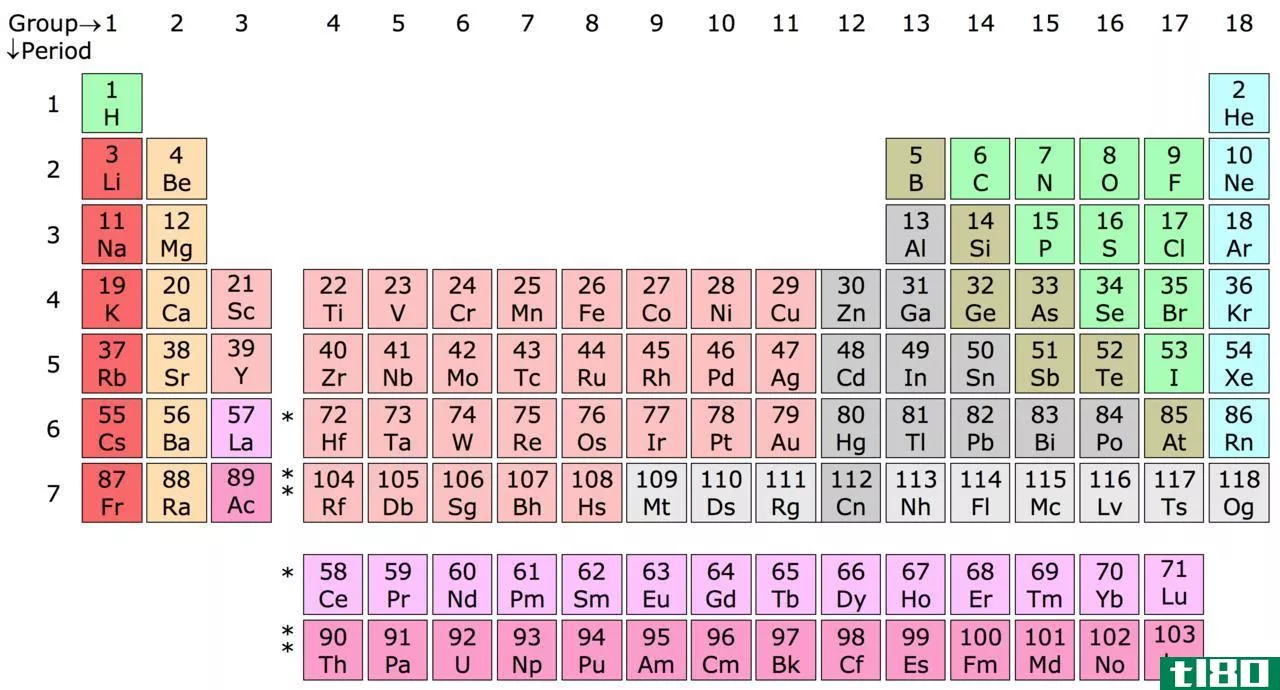
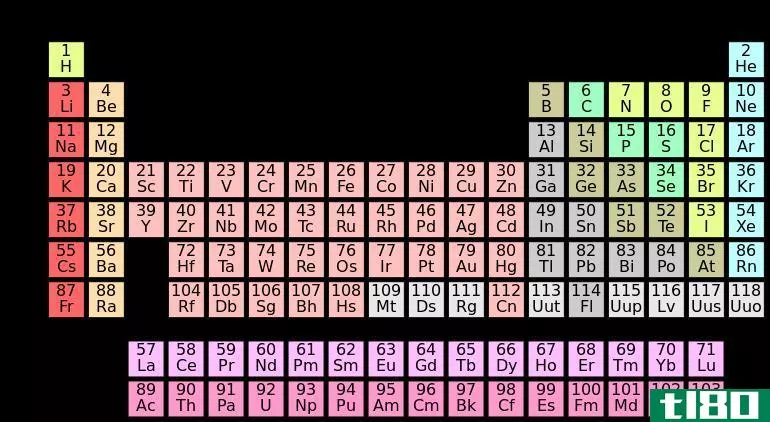
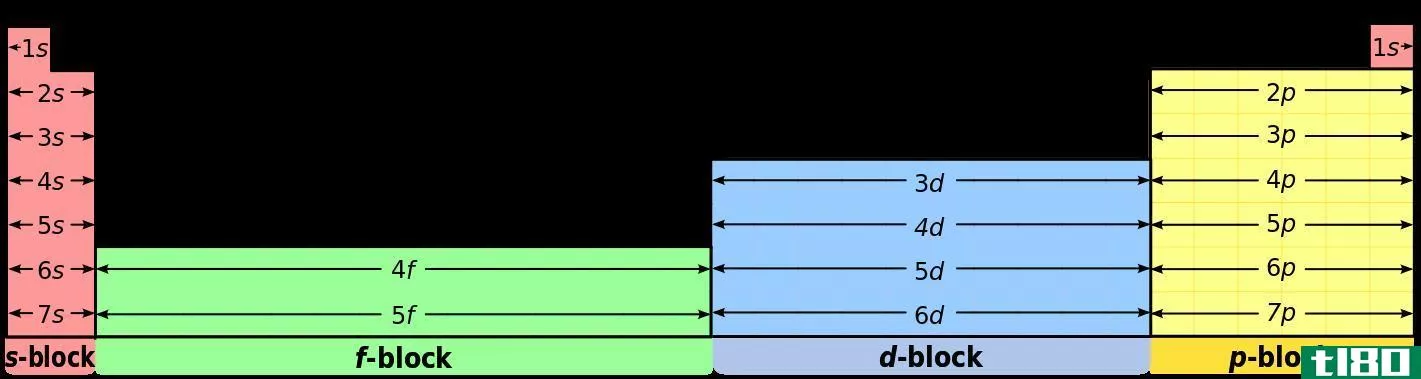
什么是d块元素(d-block elements)?

利用电子组态和元素周期表的位置可以清楚地识别D块元素。d块元素的主要特点是在d亚壳层中至少有一个电子。奇怪的是,根据Aufbau原理在d-block元素中填充电子时,4s电子首先被填充在3d电子之前,这意味着3d电子比4s电子具有更高的能量。但是,当它们除去电子形成离子时,4s电子首先从原子中移除。
| 元素 | 电子组态 | |
| 钪 | Sc公司 | 【银币】3d14s2 |
| 钛 | Ti公司 | 【银币】3d24s2 |
| 钒 | 五 | 【银币】3d34s2 |
| 铬 | Cr公司 | 【银币】3d54s1 |
| 锰 | 锰 | [543达令秒 |
| 铁质 | 铁 | 【银币】3d64s2 |
| 钴 | 一氧化碳 | 【银币】3d74s2 |
| 镍 | 镍 | 【银币】3d84s2 |
| 铜 | 特写 | 【银币】3d104s1 |
| 锌 | 锌 | 【银币】3d104s2 |
注:【Ar】=1S22S2P63S2**6
什么是过渡元素(transition elements)?
过渡元素是以不完全填充d形成稳定离子的元素-轨道。什么时候离子是由d-块元素形成的;它们首先消除s-电子(n-级),然后去除d-电子(n-1级)。锌和钪是d块中的两种特殊元素,它们不会形成具有不完全填充d轨道的离子,因此它们不被视为过渡元素。d-群中的所有其他元素形成稳定的离子,这些离子具有不完全填充的d-电子。

过渡金属溶液
d块元素(d-block elements)和过渡元素(transition elements)的区别
d块元素和过渡元素的定义
D-块元素:在D-亚壳层中有一个或多个D-电子的元素称为D-块元素。大多数d块元素是金属。
过渡元素:能形成不完全填充d轨道的稳定离子的元素称为过渡元素。
注:
Zn和Sc不是过渡元素。它们不仅形成Zn2+和Sc3+离子,它们不包含未填充的d-轨道。
222P263ZNs20+
Sc3+=1S22S2P63S2**63D10
下列离子含有未填充的d-轨道。因此,这些元素被视为过渡元素。
Cu2+=1S22S2P63S2**63D9
Ni4+=1S22S2P63S2**63D6
Mn2+=1S22S2P63S2**63D5
Fe2+=1S22S2P63S2**63D6
氧化状态:
D-嵌段元素:部分D-嵌段元素呈现多重氧化状态,少数元素呈现单一氧化状态。
例子:
锌只有+2氧化态,钪只有+3氧化态。
d区其它元素呈现多重氧化状态。
过渡元素:过渡元素呈现多种氧化状态。至少有一个状态包含未填充的d轨道。
例子:
钛+2,+4
钒+2、+3、+4、+5
铬+2,+3,+6
锰+2、+3、+4、+6、+7
铁+2,+3
钴+2,+3
镍+2,+4
铜+1,+2
Image Courtesy:
1. “Periodic table blocks spdf (32 column)” by User:DePiep [CC BY-SA 3.0] via Comm***