卤素和卤化物的关键区别在于卤素是在最外层p轨道上有一个未成对电子的化学元素,而卤化物没有未成对电子。
卤素是7族元素。由于卤素在p轨道上有一个不成对的电子,卤素最常见的氧化状态是-1,因为它们可以通过获得一个电子而稳定下来。这个电子获得形成卤化物。因此,卤化物是卤素的阴离子形式。
目录
1. 概述和主要区别
2. 什么是卤素
3. 什么是卤化物
4. 并列比较-卤素与卤化物的表格形式
5.摘要
什么是卤素(halogens)?
卤素是7族化学元素,在最外层的p轨道上有5个电子。此外,这些元素的最外层p轨道上有一个未配对的电子。因此,从外界获得一个电子并使之稳定是高度反应的。它们很容易形成阴离子形式,卤化物,通过获得一个电子。

图01:卤素的外观。(从左至右:氯、溴、碘)
这一组的成员是氟(F)、氯(Cl)、溴(Br)、碘(I)和虾青素(At)。此外,给它们起“卤素”这个名字的原因是它们都能形成具有类似性质的钠盐。我们可以看到这组物质的所有相;在正常情况下,氟和氯是气体,溴是液体,碘是固体化合物。阿斯他丁是一种放射性元素。此外,这些元素的一般电子构型是ns2np5。
什么是卤化物(halides)?
卤化物是卤素的阴离子形式。因此,当卤素从外部获得电子以获得稳定的电子构型时,这些化学物种就会形成。然后电子构型变成ns2np6。然而,卤化物总是负电荷。该组成员包括氟化物(F-)、氯化物(Cl-)、溴(Br-)、碘化物(I-)和阿斯汀(At负极)。这些离子的盐是卤化物盐。此外,所有这些卤化物都是无色的,并存在于固体晶体化合物中。这些固体具有很高的负生成焓。因此,这意味着这些固体很容易形成。
我们可以通过一些特殊的测试来确定卤化物的存在。例如,我们可以用硝酸银来表示氯化物、溴化物和碘化物的存在。这是因为,当我们在含有氯离子的溶液中加入硝酸银时,氯化银沉淀。如果我们在含溴化物的溶液中加入硝酸银,就会形成乳状溴化银沉淀物。对于含有碘离子的溶液,它会产生绿色沉淀。但是,由于氟化物不能与硝酸银形成沉淀物,因此我们无法从该试验中鉴别出氟化物。
卤素(halogens)和卤化物(halides)的区别
卤素是7族化学元素,在最外层的p轨道上有5个电子,其中包括一个不成对的电子。卤化物是卤素的阴离子形式,没有任何不成对的电子。这是卤素和卤化物的主要区别。此外,卤素基的成员是氟(F)、氯(Cl)、溴(Br)、碘(I)和虾青素(At)。另一方面,卤化物基团的成员是氟化物(F-)、氯化物(Cl-)、溴化物(Br-)、碘化物(I-)和阿斯他丁(At-)。下面以表格形式给出卤素和卤化物之间的详细区别。
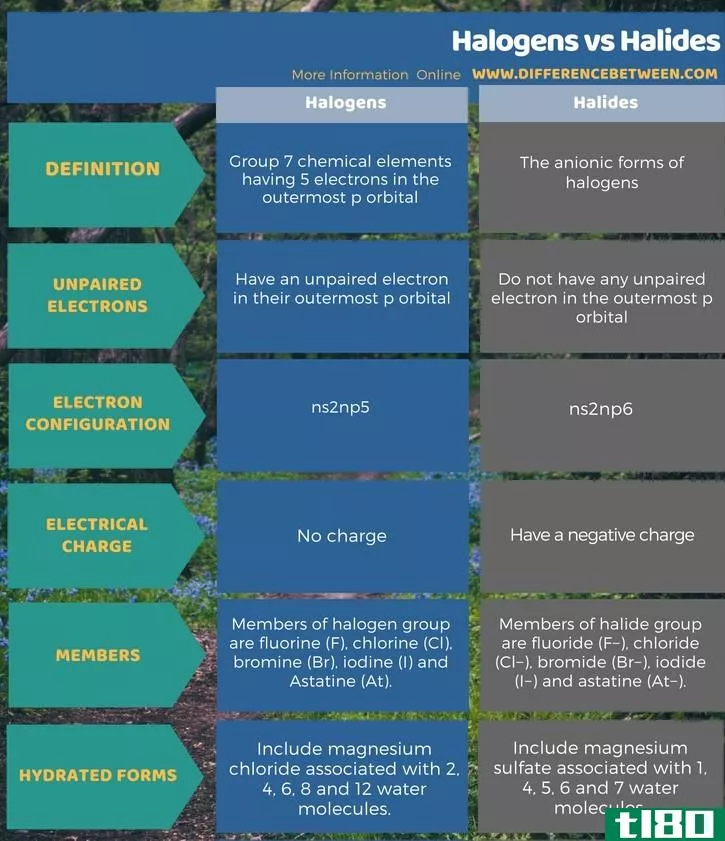
总结 - 卤素(halogens) vs. 卤化物(halides)
卤素是在外轨道上有一个不成对电子的7族元素。它们通过获得一个电子并变得稳定而形成卤化物。因此,卤素和卤化物的关键区别在于卤素是在其最外层p轨道上有一个不成对电子的化学元素,而卤化物没有未成对电子。
引用
1“卤化物”,维基百科,维基媒体基金会,2018年6月27日。这里有2个。克里斯特、卡尔等。“卤素元素”,《大英百科全书》,不列颠百科全书,2017年11月3日。此处提供
2克里斯特、卡尔等。“卤素元素”,《大英百科全书》,不列颠百科全书,2017年11月3日。