同素异形体(allotrope)和异构体(isomer)的区别
元素周期表中的某些元素在室温下稳定时,可以以不同的公式或不同的排列方式出现。它们可以是由单个元素组成的化合物,也可以是由多个元素组成的化合物。同素异形体和异构体是这类元素的好例子。同素异形体与同分异构体的关键区别在于,同素异形体是元素相同但化学式不同的化合物,而异构体则是元素不同,化学式不同的化合物。
目录
1. 概述和主要区别
2. 什么是同素异形体
3. 什么是异构体
4. 并列比较-同素异形体与异构体的表格形式
5. 摘要
什么是同素异形体(an allotrope)?
同素异形词可以定义为另一种类型。具体地说,它是指由同一单一元素组成的不同类型的化合物,但化学式不同,排列方式不同。这些同素异形体在相同的条件下(室温)以相同的物理状态存在,但它们的物理和化学性质却有所不同。在金属、非金属和类金属中可以观察到不同的同素异形体。
同素异形体的例子
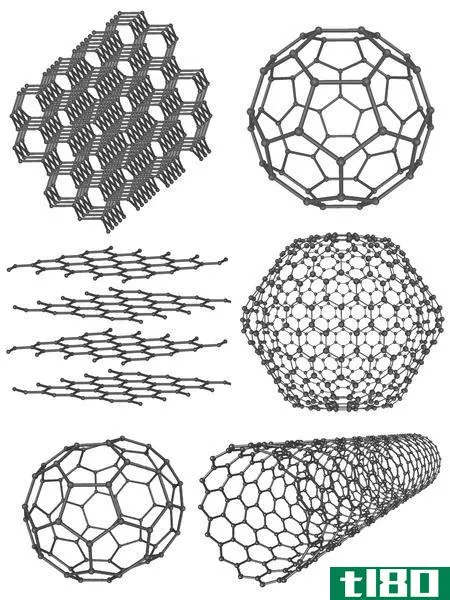
碳同素异形体
碳同素异形体以固态存在。最常见的类型是金刚石、石墨和碳黑。在这里,把它换成另一种结构是不容易的。金刚石是一种非常坚硬的结构,而石墨则没有那么硬。炭黑是以粉末的形式存在的。

图01:金刚石(左侧)和石墨(右侧)的结构和外观
氧的同素异形体
最常见的氧同素异形体是双原子氧(O2)和臭氧(O3)。它们的区别在于氧有两个氧原子与一个双键结合,而臭氧由三个氧原子组成,它们以共振结构存在。
硫同素异形体
硫的同素异形体根据附着的硫原子的数目和排列方式而不同。就硫而言,将一种形式的硫转化为另一种形式有点容易。
什么是同分异构体(an isomer)?
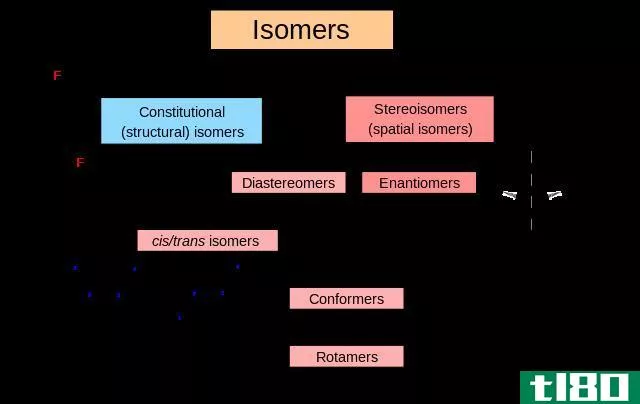
异构体是具有相同化学式但排列不同的化合物。同分异构体具有相同数量和类型的原子,但这些原子以不同的方式排列。因此,异构体的化学结构是不同的。异构体分为两大类,即结构异构体和立体异构体。
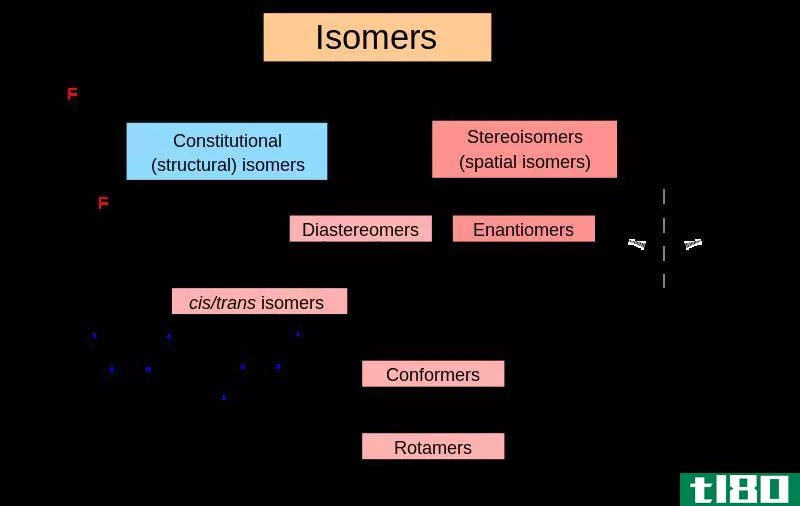
图02:异构体分类
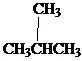
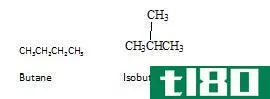
结构异构体
在这种结构中,原子和官能团以不同的方式连接在一起,形成这种结构。这种类型包括链异构、位置异构和官能团异构。
立体异构体
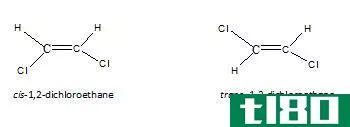
异构体的键结构和官能团位置相同,但几何位置不同。立体异构体包括顺反异构体(=非对映体)和光学异构体(=对映体)。

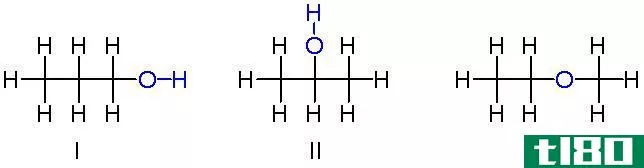
图03:丙二醇的立体异构体(注意两个分子中H原子的几何形状不同)。
同素异形体(allotrope)和异构体(isomer)的区别
| 同素异形体与异构体 | |
| 同素异形体是元素相同但化学式不同的化合物。 | 同分异构体是具有不同元素但化学式相同、排列不同的化合物。 |
| 原子数 | |
| 同素异形体是由不同数量的原子组成的。 | 同分异构体具有相同数量的原子。 |
| 元件类型 | |
| 同素异形体是由同一个元素组成的。 | 异构体由不同的元素组成。 |
| 结构 | |
| 同素异形体总是有不同的结构。 | 异构体可能具有相似或不同的结构。 |
| 存在 | |
| 同素异形体可以在金属、非金属和类金属中观察到 | 在有机分子(例如:碳氢化合物)和无机分子(例如:硅烷)中可以看到异构现象。 |
| 主要类型 | |
| 同素异形体的类型包括金属同素异形体、非金属同素异形体和非金属同素异形体 | 异构体主要包括结构异构体和立体异构体。 |
总结 - 同素异形体(allotropes) vs. 异构体(isomers)
同素异形体和同分异构体都可以定义为元素或化合物的替代类型。大多数情况下,这些都是稳定的天然化合物。同素异形体与同分异构体的主要区别在于,同素异形体是不同排列方式中具有相同元素的化合物,而同分异构体则是不同排列方式中具有相同化学式的不同元素的化合物。
下载同素异形体与异构体的pdf版本
你可以下载这篇文章的PDF版本,并根据引文注释离线使用。请在这里下载PDF版本同素异形体和异构体的区别。
引用
1.赫尔曼斯汀,安妮·玛丽。“什么是异构体?复习你的化学概念。N、 p.,N.d.网站。这里有。2017年6月1日。2.“同素异形体”。化学剧本。歌词,2017年3月21日。这里有。网状物。2017年6月1日。
2.“同素异形体。”化学歌词。歌词,2017年3月21日。