s(s)和p块元素(p block elements)的区别
s和p块元件之间的关键区别可以通过它们的电子配置得到最好的解释。在s块元素中,最后一个电子填充到s子壳层,在p块元素中,最后一个电子填充到p子壳层。当它们形成离子时,s阻挡元素很容易将电子从最外层的s亚壳层移除,而p阻挡元素接受电子进入p子壳层或从p子壳层移除电子。p-群中的一些元素形成正离子,从最外层的p-亚壳层移除电子,而一些元素(最具电负性的元素)形成负离子,接受其他元素的电子。当你考虑化学性质时,s和p块元素之间有一个显著的差异,这基本上是由于电子的配置。
什么是s块元素(s-block elements)?
S块元素是元素周期表中I族和II族的化学元素。由于s亚壳层只能容纳两个电子,这些元素的最外层通常有一个(I组)或两个(II组)电子。第一组和第二组的元素如上表所示。
| IA公司 | 二A | |
| 2 | 锂 | 是 |
| 三 | 不适用 | 毫克 |
| 4 | K | 加利福尼亚州 |
| 5 | Rb公司 | 高级 |
| 6 | 铯 | 文学士 |
| 7 | 法国 | 拉 |
| IA公司 | 碱金属 |
| 二A | 碱土金属 |
s块中的所有元素都形成正离子,它们都是非常活泼的。
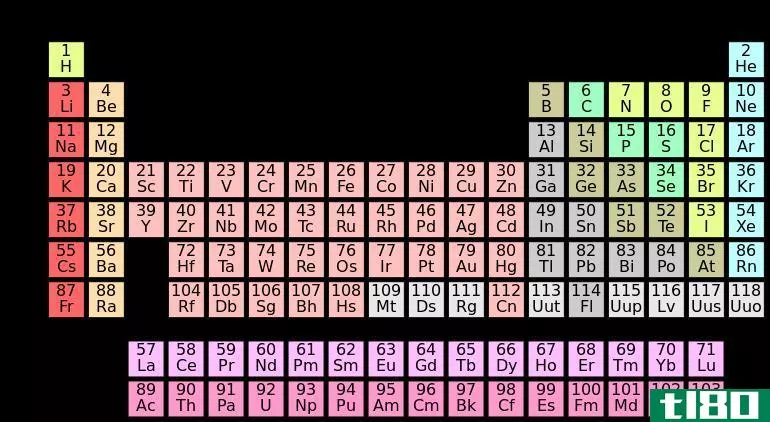
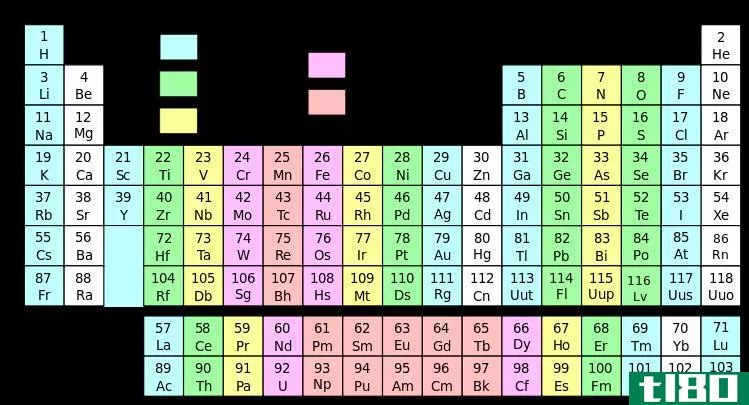
周期表中S块元素的放置
什么是区元素(p-block elements)?
P块元素是最后一个电子填充到P亚壳层中的元素。有三个p-轨道;每个轨道可以容纳两个电子,总共有六个p-电子。因此,p块元素的最外层有一到六个p电子。P-block包含金属和非金属,此外还有一些类金属。
| 13 | 14 | 15 | 16 | 17 | 18 | |
| 2 | B | C | N | O | F | 氖 |
| 三 | 艾尔 | 硅 | P | S | 氯 | 应收账 |
| 4 | 佐治亚州 | 通用电气 | 作为 | 硒 | Br公司 | 克朗 |
| 5 | 在 | 序号 | 某人 | Te公司 | 我 | Xe公司 |
| 6 | Tl公司 | 铅 | 商业智能 | 采购订单 | 在 | 注册护士 |
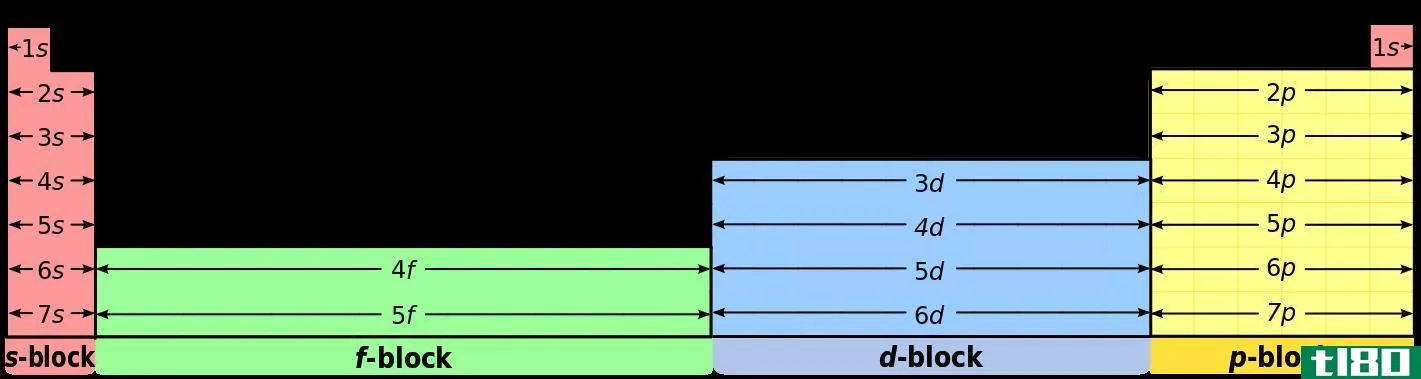
s(s)和p块元素(p block elements)的区别
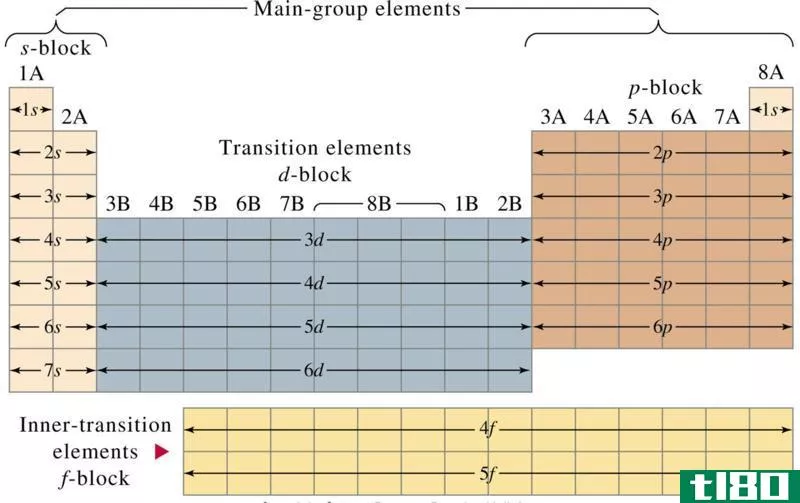
常见电子构型:
S-块元素:S-块元素具有[惰性气体]ns1(I组元素)和[惰性气体]ns2(II组元素)的常见电子构型。
P块元素:P块元素具有[惰性气体]ns2 np1-6的常见电子构型。但是,氦有1s2构型,这是一种特殊情况。
氧化状态:
S块元素:S块元素不像p块元素那样表现出多重氧化状态。例如,Ⅰ族元素呈+1氧化态,Ⅱ族元素呈+2氧化态。
P-块元素:与s-块元素不同的是,P-块元素在周期表中有一个共同的氧化状态,另外一些其他的氧化状态取决于离子的稳定性。
| 集团 | 13 | 14 | 15 | 16 | 17 | 18 |
| 一般电子组态 | ns2np1型 | ns2np2型 | ns2np3型 | ns2np4型 | ns2np5型 | ns2np6型 |
| 小组第一名成员 | 是 | C | N | O | F | 他 |
| 共氧化数 | +三 | +四 | +五 | -二 | -1 | 0 |
| 其他氧化状态 | +1 | +2,-4个 | +3,-3个 | +4,+2, | +3,+5,+1,+7 | – |
属性:
S块元素:一般来说,所有的S块元素都是金属。它们是有光泽的,良好的电导体和热导体,很容易从价壳层中移除电子。它们是周期表中最活跃的元素。
P-block元素:大多数P-block元素都是非金属元素。它们的沸点低,导电性差,很难从最外层的壳层中除去电子。相反,它们获得电子。一些非金属在室温下是固体(C,P,S,Se),而有些是气体(氧,氮)。溴是一种非金属,在室温下是液体。
此外,p块还含有一些金属元素:铝(Al)、镓(Ga)、铟(In)、锡(Sn)、铊(Tl)、铅(Pb)和铋(Bi)。
Image Courtesy:
1. “Periodic table (polyatomic)” by DePiep [CC BY-SA 3.0] via Comm***