主要区别
分子与化合物的主要区别是相似的原子结合形成分子,而不同原子结合形成化合物。
分子(molecule) vs. 复合(compound)
分子是由来自同一元素的两个或多个原子组成的。这种化合物由来自不同元素的两个或多个原子组成。在分子中,原子通过分子键结合在一起。在化合物中,有不同类型的键合原子,它们可以简单地共享它们的电子,也可以通过形成离子键将电子完全捐赠给另一个原子。分子不能用肉眼看。然而,裸眼很容易看穿。
分子表现出与原子相似的物理和化学性质。化合物在键合后表现出不同的原子化学和物理性质。分子包含有限数量的原子,而化合物包含无限数量的原子或分子。分子的最小单位是原子,而化合物的最小成分是分子。在分子中,原子的电子通过形成分子键而共享。在化合物中,电子通过形成不同的键(如离子键、金属键、共价键等)被完全转移或给予对方。
分子表现出相同的形状和相同的物理或化学性质。与它们的元素相比,这种化合物显示出不同的物理和化学性质。我们可以在化学反应中分离分子,也可以把它们连接起来形成一个大分子。化合物一旦形成,就不容易在化学反应中分离出化合物的分子。
比较图
什么是分子(a molecule)?
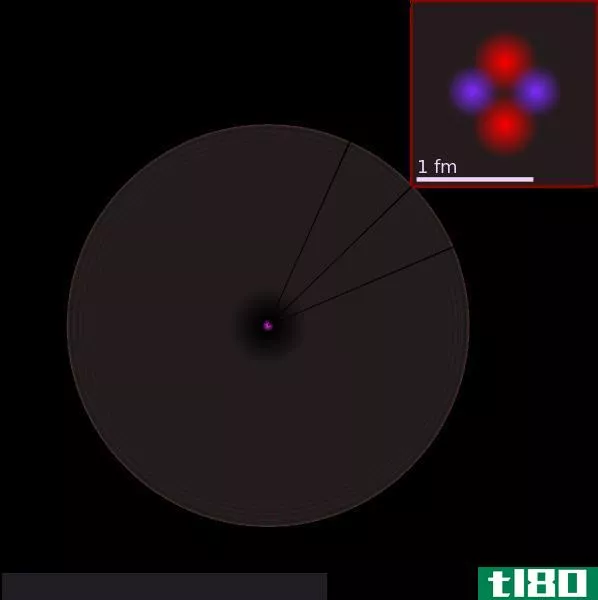
分子是化合物的基本部分。一个分子包含了化合物所具有的所有化学性质——由同一元素的原子结合而成的分子。在解释原子的结构时,它也被定义为“原子是化合物的一个小单元,它又进一步细分为电子、质子和中子,这些都是原子的子粒子。”电子在原子核外旋转,中子和质子存在于原子核内。
质子是带正电荷而电子带负电荷的物种。然而,中子是中性的,不带电荷。原子核中的每个元素都有一个特定数量的质子,称为该元素的原子序数,原子序数用Z表示。原子的质量数由质子和中子之和计算,a表示它。
原子主要是空的,但原子核的巨大质量覆盖了原子的中心。原子核拥有带正电荷的粒子,即质子,这就是为什么说原子核带正电荷的原因。分子的性质并不取决于连接原子所形成的键的类型,例如,氮气中只有一种元素是氮,它们通过分子键连接在一起。碳分子中也只含有碳元素。
什么是化合物(a compound)?
化合物是由两个或多个不同元素的分子通过共价键或离子键连接而成的。在化合物中,存在不同类型的化学键将原子结合在一起,例如,一些分子通过形成共价键形成键,一些分子形成离子键,一些通过金属键连接在一起,还有一些通过共价键共享电子。一种特定的化合物可以通过与另一种化合物的化学反应而变成不同的成分。
化合物分为两种不同类型的化合物。一种是分子化合物,另一种是盐。在分子化合物中,原子通过共价键结合在一起。然而,在盐中,原子是通过形成离子键来连接的。从不同的分子中,形成一种化合物,发生化学反应,使分子的性质变为新的稳定的不同性质、不同颜色、不同形状的元素。所有化合物都具有独特的分子空间排列,由化学式表示的化合物,即有关连接原子的信息。
例如,水分子的化学式是H2O,这意味着水分子是一个氧原子和两个氢原子的组合。相比之下,过氧化氢分子表示为过氧化氢,这意味着它含有两个氢原子和两个氧原子。食盐的化学式是氯化钠。它表明食盐是由一个钠和一个氯分子组成的。
主要区别
- 在分子中,原子通过简单共享方法共享电子,而化合物则通过部分共享方法共享电子。
- 分子体积小,重量轻;另一方面,化合物比分子大。
- 原子是分子的基本成分;相反,分子是化合物的基本成分。
- 一个分子含有最少数量的原子;另一方面,一种化合物含有最多数量的原子。
- 分子的基本成分是原子,而化合物的基本成分是分子。
- 与化合物相比,分子可以以其正确的形状存在,因为在化合物分子中,不能保持其形状。
- 与化合物相比,分子是最小的物种,而化合物是更大的物种。
- 分子用它们的符号表示;另一方面,化合物用它们恰当的化学式来表示。
- 分子是相同原子的一种形式。然而,由不完全相同的原子组成的化合物。
结论
它的结论是一个分子只包含一种元素,而这种化合物包含两种或两种以上的元素。