电解与原电池
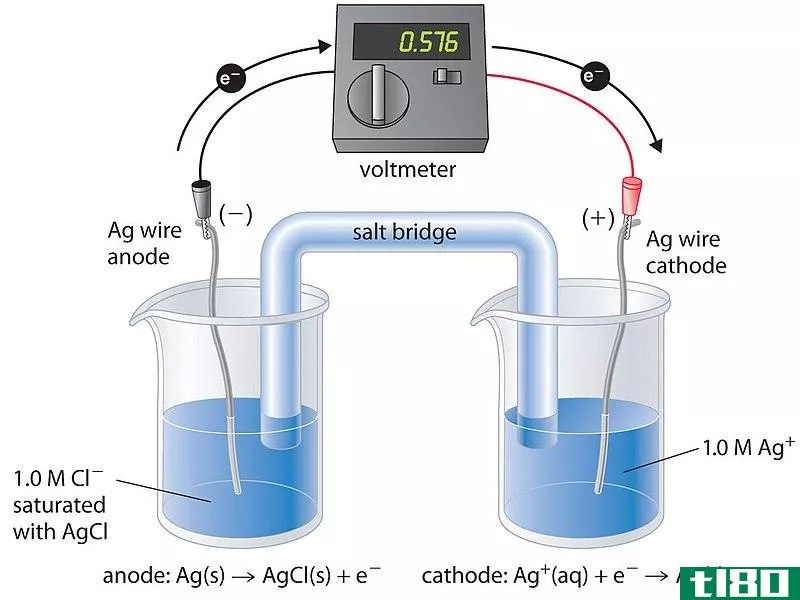
电解电池和原电池是两种类型的电化学电池。在电解槽和原电池中,都会发生氧化还原反应。在一个电池中,有两个电极,叫做阳极和阴极。氧化反应发生在阳极上,还原反应发生在阴极上。电极浸入单独的电解质溶液中。通常,这些溶液是与电极类型有关的离子溶液。例如,铜电极浸入硫酸铜溶液中,银电极浸入氯化银溶液中。这些解决方案是不同的;因此,它们必须分开。把它们分开是最常见的方法。
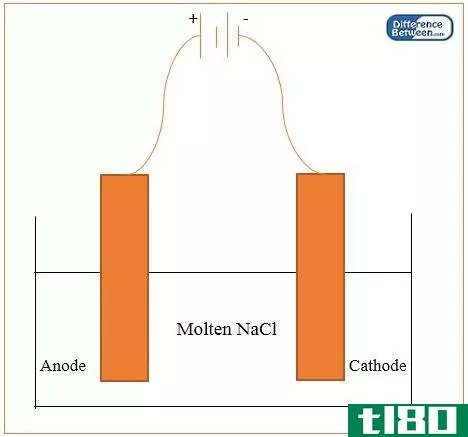
什么是电解槽?
这是一种利用电流来分解化合物,或者换句话说,进行电解的电池。所以电解电池需要外部的电能来工作。例如,如果我们把铜和银作为电池的两个电极,银就连接到外部能源(电池)的正极端子上。铜连接到负极端子。由于负端富含电子,因此电子从终端流向铜电极。所以铜被还原了。在银电极上,发生氧化反应,释放的电子被送到电池缺电子的正极端子上。以下是在一个有铜电极和银电极的电解槽中发生的整体反应。
2Ag+Cu2+(aq)⇌2Ag+(aq)+Cu(s)
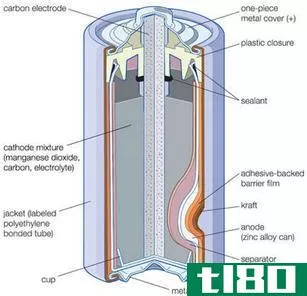
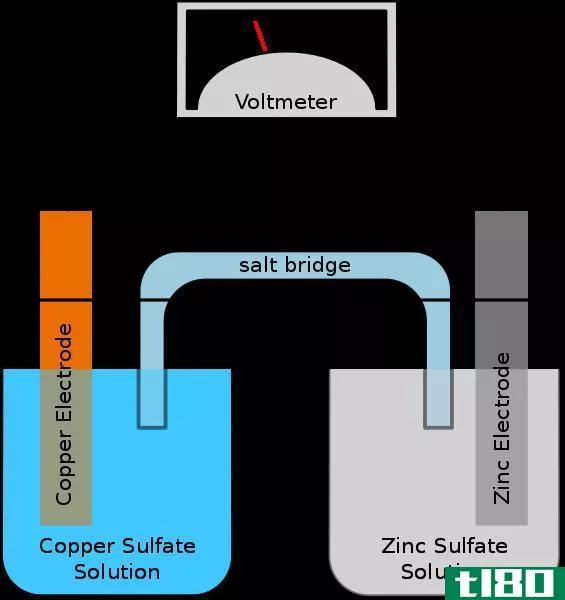
什么是原电池?
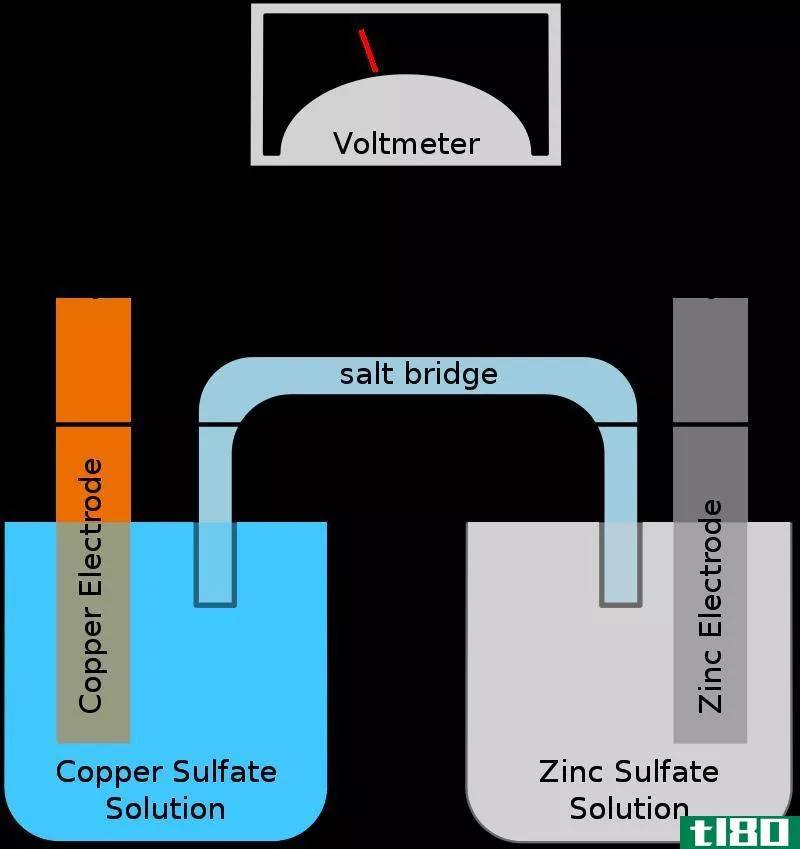
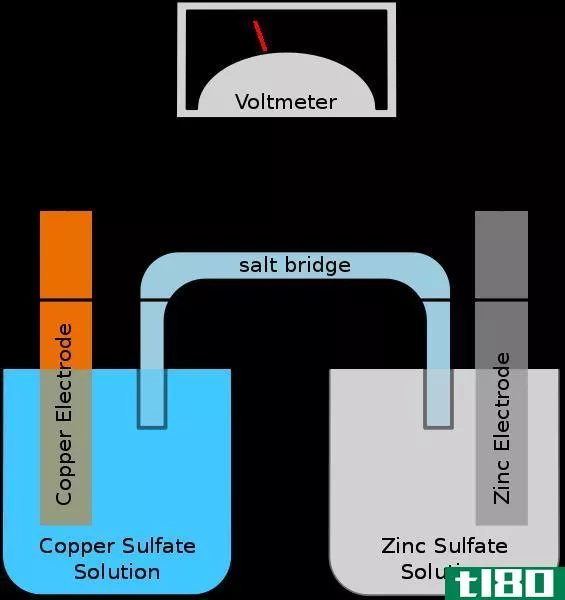
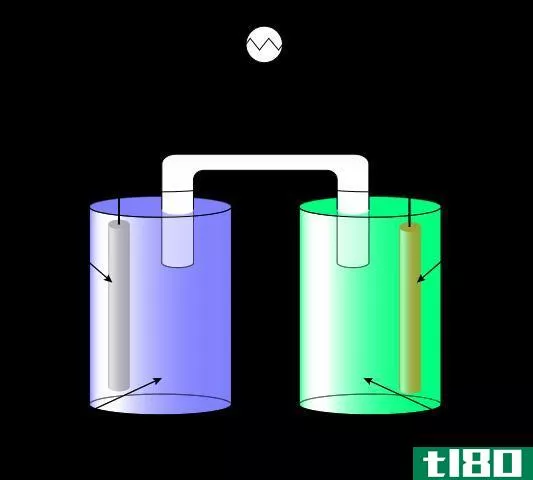
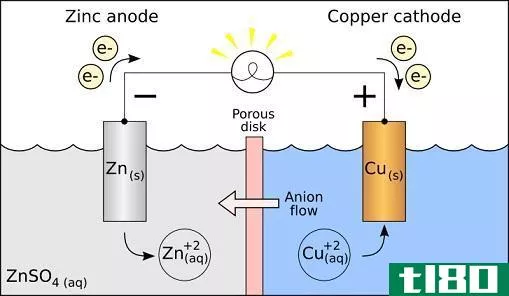
原电池或伏打电池储存电能。电池由一系列的原电池制成,以产生更高的电压。在原电池的两个电极上的反应倾向于自发进行。当反应发生时,会有电子通过外部导体从阳极流向阴极。例如,如果原电池中的两个电极是银和铜,则银电极相对于铜电极是正的。铜电极是阳极,它经过氧化反应并释放电子。这些电子通过外部电路进入银阴极。因此,银阴极发生还原反应。在允许电子流动的两个电极之间产生电位差。以下是上述原电池的自发细胞反应。
2银(aq)+Cu(s)⇌2Ag(s)+Cu2+(aq)
| 电解槽和原电池有什么区别?•电解槽的运行需要外部电能源,但原电池会自发地工作并发出电流。•在电解槽中,电流的方向与原电池中的方向相反。•两种类型的电池中,电极中的反应是相反的。在电解槽中,银电极是阳极,铜电极是阴极。然而,在原电池中,铜电极是阳极,银电极是阴极。•在电化学电池中,阴极是正的,阳极是负的。在电解槽中,阴极是负的,阳极是正的。•电解槽的操作需要比原电池更高的电压。 |