坚强的(strong)和弱电解质(weak electrolytes)的区别
主要区别强(main difference strong) vs. 弱电解质(weak electrolytes)
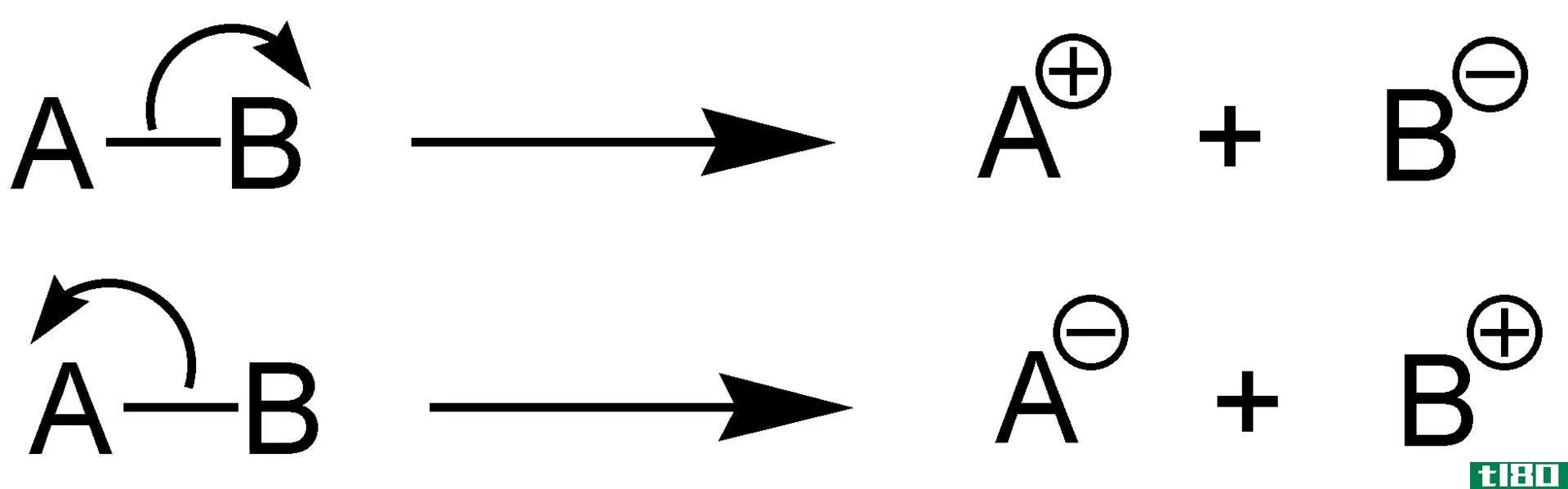
电解质是溶解在水中时产生离子的物质。三种主要电解质类型为酸、碱和盐,这些化合物在水中溶解时被分解成离子。正电荷和负电荷离子可以通过这些化合物的水溶液导电。有些电解质是强化合物,另一些是弱电解质。强电解质和弱电解质的主要区别在于,强电解质几乎完全分解成离子,而弱电解质则部分分解成离子。
覆盖的关键领域
1.什么是强电解质-定义、性质、反应2.什么是弱电解质-定义、性质、反应3.强电解质和弱电解质的区别是什么-主要区别的比较
Key Terms: Acids, Bases, Electrolytes, Salts, Strong Electrolytes, Weak Electrolytes
什么是强电解质(strong electrolytes)?
强电解质是一种化合物,当溶解在水中时,它可以完全分解成离子。因此,强电解质是一种完全溶解在水中的溶质。电解质由阳离子或正电荷离子、阴离子或负电荷离子组成。这些离子可以在溶液中传导电流。

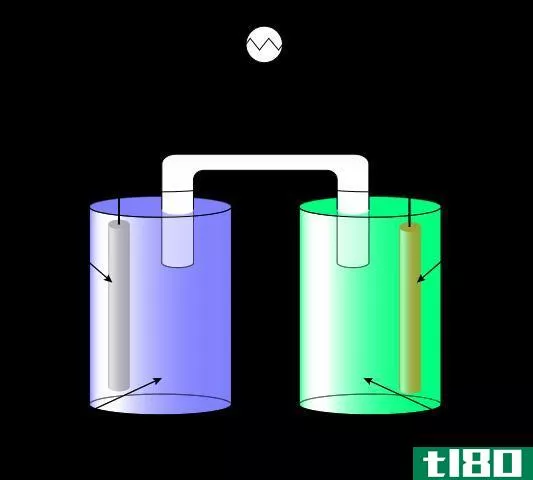
Figure 1: Strong Acids and Strong Bases are Strong Electrolytes
常见的强电解质有强酸、强碱和离子盐。然而,有些电解质不完全溶于水,但被认为是强电解质。这是因为溶解的量被完全电离成它的离子。
例如,强酸如HCl、HNO3是强电解质。这些被完全分解成阳离子H+和阴离子。像NaOH这样的强碱完全分解成能导电的离子。
什么是弱电解质(weak electrolytes)?
弱电解质是在水中溶解时部分分解成离子的化合物。弱电解质由阳离子和阴离子组成。与强电解质相比,这些化合物的离子性质较少。常见的弱电解质是弱酸、弱碱和盐。
通常,约1-10%的化合物分解成离子。大多数含氮化合物是弱电解质。水也被认为是弱电解质,因为水分子部分分解成H+和OH-离子。

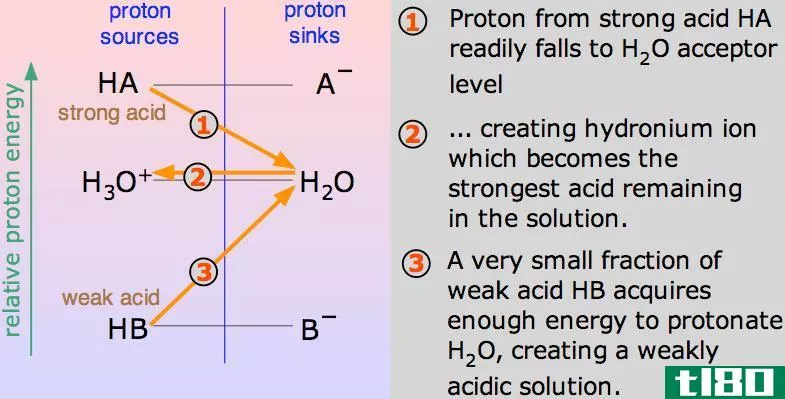
Figure 2: Water Molecules Partially Dissociate into Ion
由于这些弱电液部分溶解在水中,弱电液由分子、阳离子和阴离子组成。由于有几个带电离子,这些溶液可以传导电流。
一些常见的弱电解质是弱酸如H2CO3和弱碱如NH3。对于弱电解质,离解常数对于预测可通过溶液传导的电荷容量非常重要,因为化合物的离解形成可导电的可溶离子。
坚强的(strong)和弱电解质(weak electrolytes)的区别
定义
强电解质:强电解质是一种在水中溶解时能完全分解成离子的化合物。
弱电解质:弱电解质是在水中溶解时部分分解成离子的化合物。
离解
强电解质:强电解质能完全分解成离子。
弱电解质:弱电解质部分分解成离子。
示例
强电解质:强电解质是强酸、强碱和一些盐。
弱电解质:弱电解质是弱酸、弱碱和一些盐。
结论
电解质是一种能溶解在水中释放阳离子和阴离子的化合物。这些离子有助于通过溶液导电。强电解质和弱电解质的主要区别在于,强电解质几乎能完全解离成离子,而弱电解质部分解离成离子。
引用
1.“弱电解质:定义和示例”,Study.com,Study.com,可在此处获得。查阅日期:2017年9月15日。2.“电解质-强、弱和非电解质”,《科学笔记与项目》,2016年4月1日,可在此处查阅。2017年9月15日查阅。 2.“电解质-强、弱和非电解质”,《科学笔记与项目》,2016年4月1日,
- 发表于 2021-06-29 14:13
- 阅读 ( 286 )
- 分类:科学
你可能感兴趣的文章
是的(true)和电位电解液(potential electrolyte)的区别
...液与电位电解液的表格形式 5. 摘要 什么是真电解质(true electrolyte)? 真正的电解质是能完全分解成离子的物质。它们也被称为强电解质。这些化合物溶解在水或其他溶液中时容易产生离子形式。化合物解离后,溶液中既有阳离子...
- 发布于 2020-09-21 00:04
- 阅读 ( 237 )
电解质的综合性质(colligative properties of electrolytes)和非电解质(nonelectrolytes)的区别
...性 5. 摘要 什么是电解质的综合性质(colligative properties of electrolytes)? 电解液的综合性质是指电解质溶液的物理性质,它取决于溶质的数量,而不考虑溶质的性质。在电解质溶液中,或获得电子,或在电解质溶液中失去电子。 当...
- 发布于 2020-10-17 21:07
- 阅读 ( 271 )
强配体(strong ligand)和合配位子(weak ligand)的区别
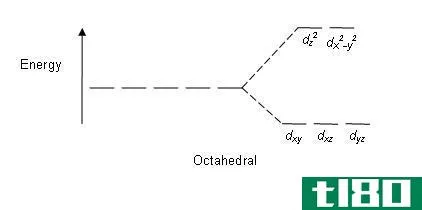
...处于较高能级,两个轨道处于较低能级。 什么是强配体(strong ligand)? 强配体或强场配体是一种能导致更高晶场分裂的配体。这意味着,一个强场配体的结合导致了高能级和低能级轨道之间的更大差异。例如CN–(氰化物配体)...
- 发布于 2020-10-19 12:13
- 阅读 ( 584 )
电解还原(electrolytic reduction)和精炼(refining)的区别
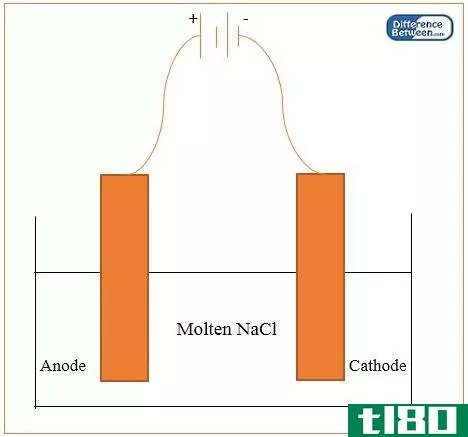
...较-电解还原与精炼的表格形式 5. 摘要 什么是电解还原(electrolytic reduction)? 电解还原是通过电解还原金属的过程。在这个过程中,我们使用两个大小相同的石墨电极作为阳极和阴极。该过程涉及金属(处于熔融状态)的氧化物...
- 发布于 2020-10-23 02:18
- 阅读 ( 293 )
电解质(electrolytes)和非电解质(nonelectrolytes)的区别
...较-电解液和非电解液的表格形式 5. 摘要 什么是电解质(electrolytes)? 电解质是产生离子的物质。这些化合物在熔融阶段或溶解在溶剂(水)中时会产生离子。因为有离子,电解质可以导电。还有固态电解质。此外,一些气体如二...
- 发布于 2020-11-06 17:55
- 阅读 ( 260 )
原电池(galvanic cells)和电解槽(electrolytic cells)的区别
...决于金属的反应性,即其溶解倾向。 什么是电解槽(electrolytic cell)? 通过电化学电池的电流可以通过两种方式启动。第一种方法是将电极和导体连接成闭合电路。通过闭合电路,可以在金属/电解液的两相上自发地诱发电极反...
- 发布于 2021-06-25 07:57
- 阅读 ( 586 )
坚强的(strong)和弱酸(weak acid)的区别
酸是一种化学物质,当混合在溶液中时会产生氢离子或质子。一种酸释放出的质子的数量实际上决定了酸的强度——无论是强酸还是弱酸。为了了解酸的强度,我们需要比较它们向类似的碱(主要是水)提供质子的倾向。强度由...
- 发布于 2021-06-25 16:37
- 阅读 ( 410 )
弱碱(weak base)和坚实的基础(strong base)的区别
...值就越低。所以较弱的碱有较低的平衡常数。 弱碱是弱电解质。 溶液导电的能力取决于离子的浓度。弱碱溶液中的离子比强碱溶液中的离子少,因此导电率较低。 弱碱的例子有: 丙氨酸 (C3H5O2NH2); 乙胺(C2H5NH2); 二甲胺...
- 发布于 2021-06-25 17:49
- 阅读 ( 294 )
坚强的(strong)和弱ai(weak ai)的区别
“人工智能”一词经常被误用或误解,但这项技术的好处大于坏处。人工智能领域的早期发展可能与今天无关,但这一过程多年来经历了重大变化。虽然人工智能被认为是最新的智力研究领域之一,但它的基础是在几千年前建立...
- 发布于 2021-06-26 12:17
- 阅读 ( 379 )
陶瓷(ceramic)和电解电容器(electrolytic capacitor)的区别
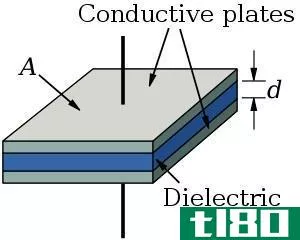
...积效率(单位体积的电容更多)。 什么是电解电容器(an electrolytic capacitor)? An electrolytic capacitor is a type of capacitor that uses an electrolyte in order to increase its capacitance. Typically aluminium, tantalum, or niobium acts as the conductive material. The dielectr...
- 发布于 2021-06-27 07:31
- 阅读 ( 486 )