配价(valency)和共价性(covalency)的区别
主差价(main difference valency) vs. 共价性(covalency)
原子是物质的组成部分。每个原子都由一个原子核和一个电子云组成。原子核是原子的核心,被电子云所包围。电子云的概念是根据电子位置的概率演化而来的。这意味着电子总是绕着原子核运动。这个路径被称为轨道或壳层。据说电子是沿着这些轨道运动的。价态和共价态是两个与原子中存在的电子数有关的项。价态和共价态之间的主要区别在于,价态是原子为了稳定自身而失去或获得的电子数,而共价态是原子利用其空轨道可以形成的最大共价键数。
覆盖的关键领域
1.什么是价-定义、性质、示例2.什么是共价-定义、性质、示例3.价和共价之间的区别是什么-关键区别的比较
Key Terms: Atom, Covalency, Covalent Bond, Electron, Orbital, Shell, Valency
什么是配价(valency)?
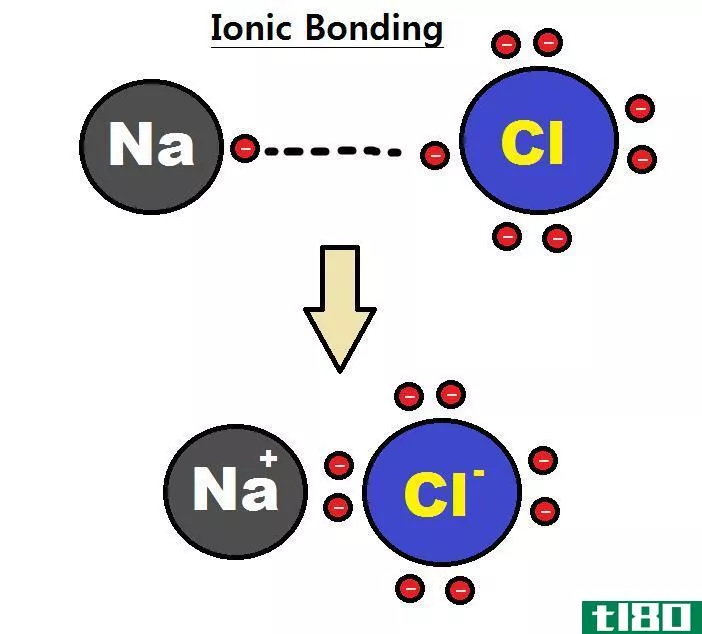
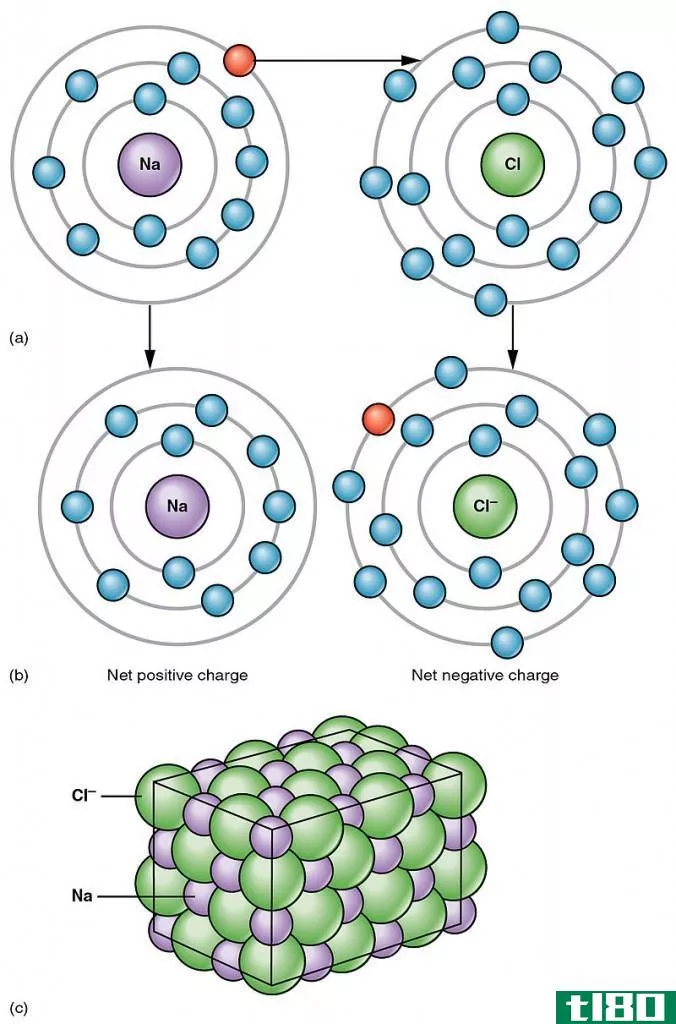
价态可以定义为原子为了稳定自身而失去或获得的电子数。原子最外层轨道上的电子称为价电子。有时,价电子的数目被认为是该元素的价。例如,氢的价态(H)是1,因为氢原子可以通过失去或获得1个电子而稳定。氯原子在最外层轨道上有7个电子(价电子数为7),但再获得1个电子,就可以得到更稳定的氩(Ar)的惰性气体电子构型。得到一个电子比损失7个电子容易,所以氯的价态被认为是1。
元素的电子构型决定了特定元素的价态。下表显示了一些元素及其值。
| 元素 | 电子构型 | 为了遵守八位元规则而需要获得或释放的电子 | 配价 |
| 钠(Na) | 1s22s22p63s1型 | (-)1 | 1 |
| 钙(Ca) | 1S222S2P63S2**64S2 | (-)2 | 2 |
| 氮(N) | 第22页 | (+)3 | 三 |
| 氯(Cl) | 1S222S2P63S2**5型 | (+)1 | 1 |
上表显示了一些元素的价态。在那里,(-)标记表示为了得到稳定必须去除的电子数。(+)标记表示为了稳定而必须获得的电子数。

Figure 1: The periodic table of elements
除此之外,元素周期表还可以给出元素的价态。第一组元素的价总是1,第二组元素的价是2。
什么是共价性(covalency)?
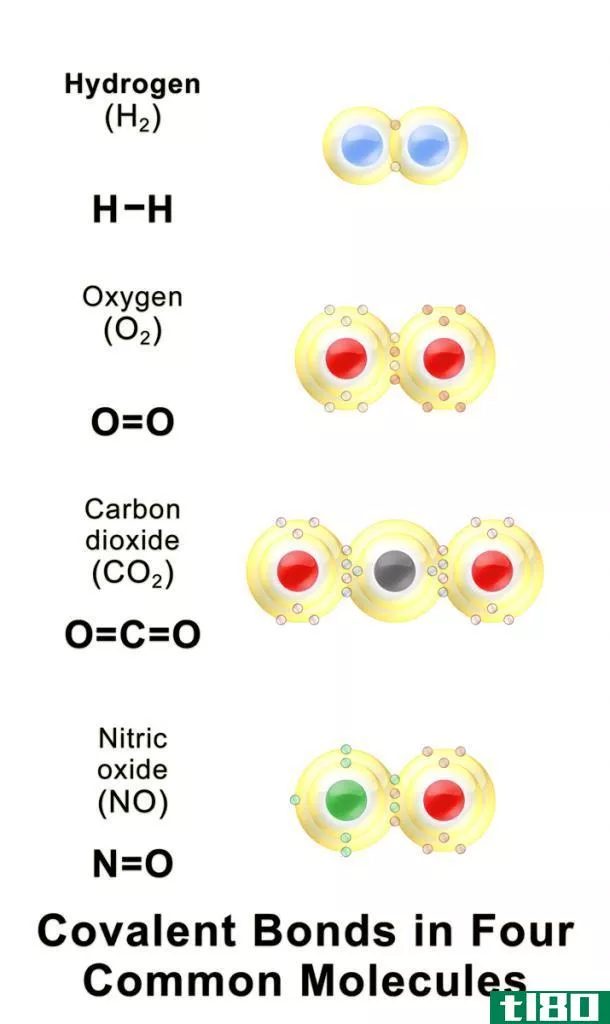
共价性是原子利用其空轨道可以形成的最大共价键数。共价性取决于元素的价电子数。例如,氢中存在的价电子数为1,氢的共价性也为1,因为它只有一个电子可以与另一个原子共享以形成共价键。
如果考虑碳等元素,碳的电子构型为1s22s22p2。碳的价电子数是4,它有空的p轨道。因此,2s轨道上的两个s电子可以分离并包含在这些p轨道中。碳中有4个未配对的电子。因此,为了形成共价键,碳有4个电子可以共享。因此,碳的共价性是4。这是一个碳原子能拥有的最大共价键数。下面的轨道图解释了这一点。
The valence electr*** of carbon;
The spread of electr*** to the empty orbitals;
现在有4个未配对的电子供碳与其他原子共享,以形成共价键。
配价(valency)和共价性(covalency)的区别
定义
价:价是原子为了稳定自身而失去或获得的电子数。
共价性:共价性是原子利用其空轨道可以形成的最大共价键数。
与价电子的关系
价:价可以等于或不等于价电子的数目。
共价性:共价性取决于价电子的数目。
空轨道
价态:价态给出了填充空轨道所需的电子数。
共价性:共价性取决于原子中存在的空轨道数。
粘结类型
化合价:可以给出形成离子键或共价键的元素的化合价。
共价性:共价性只适用于能形成共价键的元素。
结论
原子价有时可能等于原子的价电子数,但多数情况下它们是不同的。然而,共价性完全取决于原子的价电子数。这是因为价电子决定了一个原子能有多少共价键。因此,了解价态和共价态之间的区别是很重要的。
引用
1.“共价性”,化学共价性和分子结构。N.p.,N.d.网站。这里有。2017年7月18日。 2.“价态(化学)。”维基百科。维基媒体基金会,2017年7月8日。这里有。2017年7月18日。 2.“价态(化学)。”维基百科。维基媒体基金会,2017年7月8日。
- 发表于 2021-06-29 08:25
- 阅读 ( 357 )
- 分类:科学
你可能感兴趣的文章
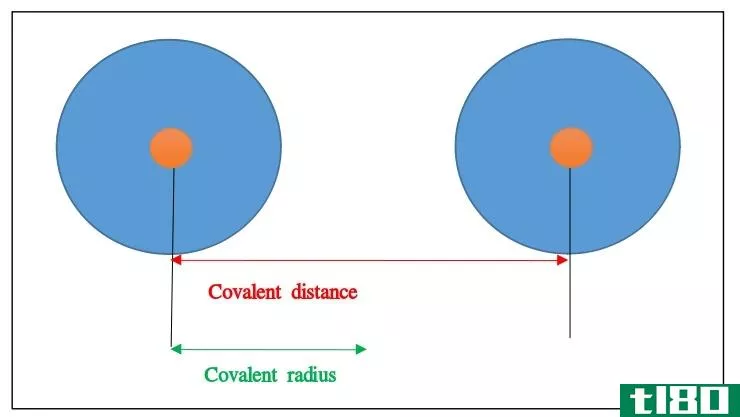
共价半径(covalent radius)和金属半径(metallic radius)的区别
共价半径和金属半径的关键区别在于共价半径是处于共价键中的两个同核原子之间距离的一半,而金属半径是金属结构中两个相邻金属离子之间距离的一半。 共价半径和金属半径都是原子核之间距离的一半;在共价半径中,...
- 发布于 2020-10-16 21:04
- 阅读 ( 746 )
电价(electrovalency)和共价性(covalency)的区别
价性和共价性的关键区别在于,价态是一个原子在形成离子时获得或损失的电子数,而共价性是一个原子可以与另一个原子共享的电子数。 尽管电价和共价这两个术语听起来很相似,但根据它们的定义,它们是不同的。主要...
- 发布于 2020-10-17 17:36
- 阅读 ( 301 )
电价的(electrovalent)和共价键(covalent bond)的区别
电子价键和共价键的关键区别在于,电子价键是通过将电子从一个原子转移到另一个原子而产生的,而共价键则是原子间共享价电子的结果。离子键也叫价键。价电子是位于原子最外层的电子,参与两种化学键合。 化学键合...
- 发布于 2020-10-23 11:30
- 阅读 ( 342 )
共价性(covalency)和氧化态(oxidation state)的区别
共价性(covalency)和氧化态(oxidation state)的区别 不同化学元素的原子相互结合形成不同的化合物。在化合物的形成过程中,原子通过离子键或共价键相互结合。共价态和氧化态是描述化合物中这些原子状态的两个术语。共价性是...
- 发布于 2020-10-24 02:21
- 阅读 ( 288 )
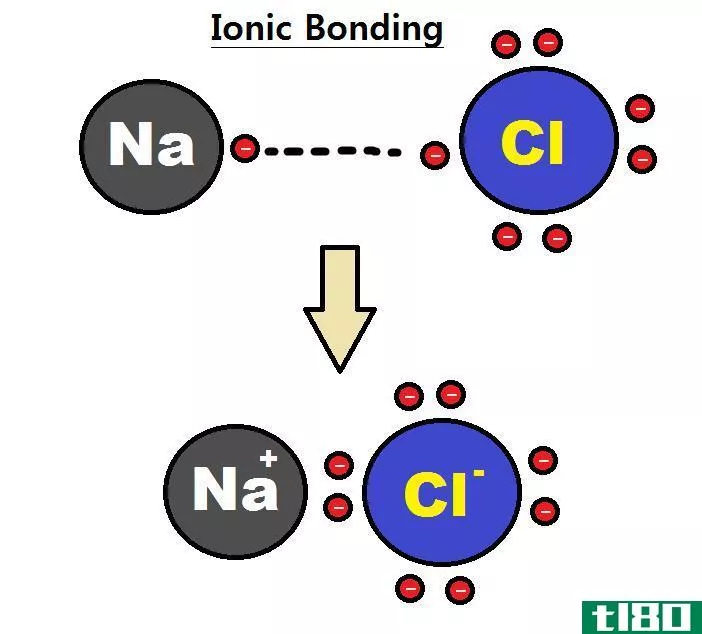
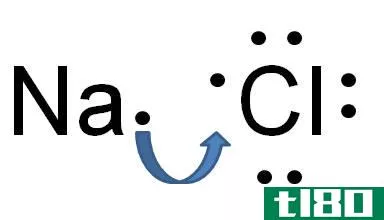
离子型(ionic)和共价化合物(covalent compounds)的区别
...。 离子化合物的例子是Na++Cl–a NaCl Sodium(metal) has only one valence electron and Chlorine (non-metal) has seven valence electr***. 什么是共价化合物(covalent compounds)? 共价化合物是由两个或多个原子共享电子而形成的,以满足“八位体规则”。...
- 发布于 2020-10-24 16:55
- 阅读 ( 488 )
离子共价(ionic covalent)和氢化物(metallic hydrides)的区别
离子共价和金属氢化物之间的关键区别在于它们的形成。当氢与高电正性s-块元素反应时形成离子氢化物;当具有可比电负性值的化学元素的原子与氢反应时形成共价氢化物,而当过渡金属与氢反应时形成金属氢化物。 氢化...
- 发布于 2021-03-04 17:20
- 阅读 ( 426 )
共价的(covalent)和离子键(ionic bonds)的区别
主要差异共价(main difference covalent) vs. 离子键(ionic bonds) 元素的本质是在它们之间形成键,以便变得稳定。共价键和离子键是元素相互结合的两种不同方式。共价键和离子键的主要区别在于,离子键发生在静电相互吸引的...
- 发布于 2021-06-27 08:52
- 阅读 ( 1724 )
配价(valency)和价电子(valence electrons)的区别
...键的数目,而价电子是参与这种键形成的电子。 什么是配价(valency)? 根据IUPAC的定义,价态是“可能与所考虑元素的一个原子结合,或与一个片段结合,或该元素的一个原子可以被取代的一价原子(最初为氢原子或氯原子)的...
- 发布于 2021-06-27 10:49
- 阅读 ( 593 )
离子共价(ionic covalent)和金属键(metallic bonds)的区别
...(covalent bonds)? Covalent bonds are formed when two atoms share their valence electr***. The two atoms have a **all difference in electronegativity. Covalent bonds occur between same atoms or different types of atoms. For example, fluorine needs one electron to complete its outer shell, thus, one...
- 发布于 2021-06-28 11:41
- 阅读 ( 808 )
配价(valency)和共价性(covalency)的区别
...Atom, Covalency, Covalent Bond, Electron, Orbital, Shell, Valency 什么是配价(valency)? 价态可以定义为原子为了稳定自身而失去或获得的电子数。原子最外层轨道上的电子称为价电子。有时,价电子的数目被认为是该元素的价。例如,氢的价...
- 发布于 2021-06-29 08:25
- 阅读 ( 357 )