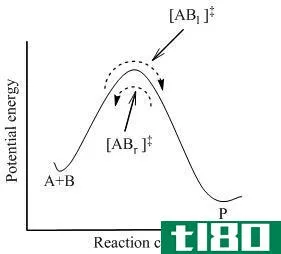
关键区别-碰撞理论与过渡状态理论
碰撞理论和过渡态理论是在分子水平上解释不同化学反应速率的两种理论。碰撞理论描述了气相化学反应中气体分子的碰撞。过渡态理论通过假设过渡态中间化合物的形成来解释反应速率。碰撞理论与过渡态理论的主要区别在于,碰撞理论涉及气体分子之间的碰撞,而过渡态理论则涉及过渡态中中间化合物的形成。
目录
1. 概述和主要区别
2. 什么是碰撞理论
3. 什么是过渡态理论
4. 并列比较-碰撞理论与过渡状态理论的表格形式
5. 摘要
什么是碰撞理论(collision theory)?
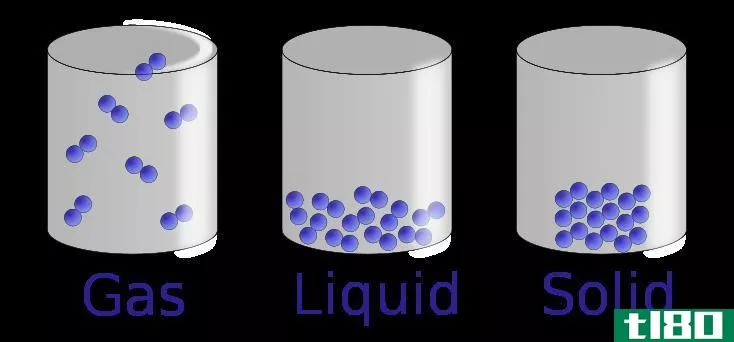
碰撞理论解释了分子与足够动能碰撞时发生气相化学反应。该理论是基于气体动力学理论建立的(气体动力学理论描述气体中含有没有定义体积但具有定义质量且这些气体颗粒之间没有分子间吸引或排斥的粒子)。
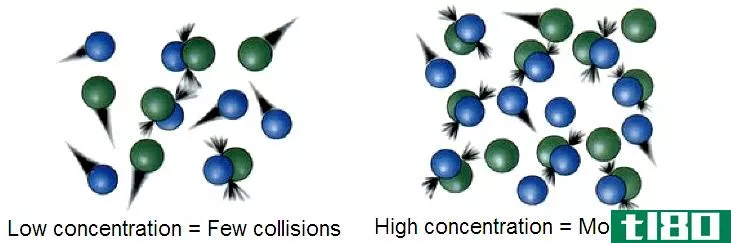
图01:如果在一个小体积中有许多气体颗粒,那么浓度很高,那么两个气体颗粒碰撞的概率就很高。这会导致大量的成功碰撞
根据碰撞理论,气体粒子之间只有很少的碰撞会使这些粒子发生相当大的化学反应。这些碰撞称为成功碰撞。这些成功碰撞所需的能量称为活化能。这些碰撞会导致化学键的断裂和形成。
什么是过渡态理论(transition state theory)?
过渡态理论指出,在分子是反应物的状态和分子是产物的状态之间,存在一种称为过渡态的状态。过渡态理论可以用来确定基本反应的反应速率。根据这一理论,反应物、产物和过渡态化合物之间处于化学平衡状态。
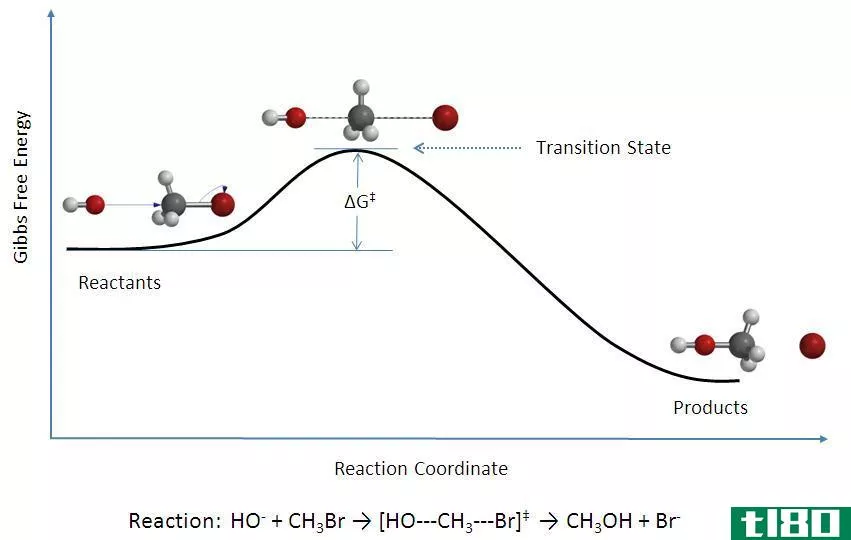
图02:显示反应物、产物和过渡态络合物的图
过渡态理论可以用来理解基本化学反应的机理。这个理论是一个更精确的替代阿伦尼斯方程。根据过渡态理论,影响反应机理的主要因素有三个;
- 过渡态化合物(称为活化络合物)的浓度
- 活化复合物的分解速率-这决定了所需产物的形成速率
- 活化复合物的分解方式决定了化学反应中生成的产物
然而,根据这一理论,化学反应有两种途径:活化的络合物可能会回到反应物的形式,也可能会因分解而形成产物。反应物能量和过渡态能量之间的能量差称为活化能。
碰撞理论(collision theory)和过渡态理论(transition state theory)的区别
| 碰撞理论与过渡态理论 | |
| 碰撞理论解释了当分子以足够的动能碰撞时,会发生气相化学反应。 | 过渡态理论指出,在分子是反应物的状态和分子是产物的状态之间,存在一种称为过渡态的状态。 |
| 原则 | |
| 碰撞理论认为化学反应(在气相中)是由于反应物之间的碰撞而发生的。 | 过渡态理论认为化学反应是通过过渡态发生的。 |
| 要求 | |
| 根据碰撞理论,只有成功的碰撞才会导致化学反应的发生。 | 根据过渡态理论,如果反应物能克服活化能垒,化学反应就会进行。 |
总结 - 碰撞理论(collision theory) vs. 过渡态理论(transition state theory)
用碰撞理论和过渡态理论解释了不同化学反应的反应速率和机理。碰撞理论与过渡态理论的区别在于,碰撞理论涉及气体分子之间的碰撞,而过渡态理论则涉及过渡态中间化合物的形成。
引用
1.“碰撞理论”,《化学歌词》,歌词,2017年5月22日。此处提供2.“过渡状态理论”,维基百科,维基媒体基金会,2018年2月28日。可在这里查阅3.“9.7:反应速率理论”,化学图书馆,图书馆,2016年7月21日。此处提供
2.“过渡状态理论”,维基百科,维基媒体基金会,2018年2月28日。
3.“9.7:反应速率理论”,《化学图书馆》,图书馆,2016年7月21日。