主要区别
金属和类金属之间的主要区别在于,金属被认为是包含极低电负性值的元素,而类金属是被认为包含电负性中间值的元素。
金属(metals) vs. 类金属(metalloids)
金属被称为能够表现出最高程度金属行为的元素。另一方面,类金属是指能够表现出较低程度金属行为的元素。
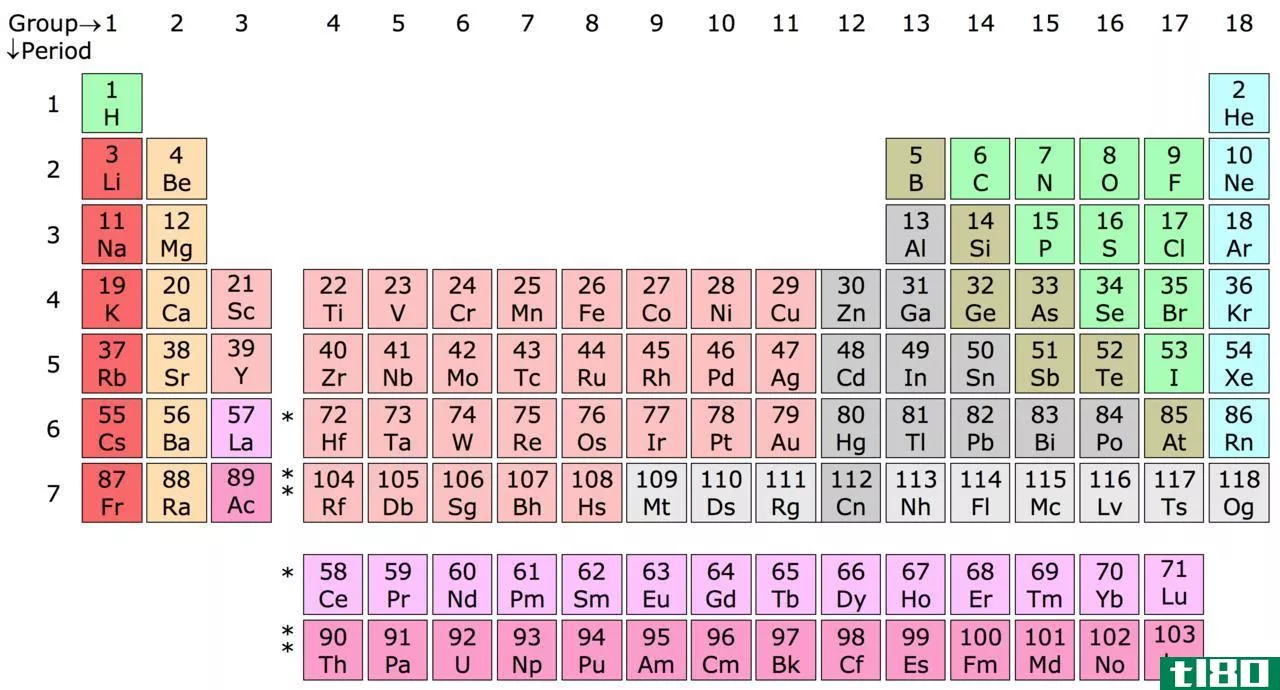
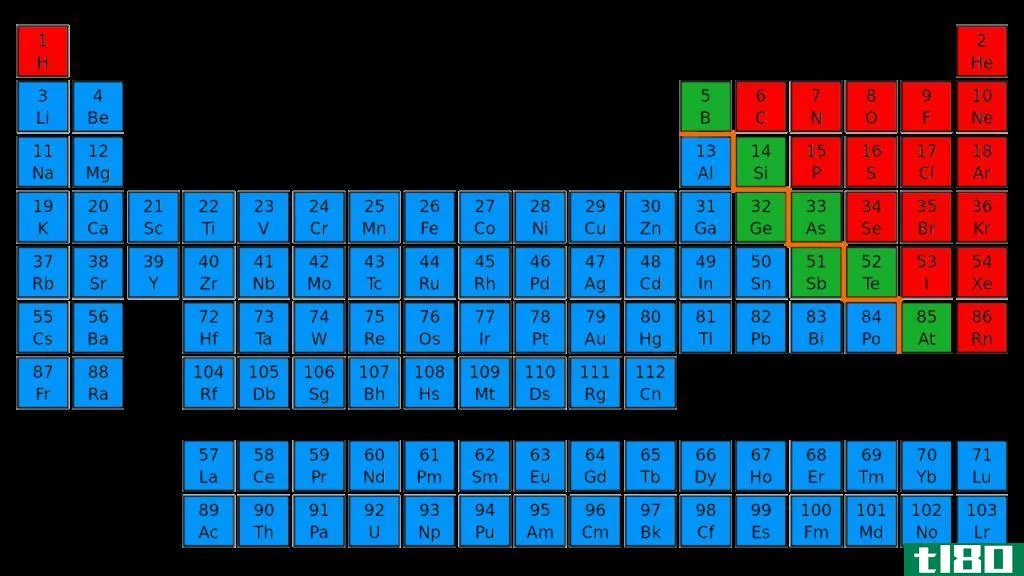
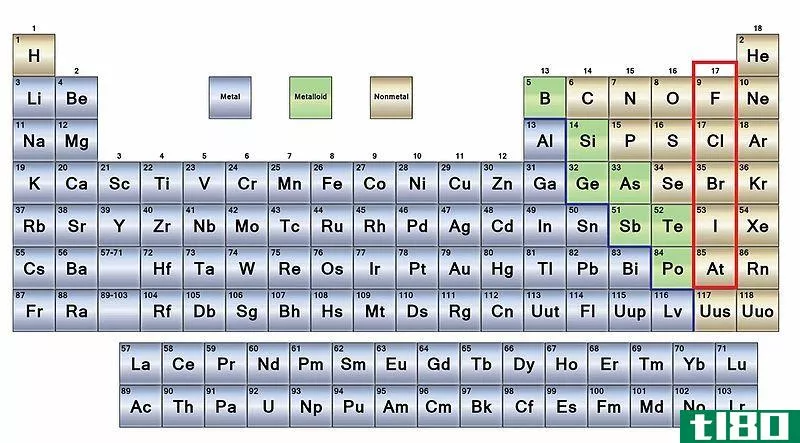
在元素周期表中,金属被认为位于左侧。另一方面,类金属被认为位于周期表中金属与非金属分离的地方。
在化学反应中,金属被称为容易失去电子的元素。另一方面,类金属是在化学反应中失去或获得电子的元素。钠、铁、锡和钚是金属的一些例子。硅、硼和砷是类金属的一些例子。
比较图
什么是金属(the metals)?
元素周期表中含有最高程度金属行为的元素被称为金属。金属被认为存在于元素周期表的左边。光泽或光泽是指元素周期表中这些元素特有的金属外观。塑性和延展性是金属的主要特征。
金属在压力下变形的能力被称为延展性,而金属被拉伸成线状结构的能力称为延展性。当我们讨论金属的状态时,我们知道在室温下,它们通常是固体。但汞元素被认为是一个例外情况。
尽管汞被称为一种金属元素,但在室温下,它以液态形式存在,因为元素周期表中所有剩余的金属通常都具有较高的熔点。当我们比较汞原子和金属原子时,我们发现它们被称为相互共享电子的弱原子。这就是它们之间显示出弱相互作用的原因。
由于上述原因,汞原子很容易逃逸,因此显示出较低的熔点。金属被称为热和电的优良导体,因为它们容易丢失电子,因此能够参与导电。简而言之,我们可以说金属中存在自由电子。
在盐水和潮湿条件下,金属被认为会受到腐蚀。金属元素被认为存在于元素周期表的所有s、p、d和f块中。元素周期表中金属的最外层的s和p轨道(除了少数金属)中存在的电子数量较少。
阳离子通常由金属形成。因此,金属的氧化数几乎保持为正值。金属表现出极低的电负性,因此能够形成离子化合物。钠、铁、锡和钚被称为金属的一些例子。
什么是类金属(metalloids)?
元素周期表中含有低程度金属行为的元素称为金属。类金属元素是周期表中能够显示某些金属和非金属性质的元素。类金属可能具有暗淡或闪亮的外观。延展性和延展性不在元素周期表的这些类型中显示出来。
半导体的生产被称为类金属的主要应用。在室温下,所有类金属都被认为是固体。我们发现在金属和非金属之间的类金属密度。它们被称为周期表中的脆性元素。类金属被认为存在于周期表的p块中。
类金属是指元素周期表中位于元素周期表中金属和非金属之间的元素。中等数量的电子存在于s和p轨道中。类金属参与电和热的传导,尽管它们不被认为是优秀的电导体和热导体。
类金属能够形成共价键,因此,人们认为它们存在于共价化合物中。众所周知,类金属在室温下以固态存在,因此被认为具有高熔点。类金属能在水溶液中形成阴离子。
由于类金属具有形成阴离子的能力,所以它们可以显示负或正氧化数。类金属被称为周期表中能够在化学反应中失去或获得电子的元素。硅、硼和砷被认为是类金属的一些例子。
主要区别
- 周期表中被认为包含极低电负性值的元素称为金属,而元素周期表中被认为包含电负性中间值的元素称为类金属。
- 在元素周期表中,金属被视为位于元素周期表左侧的元素;而类金属元素则被视为位于周期表中间的元素。
- 金属行为的最高程度被认为是由金属表现出来的。相反,低程度的金属行为,被认为是由类金属表现出来的。
- 金属被称为周期表中被认为存在于s、p、d和f块中的元素;相反,类金属被称为周期表中被认为存在于p块中的元素。
- 金属被认为是元素周期表的组成部分,有光泽的外观,另一方面,类金属被认为是元素周期表的元素,可能包含暗淡或有光泽的外观。
- 可锻性被认为是由金属表现出来的,而可锻性不是由类金属表现出来的。
- 韧性被认为是由金属表现出来的;另一方面,延展性不是由类金属表现出来的。
- 金属表现出很高的热导率,而类金属表现出良好的导热性。
- 金属表现出很高的导电性,在另一方面,非金属则表现出良好的导电性。
- 除钾、钠、钙外,其余金属一般都是高密度的;另一方面,我们发现类金属的密度介于金属和非金属之间。
- 钠、铁、锡和钚被称为金属的一些例子,而硅、硼和砷则被称为类金属的一些例子。
- 在化学反应中,金属被称为容易失去电子的元素,另一方面,类金属是周期表中能够在化学反应中失去或获得电子的元素。
对比视频
结论
所有上述讨论的结论是,金属和类金属都被称为地球上存在的元素。前者是元素周期表中涉及显示最高程度金属行为的元素,另一方面,后者是元素周期表中涉及显示低程度金属行为的元素。