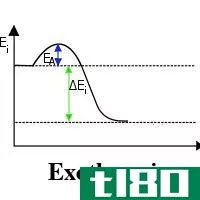
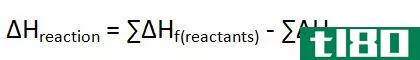吸热反应和放热反应的关键区别在于吸热反应吸收周围环境的能量,而放热反应则向周围环境释放能量。
能量是做功的能力。在一个系统中,能量可以做功;它可以转变成其他形式,如热、声、光等。当系统的能量因系统与周围环境之间的温差而改变时,我们称之为能量以热的形式传递。吸热反应是从周围环境向系统获取能量的过程,而放热反应是从系统向周围释放能量的过程。
目录
1. 概述和主要区别
2. 什么是吸热反应
3. 什么是放热反应
4. 并列比较-吸热反应和放热反应的表格形式
5. 摘要
什么是吸热反应(endothermic reacti***)?
吸热反应是一个以热的形式从周围获得能量的过程。如果周围没有热量供应,反应就不会发生。在这个反应过程中,反应容器会变冷,因为它从周围环境中吸收热量,从而降低温度。
要打破化学键,它需要能量。在吸热反应中,反应物的键断裂能大于产物的总成键能。因此,焓变为正值,反应不是自发的。因此,对于吸热反应,我们必须从外部提供能量。
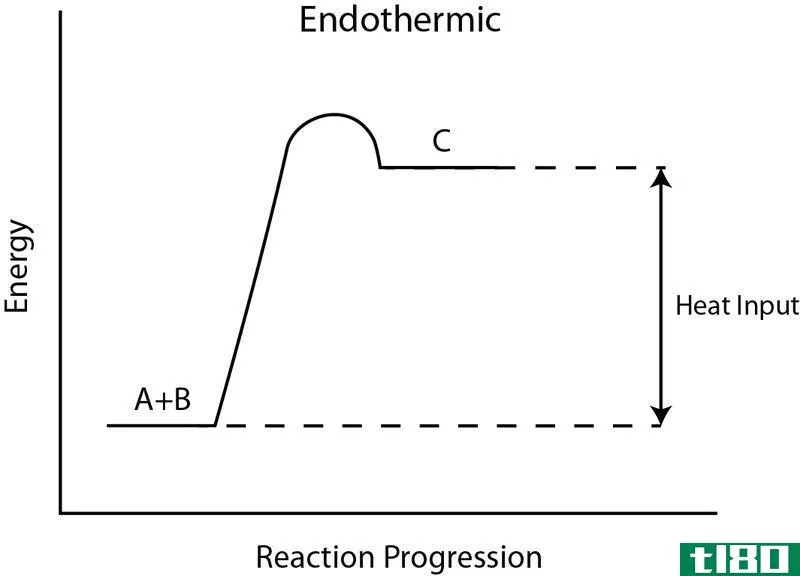
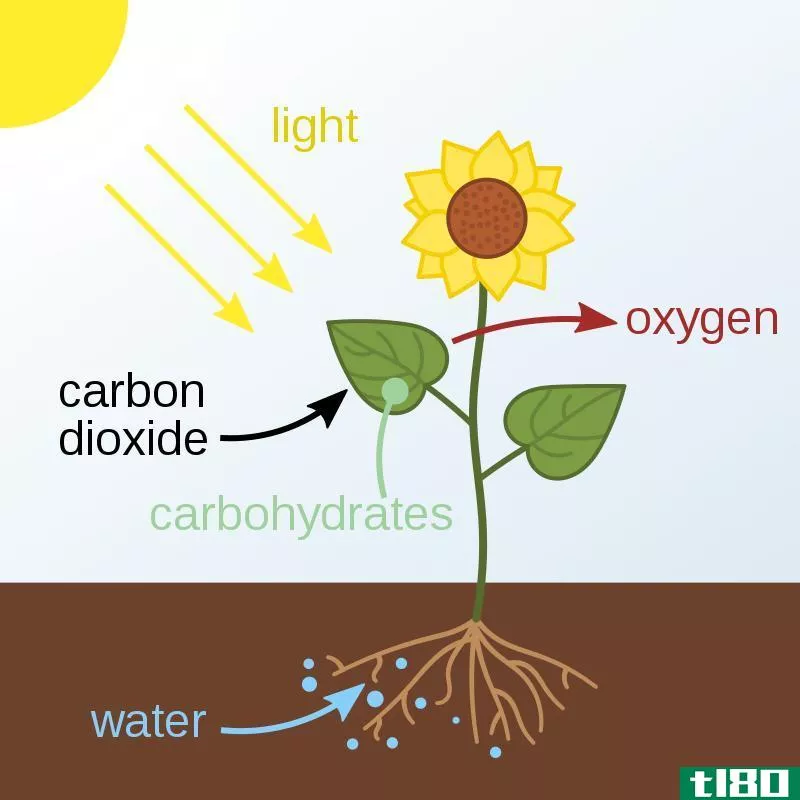
例如,当氯化铵溶解在水中时,烧杯会变冷,因为溶液会吸收外界环境的能量。光合作用是发生在自然环境中的吸热反应。对于光合作用,阳光提供所需的能量。
什么是放热反应(exothermic reacti***)?
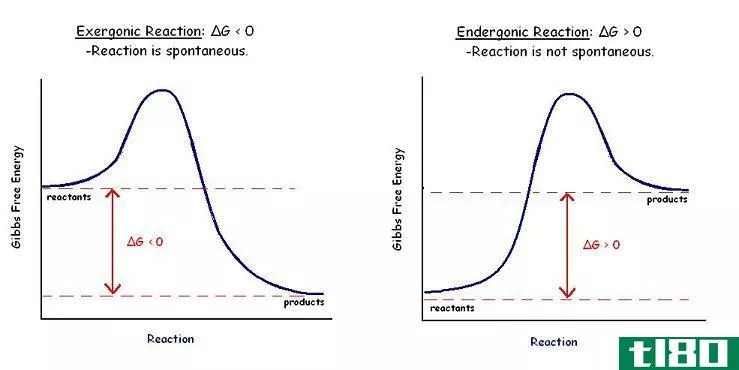
放热反应是一个向周围环境释放能量的过程,通常是以热的形式。此外,能量也可能以声音、光等其他形式释放。由于能量是在反应过程中释放的,因此产物所含能量比反应物少。因此,焓变(∆H)变为负值。
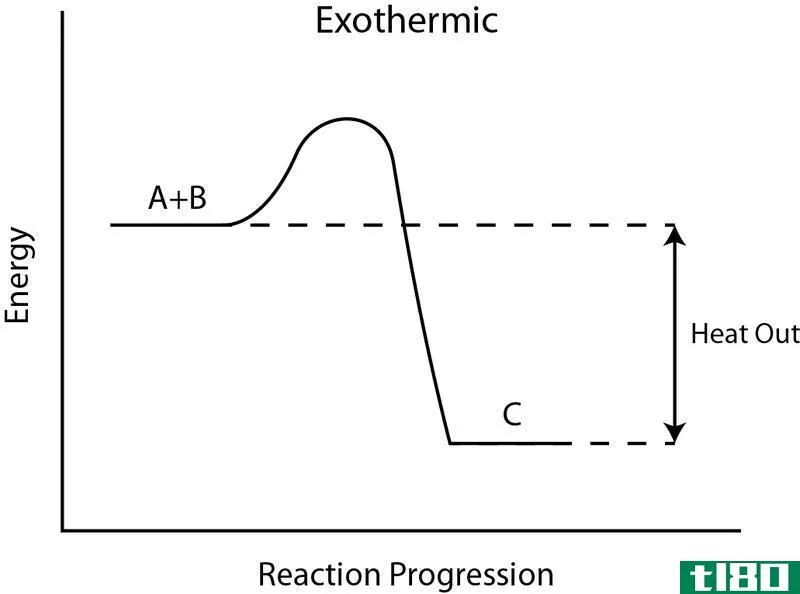
在这种反应中,能量在键形成过程中释放出来。如果反应过程中总成键能大于键断裂能,则为放热。如果能量以热的形式释放出来,周围的温度就会升高,因此反应有时会爆炸。放热反应是自发的。放热反应不需要外部能量供应,因为它们在反应进行时会产生所需的能量。然而,要开始反应,可能需要初始能量供应。
如果我们能捕捉到释放出来的能量,我们就可以把它用于很多有用的工作。例如,燃料燃烧所释放的能量在操作车辆或机器时是有用的。此外,所有的燃烧反应都是放热的。
吸热的(endothermic)和放热反应(exothermic reacti***)的区别
吸热和放热是与热力学系统中的传热有关的术语。吸热反应和放热反应的关键区别在于吸热反应吸收周围环境的能量,而放热反应则向周围环境释放能量。此外,吸热过程中的焓变化是正的,而放热过程中的焓变化是负的。当考虑最终产物时,吸热反应的产物比反应物的能量高,而在放热反应中,产物的能量比反应物的能量低。
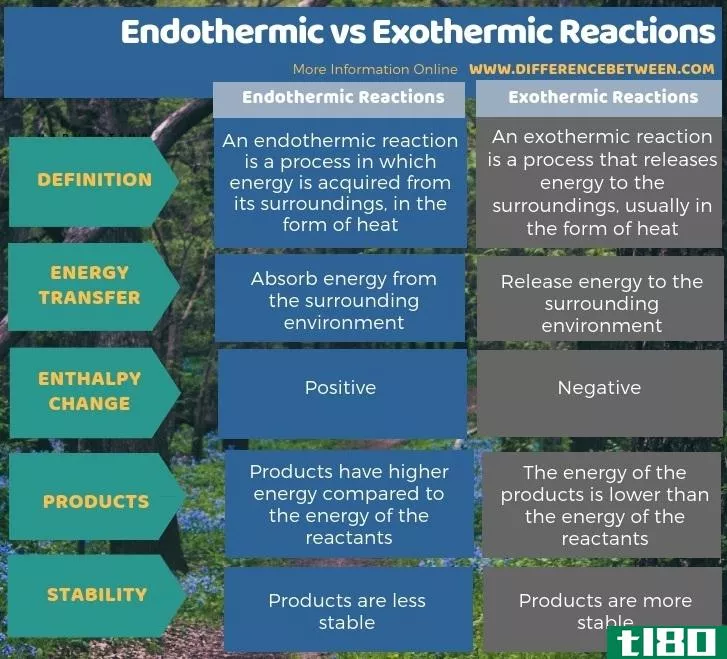
总结 - 吸热的(endothermic) vs. 放热反应(exothermic reacti***)
吸热和放热是与热力学系统中的传热有关的术语。吸热反应和放热反应的关键区别在于吸热反应吸收周围环境的能量,而放热反应则向周围环境释放能量。
引用
赫尔曼斯汀,安妮·玛丽。“吸热反应实例”,ThoughtCo,May。2019年9月9日,可在这里购买。