共振和π共轭的关键区别在于共振是指分子在离域电子存在下的稳定性,而π共轭是指π电子分布在分子的整个区域,而不是属于分子中的单个原子。
共振和π共轭是密切相关的术语,因为π共轭在化合物中引起共振。
目录
1. 概述和主要区别
2. 什么是共振
3. 什么是π共轭
4. 并列比较-共振与π共轭的表格形式
5. 摘要
什么是共振(resonance)?
共振是描述化合物中孤电子对和键电子对之间相互作用的化学概念。一般来说,共振效应有助于确定有机或无机化合物的实际化学结构。这种效应也出现在含有双键和孤电子对的化合物中。此外,这种效应会引起分子的极性。
共振表明化合物通过pi键中的离域电子而稳定。在这里,分子中的电子可以绕原子核运动,因为电子在原子内没有固定的位置。因此,孤电子对能够移动到π键,反之亦然。这样做是为了获得一个稳定的状态。这种电子运动过程称为共振。此外,我们可以利用共振结构来获得最稳定的分子结构。
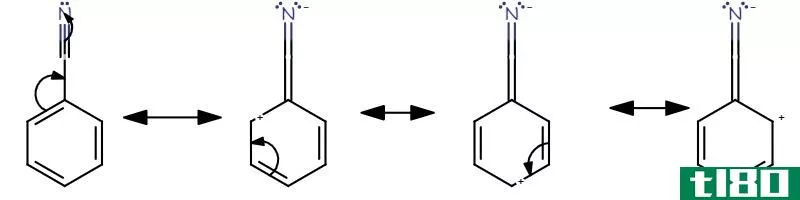
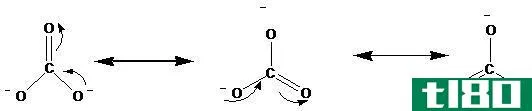
图01:苯甲腈中的共振
根据分子中存在的孤对和π键的数目,一个分子可以有几个共振结构。一个分子的所有共振结构都有相同数量的电子和相同的原子排列。该分子的实际结构是所有共振结构中的杂化结构。共振效应有两种类型:正共振效应和负共振效应。
正共振效应解释了具有正电荷的化合物中的共振现象。正共振效应有助于稳定分子中的正电荷。负共振效应解释了分子中负电荷的稳定。然而,考虑共振的混合结构比所有共振结构具有更低的能量。
什么是π共轭(π conjugation)?
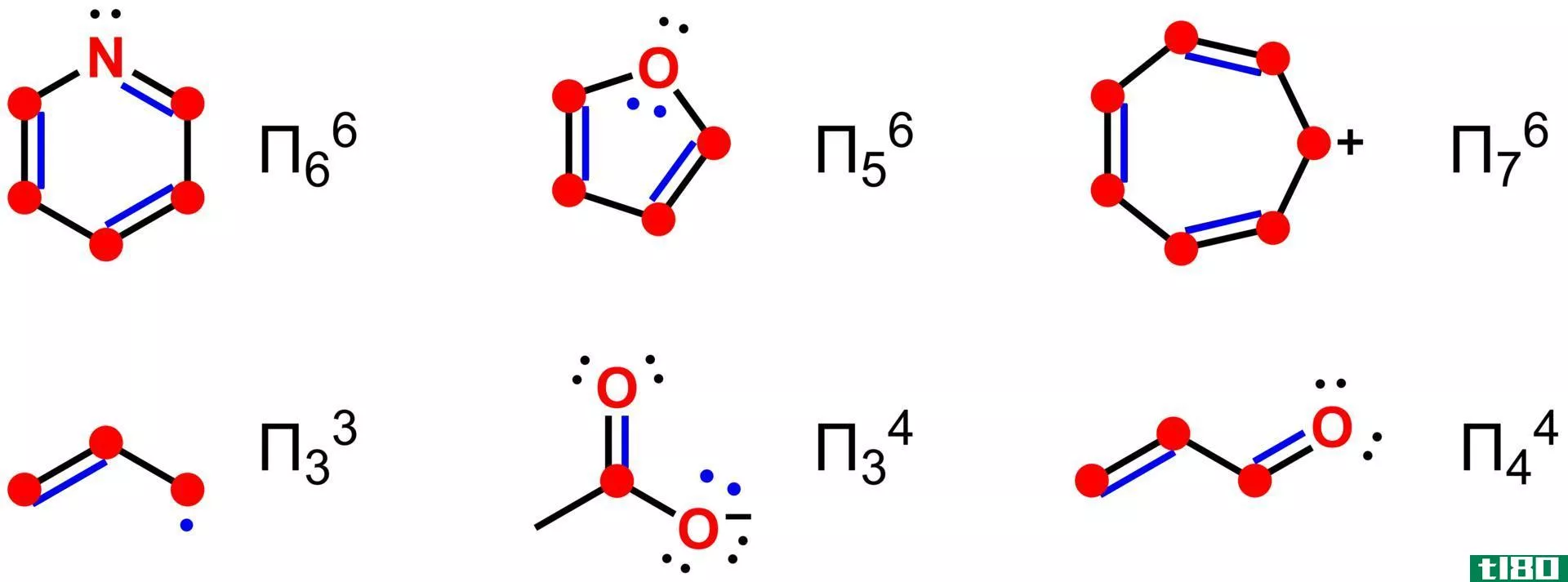
π共轭一词是指有机化合物中的离域作用,我们可以观察到非键π电子在分子中的分布。因此,我们可以把π共轭体系中的电子描述为化合物中的非键电子。此外,这个术语指的是与单个原子或共价键无关的电子。
作为一个简单的例子,我们可以把苯作为一个具有离域电子的芳香体系。一般来说,一个苯环在苯分子中有六个π电子,我们通常用圆圈来表示。这个圆意味着π电子与分子中的所有原子相关联。这种离域作用使苯环上的化学键具有相似的键长。
共振(resonance)和π共轭(π conjugation)的区别
共振和π共轭是密切相关的术语。共振和π共轭的关键区别在于,共振是指分子在离域电子存在下的稳定性,而π共轭是指π电子分布在分子的整个区域,而不是属于分子中的单个原子。
下面的信息图表以表格形式总结了共振和π共轭之间的区别。
总结 - 共振(resonance) vs. π共轭(π conjugation)
共振和π共轭是密切相关的术语,其中π共轭引起化合物的共振。共振和π共轭的关键区别在于,共振是指分子在离域电子存在下的稳定性,而π共轭是指π电子分布在分子的整个区域,而不是属于分子中的单个原子。
引用
1“有机化学中的共轭与共振”,《有机化学硕士》,2020年1月26日,可在此查阅。