主要区别
疏水分子和亲水分子的主要区别在于疏水分子是疏水分子,而亲水分子是亲水分子。
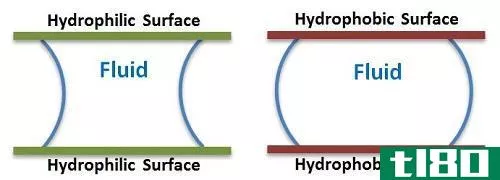
疏水分子(hydrophobic molecules) vs. 亲水分子(hydrophilic molecules)
疏水分子被认为是非极性分子,而亲水性分子则是极性分子。疏水分子被认为是不易在水中吸收的分子,而亲水分子则是容易在水中吸收的分子。疏水分子也叫疏水分子;另一方面,亲水分子也叫亲水分子。
疏水分子抵抗溶液中的水分子;相反,亲水分子吸引溶液中的水分子。当疏水分子加入水中时,吉布斯自由能为正值;反之,亲水分子加入水中时,吉布斯自由能为负值。疏水分子的熵随分子加入水中而降低;反之,亲水分子的熵随分子加入水中而增加。
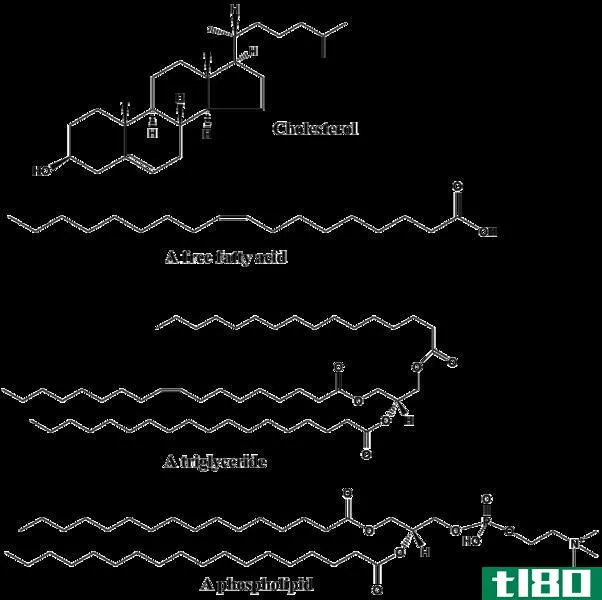
疏水分子在水中的溶解过程被认为是一个吸热反应;另一方面,亲水分子在水中的溶解过程被认为是放热反应。一些疏水分子的例子是脂质、脂肪和油,而亲水分子是盐、糖和水。在各种细胞活动中,疏水分子发生被动扩散,而亲水分子发生促进扩散。
比较图
什么是疏水分子(hydrophobic molecules)?
疏水分子这个术语被认为是不易在水中吸收的分子。因此,这些分子是防水的。疏水分子也被认为是疏水分子。疏水分子的疏水性解释了疏水分子的数量。由于疏水分子的非极性,他们认为是疏水的。
从另一个意义上讲,亲水性分子通常是由长链烃基组成的非极性非极性分子。疏水分子形成胶束,当疏水分子加入水中时,它看起来像一团团块,与水有轻微的相互作用。但是水分子在这些疏水分子的周围排列形成一个笼子。当胶束产生时,氢键就会断裂,而氢键存在于水分子中,从而为团簇的存在创造了一定的区域。
由于化学键如氢键在这个反应中被分解并释放能量,所以被认为是一个吸热反应,整个过程导致系统的熵降低。疏水分子之间的特殊协作形式通常是范德华界面,因为它们通常是非极性的。水里的疏水分子**在一起并混合,以减少与水的进一步联系。
由于水分子之间的氢键倾向于包围疏水分子团,导致焓值变化为正值,而系统的焓值进一步增加,这是由于水分子从团块周围释放疏水分子的笼体破裂而引起的。疏水分子的例子有脂类、脂肪和油。
什么是亲水分子(hydrophilic molecules)?
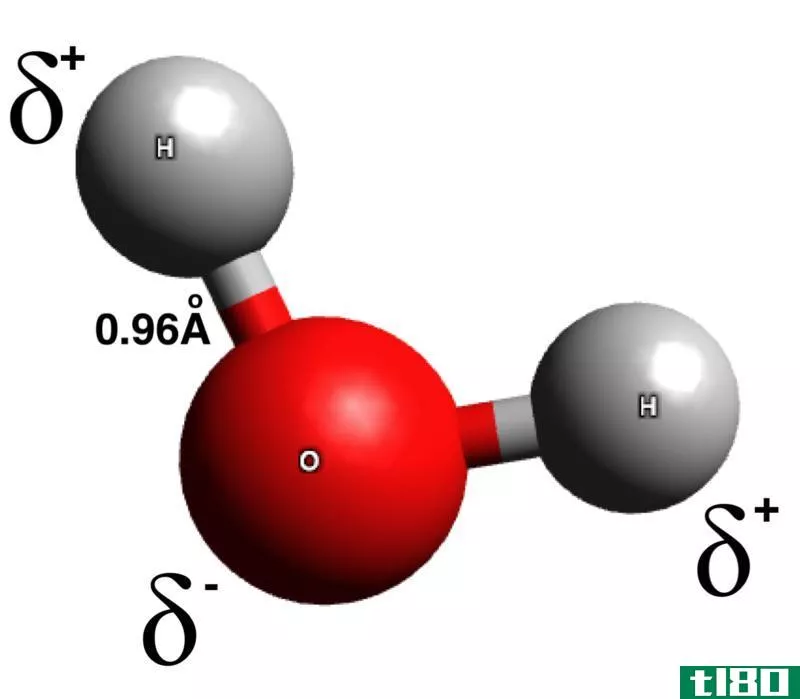
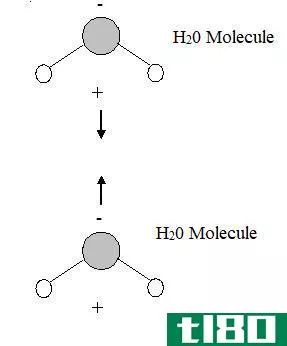
亲水分子这一术语描述了这些分子很容易溶于水,因为它们热爱水,并且它们能吸引水分子。亲水分子也被认为是亲水分子,因为它们通常是极性分子,可以被水吸收。与水形成各种化学键的亲水分子。
亲水分子,如果由O-H或N-H键构成,则它们将与水形成氢键,并完全溶解在水中。由于水中亲水分子的混合,系统的熵也会增大。
同时,水和亲水分子之间产生了新的键,所以这是一个放热反应,但是焓的变化会是负的。当亲水分子加入水中时,Gibbs自由能出现负值,表明该反应是自发的。化学键中原子的电负性值之间的差异是增加不同分子间极化的主要原因。亲水性的例子有盐、糖和水。
主要区别
- 疏水分子被认为是非极性分子,而亲水分子则被称为极性分子。
- 在水中不易吸收的分子通常被认为是疏水分子,而容易在水中吸收的分子则被认为是亲水分子。
- 疏水分子也被称为疏水分子;另一方面,亲水分子也被称为亲水分子。
- 疏水分子起到水排斥作用;相反,亲水分子起到了水的作用。
- 疏水分子的正值由吉布斯自由能发展,反之,亲水分子的负值由吉布斯自由能发展。
- 疏水分子的熵减小,而在疏水分子中熵则增加。
- 水溶性疏水分子的过程被认为是吸热反应,另一方面,溶解在水中的亲水分子过程被认为是放热反应。
- 脂肪、脂肪和油是疏水分子的一些例子,而盐、糖和水是亲水分子的例子。
- 疏水分子中,被动扩散过程发生,而亲水分子中则发生了促进扩散的过程。
结论
以上讨论的结论是疏水性分子是疏水性的,是非极性的,而亲水性分子是亲水性的,是极性分子。