弱酸和稀酸的关键区别在于,弱酸是一种化合物,当溶解在水中时会部分分解,而稀酸是一种含有比酸更多的水的溶液。
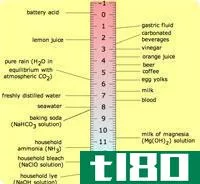
酸是一种能在水中离解释放质子(氢离子)的化合物。因此,酸的pH值低于7。根据酸的强度有强酸和弱酸两种类型。但根据酸的浓度,有浓酸和稀酸两种酸溶液。
目录
1. 概述和主要区别
2. 什么是弱酸
3. 什么是稀酸
4. 并列比较-弱酸与稀酸的表格形式
5. 摘要
什么是弱酸(a weak acid)?
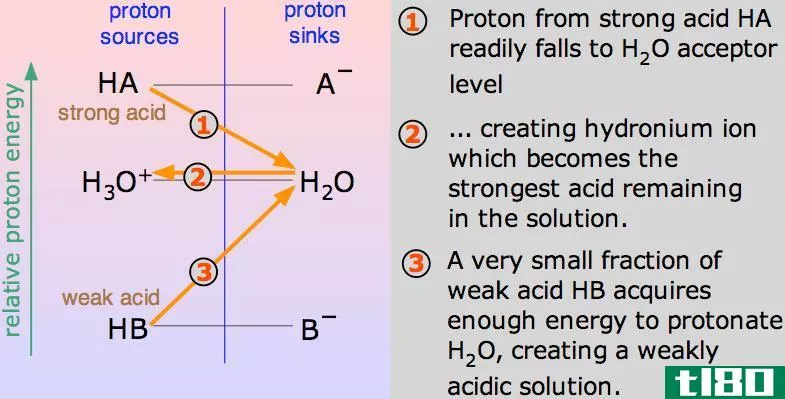
弱酸是一种化合物,当溶解在水中时会部分分解成离子。弱酸是弱碱的共轭酸。此外,与相同浓度的强酸相比,弱酸的pH值较高。在写弱酸解离的化学方程式时,我们用双箭头来包括正向和反向反应,因为弱酸的解离是可逆的。
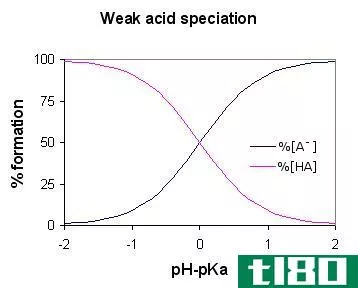
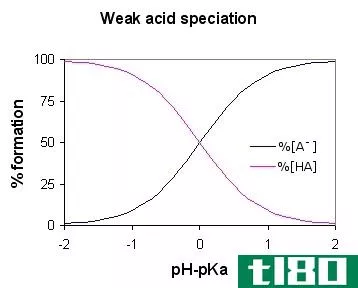
图01:弱酸的形态(AH是弱酸)
弱酸变弱是因为酸性化合物的极性较弱;如果化合物的极性更强,质子很容易离开酸分子,但在这里,由于化合物的极性较低,很难分解化学键。一些弱酸的例子包括乙酸、甲酸、氢氟酸、硫化氢等。
什么是稀酸(a dilute acid)?
稀酸是一种低浓度酸的水溶液。这意味着,稀酸溶液中的水比酸的含量多。稀酸可以是弱酸,也可以是强酸。术语“稀释”仅描述酸的浓度。稀酸的反义词是浓酸。

图02:浓盐酸
此外,我们可以通过加入更多的水来稀释酸。然而,在浓酸中加水是危险的。因此,安全的方法是在水中加酸。稀释酸是非常重要的,因为使用高浓度的酸如果接触到皮肤会导致严重烧伤。
弱酸(weak acid)和稀酸(dilute acid)的区别
弱酸根据酸的强度属于酸的分类,而稀酸属于酸的浓度范畴。弱酸和稀酸的关键区别在于,弱酸是一种化合物,当溶解在水中时会部分分解,而稀酸是一种含有比酸更多的水的溶液。然而,酸的稀释不影响酸的反应性。这意味着,强酸在稀释后不会变成弱酸。但是,弱酸天生就不那么活泼。
下面的信息图总结了弱酸和稀酸之间的区别。

总结 - 弱酸(weak acid) vs. 稀酸(dilute acid)
弱酸根据酸的强度属于酸的分类,稀酸属于酸浓度的范畴。弱酸和稀酸的关键区别在于,弱酸是一种化合物,当溶解在水中时会部分分解,而稀酸是一种含有比酸更多的水的溶液。
引用
1赫尔曼斯汀,安妮·玛丽。“弱酸的定义和化学中的例子”,ThoughtCo,May。2019年5月5日,Comm*** Wikimedia。