热力学定律
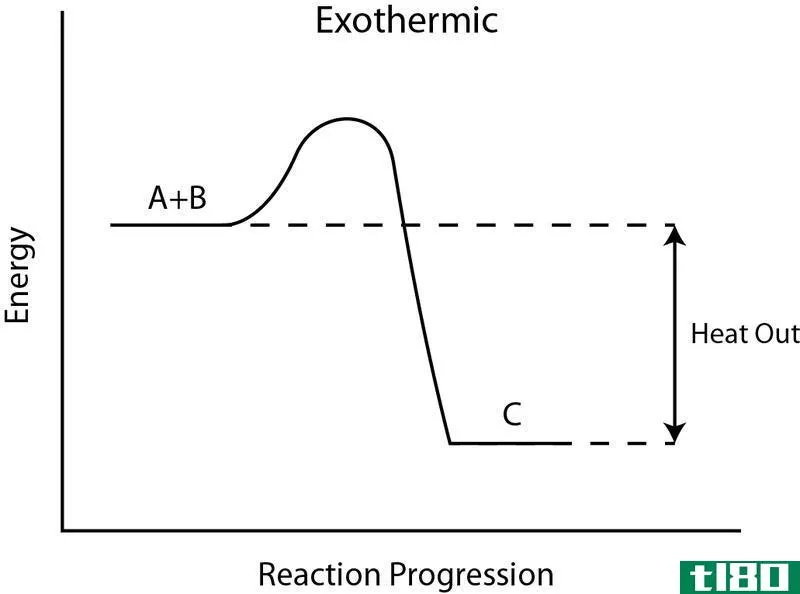
被称为热力学的科学分支研究的是能够将热能转换成至少一种其他形式的能量(机械能、电能等)或功的系统。热力学定律是多年来发展起来的,是热力学系统发生某种能量变化时所遵循的一些最基本的规则。

热力学史
热力学的历史始于奥托·冯·盖里克(Otto von Guericke),他于1650年制造了世界上第一台真空泵,并用他的马格德堡半球演示了真空。盖里克被迫制造了一个真空,以反驳亚里士多德长期坚持的“大自然厌恶真空”的假设。盖瑞克之后不久,英国物理学家和化学家罗伯特·博伊尔就知道了盖瑞克的设计,并于1656年与英国科学家罗伯特·胡克合作建造了一台气泵。使用这种泵,博伊尔和胡克发现了压力、温度和体积之间的相关性。随着时间的推移,波义耳定律逐渐形成,它表明压力和体积成反比。
热力学定律的后果
热力学定律往往很容易陈述和理解。。。如此之多以至于很容易低估它们的影响。除其他外,他们还限制了能量在宇宙中的使用。很难过分强调这一概念的重要性。热力学定律的结果在某种程度上涉及到科学研究的几乎每个方面。
理解热力学定律的关键概念
要理解热力学定律,必须理解与之相关的其他热力学概念。
- 热力学概述-概述热力学领域的基本原理
- 热能-热能的基本定义
- 温度-温度的基本定义
- 传热介绍-各种传热方法的说明。
- 热力学过程——当热力学系统经历某种能量转移时,热力学定律主要适用于热力学过程。
热力学定律的发展
热作为一种独特的能量形式的研究大约始于1798年,当时英国军事工程师本杰明·汤普森爵士(也被称为拉姆福德伯爵)注意到,热量的产生与所做的工作量成比例。。。这是一个基本概念,最终将成为热力学第一定律的结果。
法国物理学家萨迪·卡诺(Sadi Carnot)在1824年首次提出了热力学的基本原理。卡诺用来定义卡诺循环热机的原理最终将由德国物理学家鲁道夫·克劳修斯(Rudolf Clausius)转化为热力学第二定律,他也经常被认为是热力学第一定律的制定者。
19世纪热力学迅速发展的部分原因是工业革命期间需要开发高效的蒸汽机。
动力学理论;热力学定律
热力学定律本身并不特别关注热传递的具体方式和原因,这对于原子理论被完全采用之前制定的定律来说是有意义的。它们处理系统内能量和热转换的总和,不考虑原子或分子水平上热传递的具体性质。
热力学零定律
这个零定律是热平衡的一种传递性质。数学的传递性表明,如果A=B和B=C,那么A=C。处于热平衡的热力学系统也是如此。
零定律的一个结果是认为测量温度有任何意义。为了测量温度,温度计整体、温度计内的水银和被测物质之间必须达到热平衡。这反过来又导致能够准确地说出物质的温度。
在热力学研究的大部分历史中,人们对这条定律的理解并没有得到明确的阐述,直到20世纪初才意识到这条定律本身就是一条定律。英国物理学家拉尔夫·H·福勒(Ralph H.Fowler)首次创造了“零定律”一词,因为他相信零定律甚至比其他定律更为基本。
热力学第一定律
虽然这听起来很复杂,但实际上是一个非常简单的想法。如果你给一个系统添加热量,只有两件事可以做——改变系统的内能或使系统做功(当然,也可以两者结合)。所有的热能都必须用于做这些事情。
第一定律的数学表示
物理学家通常使用统一的约定来表示热力学第一定律中的量。他们是:
- U1(或Ui)=过程开始时的初始内能
- U2(或Uf)=过程结束时的最终内能
- delta-U=U2-U1=内能的变化(用于开始和结束内能的细节无关的情况)
- Q=进入(Q>0)或离开(Q<0)系统的热量
- W=系统(W>0)或系统(W<0)上执行的功。
这就产生了第一定律的数学表示法,它被证明非常有用,可以用两种有用的方式重写:
热力学过程的分析,至少在物理课堂情境中,通常涉及分析其中一个量为0或至少以合理方式可控的情境。例如,在绝热过程中,传热(Q)等于0,而在等容过程中,功(W)等于0。
第一定律;能量守恒
许多人认为热力学第一定律是能量守恒概念的基础。它基本上说,进入一个系统的能量不能在过程中损失,但必须用来做一些事情。。。在这种情况下,要么改变内能,要么做功。
从这个角度来看,热力学第一定律是迄今为止发现的影响最深远的科学概念之一。
热力学第二定律
热力学第二定律:热力学第二定律有很多形式,我们将很快讨论,但它基本上是一个定律,与物理学中的大多数其他定律不同,它不涉及如何做某事,而是完全涉及对可以做的事施加限制。
这是一条定律,它说大自然限制我们在不付出大量努力的情况下获得某些结果,因此它也与能量守恒的概念密切相关,就像热力学第一定律一样。
在实际应用中,这一定律意味着任何基于热力学原理的热机或类似装置,即使在理论上,也不能100%有效。
法国物理学家兼工程师萨迪·卡诺(Sadi Carnot)在1824年开发卡诺循环发动机时首次阐明了这一原理,后来德国物理学家鲁道夫·克劳修斯(Rudolf Clausius)将其正式化为热力学定律。
熵与热力学第二定律
热力学第二定律可能是物理学领域之外最流行的,因为它与熵的概念或热力学过程中产生的无序密切相关。第二定律重新表述为关于熵的陈述,内容如下:
换句话说,在任何封闭系统中,每次系统经过热力学过程时,系统都不可能完全恢复到与以前完全相同的状态。这是时间之箭的一个定义,因为根据热力学第二定律,宇宙的熵总是会随着时间的推移而增加。
第二定律的其他表述
A cyclic transformation whose only final result is to transform heat extracted from a source which is at the same temperature throughout into work is impossible. - Scottish physicist William Thompson ( A cyclic transformation whose only final result is to transfer heat from a body at a given temperature to a body at a higher temperature is impossible. - German physicist Rudolf Clausius热力学第二定律的所有上述公式都是相同基本原理的等价陈述。
热力学第三定律
热力学第三定律本质上是关于创造绝对温度标度的能力的陈述,对于绝对温度标度,绝对零是固体内能精确为0的点。
各种来源显示了热力学第三定律的以下三种潜在公式:
- 在有限的一系列操作中,不可能将任何系统降至绝对零。
- 当温度接近绝对零度时,元素最稳定形式的完美晶体的熵趋于零。
- 当温度接近绝对零度时,系统的熵接近常数
第三定律是什么意思
第三定律意味着一些事情,所有这些公式都会产生相同的结果,这取决于你考虑的程度:
公式3包含最少的限制,仅仅说明熵是一个常数。事实上,这个常数是零熵(如公式2中所述)。然而,由于对任何物理系统的量子限制,它将崩溃到其最低量子态,但永远无法将熵完全减少到0,因此不可能在有限的步骤内将物理系统减少到绝对零(这产生了公式1)。
- 发表于 2021-09-23 18:27
- 阅读 ( 274 )
- 分类:物理
你可能感兴趣的文章
热化学(thermochemistry)和热力学(thermodynamics)的区别
热化学(thermochemistry)和热力学(thermodynamics)的区别 热力学是物理科学的一个分支,研究热与其他形式的能量(如机械能、电能或化学能)之间的关系。热化学是热力学的一个分支。热化学也是化学的一个分支,它描述与化学反...
- 发布于 2020-10-24 03:12
- 阅读 ( 545 )
物质守恒定律(law of conservation of matter)和能量(energy)的区别
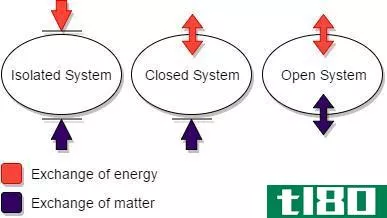
...恒定律和能量守恒定律是化学中用来解释孤立的,封闭的热力学系统的性质的两个定律。这些定律指出,物质或能量不能被创造或毁灭,但可以被转换成不同的形式或重新排列。物质守恒定律和能量守恒定律的关键区别在于,物...
- 发布于 2020-10-24 22:53
- 阅读 ( 696 )
动力学(kinetics)和运动学(kinematics)的区别
...何运动,投掷的球如何飞等等。 整个区域所依据的基本定律是著名的牛顿第二运动定律,即力等于质量乘以加速度。但是,运动学不会计算任何导致这些加速度出现的力。 相反,它只关注物体的速度、加速度和位置。由于它只...
- 发布于 2021-06-25 06:47
- 阅读 ( 355 )
热力学(thermodynamics)和动力学(kinetics)的区别
与气体的分子动力学理论相似,热力学涉及气体的分析。然而,当气体分子动力学理论用微观的方法研究气体过程时,热力学则用宏观的方法。这意味着热力学不考虑分子水平上的过程,而是把气体看作一个整体,气体过程是现...
- 发布于 2021-06-25 17:02
- 阅读 ( 722 )
第一(first)和热力学第二定律(second law of thermodynamics)的区别
第一个主要区别(main difference first) vs. 热力学第二定律(second law of thermodynamics) 热力学是物理学、材料科学、工程、化学、环境科学等多个领域的重要组成部分。热力学有四个定律;热力学第零定律、热力学第一定律、热力学第二...
- 发布于 2021-06-27 20:26
- 阅读 ( 506 )
一阶(first order)和零级动力学(zero order kinetics)的区别
...述化学反应的速率。化学动力学的概念首先是由质量作用定律发展起来的。质量作用定律描述了化学反应的速度与反应物的质量成正比。根据化学动力学,反应可分为零级反应、一级反应和二级反应。一级动力学和零级动力学的...
- 发布于 2021-06-29 08:18
- 阅读 ( 914 )
亨利定律(henry’s law)和拉乌尔定律(raoult’s law)的区别
...vs. 拉乌尔定律(raoult’s law) 亨利定律和拉乌尔特定律都是热力学中发现的两个定律,描述了一个解与其蒸汽之间的关系,它们之间是相互平衡的。亨利定律可以用来解释气体在液体溶剂(如水)中的溶解。拉乌尔特定律表明溶剂...
- 发布于 2021-06-29 11:05
- 阅读 ( 908 )
化学的主要规律
...既不能创造也不能破坏能源;宇宙的能量是恒定的。这是热力学第一定律。 质量物质的守恒既不能被创造也不能被破坏,尽管它可以被重新安排。质量在普通的化学变化中保持不变。这一原理也被称为物质守恒。 道尔顿定律...
- 发布于 2021-09-15 12:45
- 阅读 ( 183 )
赫斯的法律定义
...)并不取决于初始状态和最终状态之间的路径。该定律是热力学第一定律和能量守恒定律的一种变体。 赫斯定律的重要性 因为赫斯定律成立,所以可以将化学反应分解为多个步骤,并使用标准生成焓来计算化学反应的总能...
- 发布于 2021-09-22 03:43
- 阅读 ( 254 )
热力学第一定律的定义
热力学第一定律是物理定律,它规定一个系统及其周围环境的总能量保持不变。该定律也被称为能量守恒定律,它规定能量可以从一种形式转换为另一种形式,但在一个孤立的系统中既不能产生也不能消灭。根据热力学第一定...
- 发布于 2021-09-22 21:43
- 阅读 ( 182 )