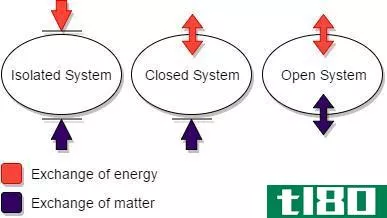
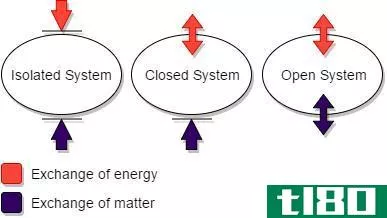
热力学第一定律的定义
热力学第一定律是物理定律,它规定一个系统及其周围环境的总能量保持不变。该定律也被称为能量守恒定律,它规定能量可以从一种形式转换为另一种形式,但在一个孤立的系统中既不能产生也不能消灭。根据热力学第一定律,第一类永动机是不可能的。换言之,不可能构造一台能够从无到有连续循环并产生功的发动机。

热力学第一定律方程
第一定律的方程式可能会令人困惑,因为有两种不同的符号约定在使用。
在物理学中,特别是在讨论热机时,系统能量的变化等于系统中来自周围环境的热流减去系统对周围环境所做的功。该定律的方程式可以写成:
ΔU=Q-W
这里,ΔU是封闭系统内能的变化,Q是供给系统的热量,W是系统对周围环境所做的功。这一版本的法律遵循克劳修斯的签字惯例。
然而,IUPAC使用Max Planck提出的符号约定。这里,系统的净能量转移为正,系统的净能量转移为负。然后方程变成:
ΔU=Q+W
来源
- 阿德金斯,C.J.(1983年)。平衡热力学(第三版)。剑桥大学出版社。ISBN 0-521-25445-0。
- Bailyn,M.(1994年)。热力学概论。美国物理学会出版社。纽约。ISBN 0-88318-797-3。
- Denbigh,K.(1981年)。化学平衡原理及其在化学和化学工程中的应用(第四版)。剑桥大学出版社。剑桥英国。ISBN 0-521-23682-7。
- 发表于 2021-09-22 21:43
- 阅读 ( 184 )
- 分类:数学
你可能感兴趣的文章
物质守恒定律(law of conservation of matter)和能量(energy)的区别
...恒定律和能量守恒定律是化学中用来解释孤立的,封闭的热力学系统的性质的两个定律。这些定律指出,物质或能量不能被创造或毁灭,但可以被转换成不同的形式或重新排列。物质守恒定律和能量守恒定律的关键区别在于,物...
- 发布于 2020-10-24 22:53
- 阅读 ( 706 )
孤立系统(isolated system)和封闭系统(closed system)的区别
...,这些系统通过平衡压力、温度或其他参数,随时间达到热力学平衡。 实际上,孤立的系统并不存在,因为所有的事物都以某种方式相互作用。然而,我们不能把宇宙看作是一个孤立的系统,把它看作是一个孤立的系统。理论...
- 发布于 2020-10-28 02:59
- 阅读 ( 1535 )
热力学(thermodynamics)和动力学(kinetics)的区别
与气体的分子动力学理论相似,热力学涉及气体的分析。然而,当气体分子动力学理论用微观的方法研究气体过程时,热力学则用宏观的方法。这意味着热力学不考虑分子水平上的过程,而是把气体看作一个整体,气体过程是现...
- 发布于 2021-06-25 17:02
- 阅读 ( 730 )
第一(first)和热力学第二定律(second law of thermodynamics)的区别
第一个主要区别(main difference first) vs. 热力学第二定律(second law of thermodynamics) 热力学是物理学、材料科学、工程、化学、环境科学等多个领域的重要组成部分。热力学有四个定律;热力学第零定律、热力学第一定律、热力学第二...
- 发布于 2021-06-27 20:26
- 阅读 ( 512 )
等熵(isentropic)和绝热的(adiabatic)的区别
...(main difference isentropic) vs. 绝热的(adiabatic) 等熵和绝热是热力学系统中发生的两个特殊化学过程的两个术语。这些过程是用热力学来解释的。热力学是物理科学的一个分支,研究热和其他形式能量之间的关系。等熵过程是一个理...
- 发布于 2021-06-29 21:23
- 阅读 ( 720 )
化学的主要规律
...既不能创造也不能破坏能源;宇宙的能量是恒定的。这是热力学第一定律。 质量物质的守恒既不能被创造也不能被破坏,尽管它可以被重新安排。质量在普通的化学变化中保持不变。这一原理也被称为物质守恒。 道尔顿定律...
- 发布于 2021-09-15 12:45
- 阅读 ( 186 )
拉乌尔定律在化学中的定义
...,Comptes rendus,104:1430-1433。 洛克,彼得A.(1969)。化学热力学。麦克米伦。p、 261 ISBN 1891389327。
- 发布于 2021-09-15 16:21
- 阅读 ( 187 )
赫斯的法律定义
...)并不取决于初始状态和最终状态之间的路径。该定律是热力学第一定律和能量守恒定律的一种变体。 赫斯定律的重要性 因为赫斯定律成立,所以可以将化学反应分解为多个步骤,并使用标准生成焓来计算化学反应的总能...
- 发布于 2021-09-22 03:43
- 阅读 ( 260 )
什么是热力学过程?(a thermodynamic process?)
当系统内存在某种能量变化时,系统会经历热力学过程,通常与压力、体积、内能、温度或任何类型的热传递的变化有关。 热力学过程的主要类型 有几种特定类型的热力学过程经常发生(在实际情况下),它们通常在热力...
- 发布于 2021-09-22 23:00
- 阅读 ( 289 )
等容过程
等容过程是体积保持恒定的热力学过程。由于体积恒定,系统不工作,W=0。(“W”是功的缩写。)这可能是最容易控制的热力学变量,因为它可以通过将系统置于既不膨胀也不收缩的密封容器中获得。 热力学第一定律 要理...
- 发布于 2021-09-23 15:01
- 阅读 ( 397 )