原子序数与原子量
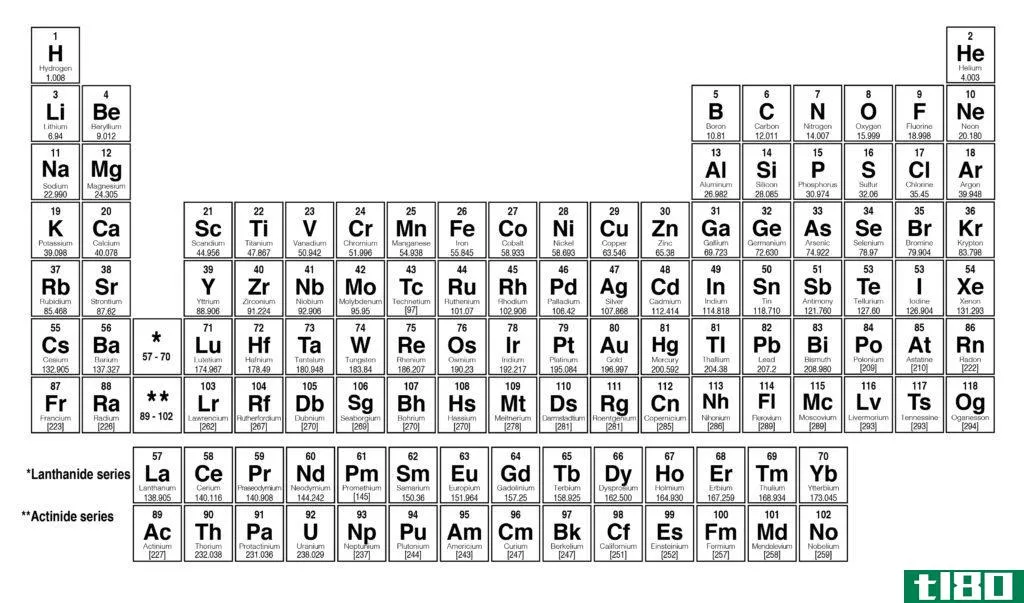
原子的特征是原子数。在周期表中,原子是根据原子数排列的。原子数提供了有关原子及其性质的各种信息。原子量对于了解元素也很重要。
原子序数是多少?
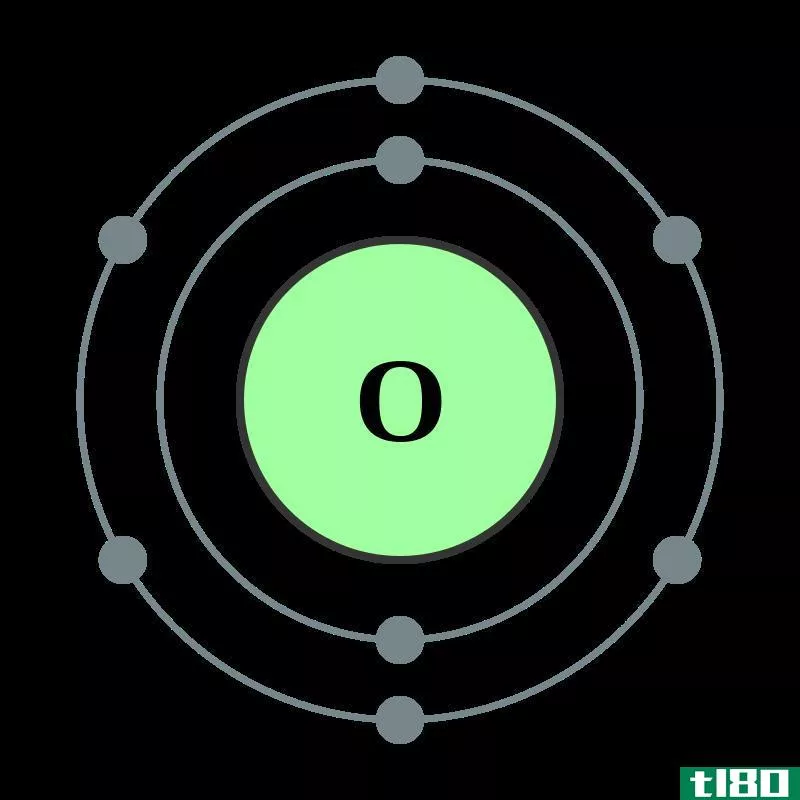
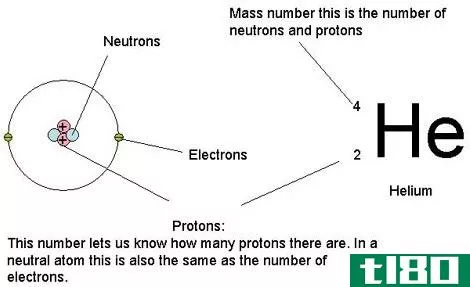
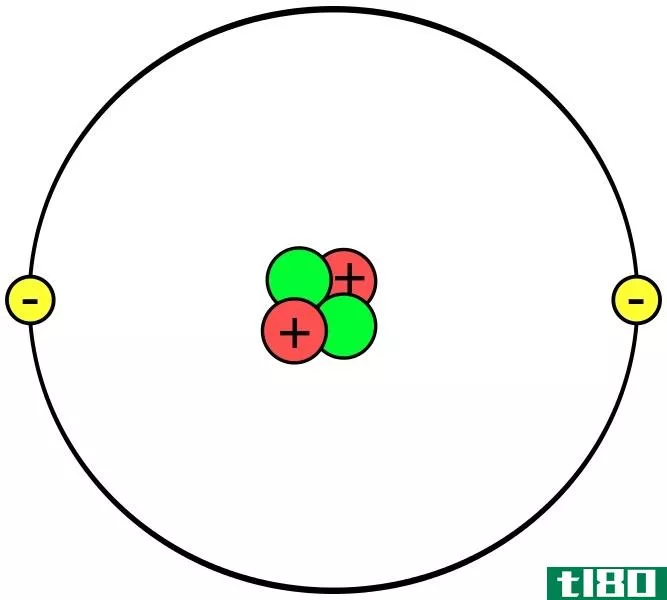
原子主要由质子、中子和电子组成。原子核含有质子和中子。此外,还有电子绕着原子核绕轨道旋转。元素的原子序数是它在原子核中的质子数。表示原子序数的符号是Z。当原子为中性时,它的电子数与质子相同。因此,在这种情况下,原子序数等于电子数。然而,用质子数作为原子序数总是可靠的。周期表中的元素是根据原子序数的增加排列的。这种排列方式在大多数情况下会自动地以增加的原子量排列它们。每个元素都有独立的原子序数,没有一个元素具有相同的原子序数。因此,原子序数是区分不同元素的好方法。通过观察原子序数本身,许多关于元素的信息都可以被提取出来。例如,它告诉元素在周期表中所属的组和周期。此外,它还提供了氧化态、离子电荷、键合行为、原子核电荷等信息。
原子量是多少?
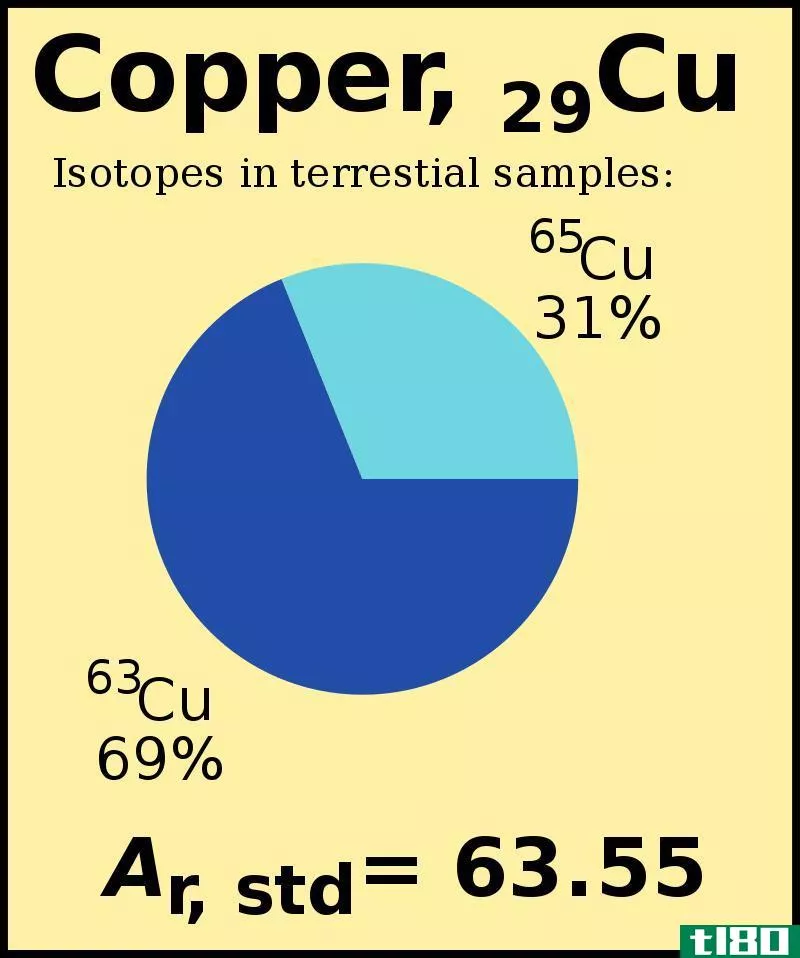
元素周期表中的大多数原子都有两种或两种以上的同位素。同位素的不同之处在于它们有不同数量的中子,即使它们有相同的质子和电子量。由于它们的中子量不同,每种同位素的原子质量也不同。原子量是考虑所有同位素质量而计算的平均重量。每种同位素以不同的百分比存在于环境中。在计算原子量时,同时考虑了同位素质量及其相对丰度。此外,原子的质量非常小,所以我们不能用克或公斤这样的正常质量单位来表示它们。为了我们的目的,我们使用另一种叫做原子质量单位(amu)的单位来测量原子量。
IUPAC对原子量的定义如下:
“从指定来源中元素的原子重量(相对原子质量)是元素的平均质量与12 C原子质量的1/12之比。”
周期表中给出的权重是这样计算的,它们是作为相对原子质量给出的。
| 原子数和原子量有什么区别?•元素的原子数是它在核中的质子数量。原子重量是考虑到所有同位素质量计算的平均重量。质子和中子的数量在很大程度上是原子重量的贡献。(这是因为电子的质量比质子或中子小)。•周期表中的元素是根据原子数的增加而不是原子重量排列的,但通常,当连续元素按照原子数排列时,也可以看到原子量的增加。 |