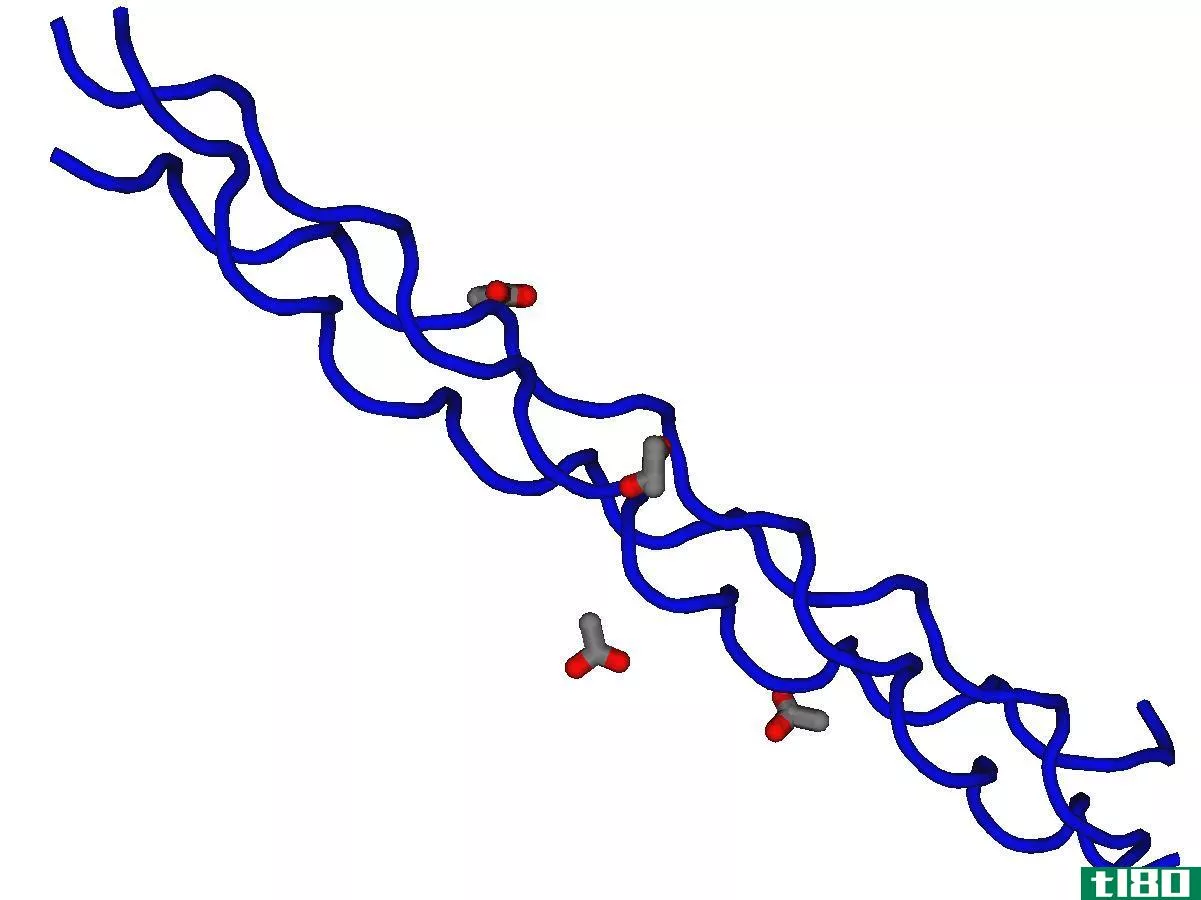
原取向和互变异构的关键区别在于,原取向讨论的是两种形式的分子,它们之间只有在特定质子的位置上不同,而互变异构则讨论了两个结构异构体通过原子或键的重新定位来相互转换。
原向性是互变异构的一种形式;它是互变异构最常见的形式。互变异构是有机化学中的一个概念,它描述了通过原子或键的重新定位将一个结构异构体转化为另一个异构体。如果重定位发生在分子中的一个质子,那么我们称之为质子性。因此,这种互变异构被称为原变异构。
目录
1. 概述和主要区别
2. 什么是原向性
3. 什么是互变异构
4. 并列比较-表格式的原向性与互变异构
5. 摘要
什么是原向性(prototropy)?
原向性是一种互变异构现象,其中质子发生重定位。它是互变异构最常见的形式。因此,它也被称为原热带互变异构。我们可以把它看作是酸碱行为的一个子集。原变异构体是在具有相同经验公式和总电荷的分子之间进行异构质子化的异构体。酸和碱可以催化这些反应。
原变异构有两种类型:环状互变异构和环链互变异构。在环状互变异构中,质子往往占据杂环系统的两个或多个位置。在环链互变异构中,质子的运动伴随着从开放结构到环状结构的变化。
什么是互变异构(tautomeri**)?
互变异构是有机化学中的一个概念,它描述了几种化合物通过重新定位一个原子或一个化学键而相互转化的效果。这种类型的相互转化在氨基酸和核酸中最常见。相互转化的过程被称为互变异构,这是一种化学反应。在这种相互转化过程中,质子或化学键的重新定位意味着另两种形式的原子之间氢原子的交换或单键或双键的迅速形成或破裂。
如果互变化发生在质子的迁移过程中,那么它就被称为原取向。如果互变化是随着单个或双键的迁移而发生的,那么它就被称为价互变异构。氢原子与接收氢原子的新原子形成共价键。互变异构体相互平衡存在。它们总是存在于两种化合物的混合物中,因为它们试图制备独立的互变异构体。
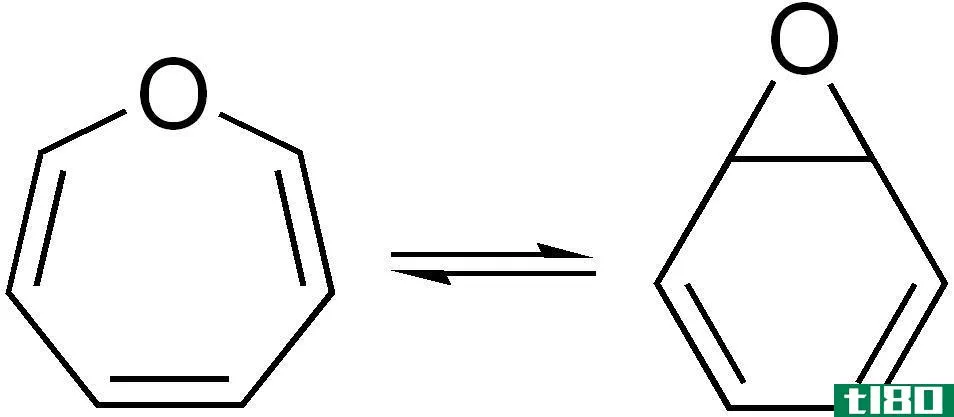
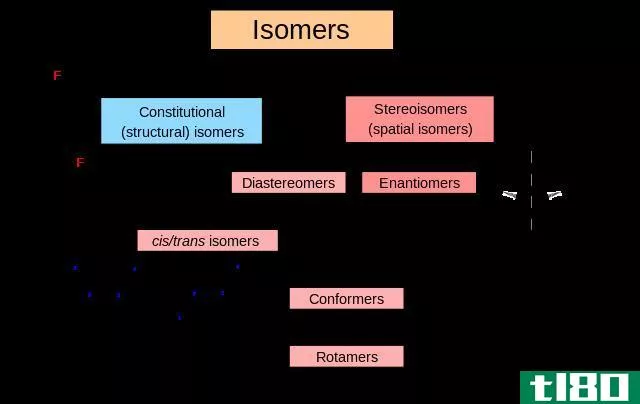
图01:价互变异构
在互变异构过程中,分子的碳骨架不发生变化。只有质子和电子的位置改变了。这个过程是一种将一种互变异构体转化为另一种形式的分子内化学过程。一个常见的例子是酮-烯醇互变异构。它是一种酸或碱催化的反应。一般来说,有机化合物的酮式比酮式更稳定,但在某些状态下,烯醇式比酮式更稳定。
原向性(prototropy)和互变异构(tautomeri**)的区别
原向性和互变异构是密切相关的术语;原向性是互变异构的一种类型。原向性与互变异构的关键区别在于,原向性讨论的是一个分子的两种形式,它们只在某一特定质子的位置上彼此不同,而互变异构体则是通过原子或键的重新定位来实现两种结构异构体的相互转化。
以下是表格形式的原向性和互变异构之间的区别的总结。
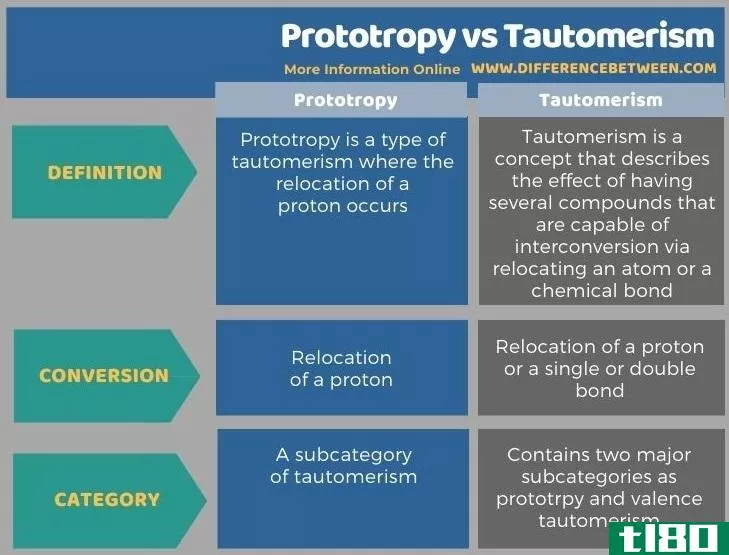
总结 - 原向性(prototropy) vs. 互变异构(tautomeri**)
原取向和互变异构是一种密切相关的术语,原语是互变异构的一种类型。原取向和互变异构的关键区别在于,原取向讨论的是两种形式的分子,它们之间只有在特定质子的位置上不同,而互变异构则讨论了两个结构异构体通过原子或键的重新定位来相互转换。
引用
1原生动物的定义。“定义,此处提供。