氧化电位和还原电位的主要区别在于氧化电位指示一种化学元素被氧化的倾向。相反,还原电位表示化学元素被还原的趋势。
氧化电位和还原电位是化学物质在标准条件下以伏特表示的两种电极电位值。因此,我们将它们命名为标准氧化电位和标准还原电位。这些电位的值决定了一种特定的化学物质进行氧化/还原的能力。
目录
1. 概述和主要区别
2. 氧化电位是多少
3. 什么是还原潜力
4. 并列比较-氧化电位与还原电位的表格形式
5. 摘要
什么是氧化电位(oxidation potential)?
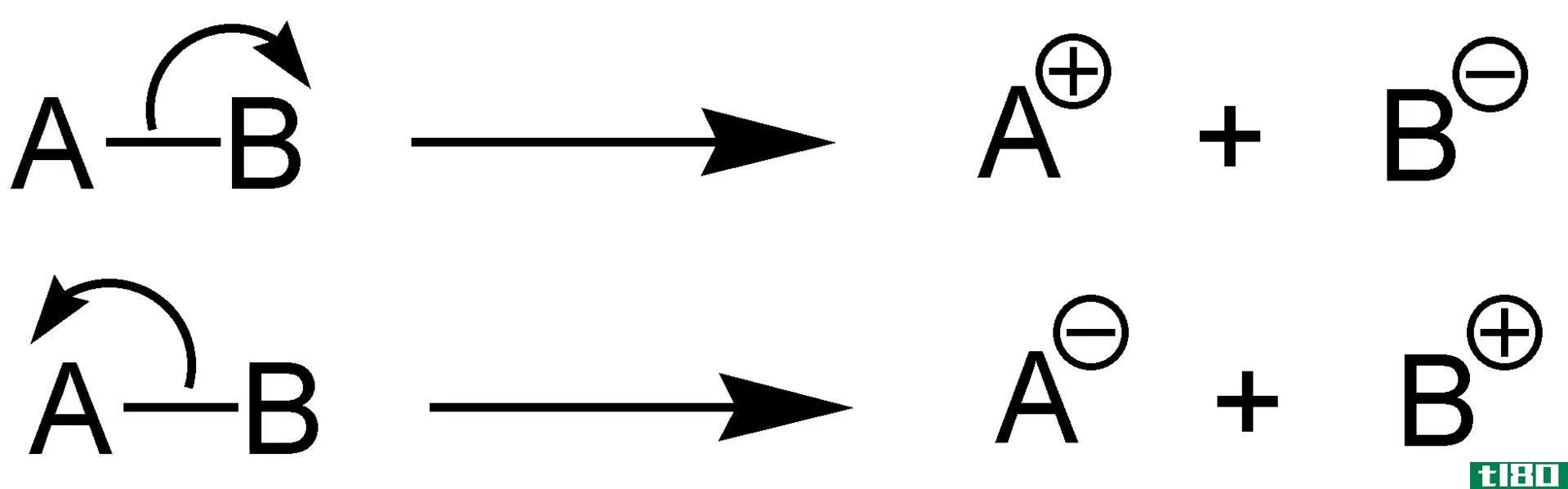
氧化电位是一个指示化学物质被氧化的趋势的值。换句话说,就是电极失去电子(氧化)的能力。通常,这个值是在标准条件下给出的;因此,我们将其命名为标准氧化电位。这个词的意思是SOP。它是用伏特来测量的。而且,这与标准还原电位非常相似,但它们的符号不同,即标准氧化电位的值是标准还原电位的负值。我们可以把氧化势写成半反应。铜的氧化反应和氧化电位的一般公式如下:

铜氧化半反应:Cu(s)⟶Cu2++2e–
上述反应(铜氧化)的标准氧化电位值为-0.34 V。
什么是还原电位(reduction potential)?
还原电位是特定化学物质发生还原的趋势。这意味着,这种特殊的化学物质愿意接受来自外界的电子(以得到还原)。它以伏特为单位,通常在标准条件下测量。因此,我们可以称之为还原标准。这个词的意思是SRP。我们可以把它写成还原半反应的形式。通式和铜为例如下:

铜还原的半反应:Cu2++2e–⟶Cu(s)
上述反应(铜的还原)的标准还原电位值为0.34v,这是精确值,但与同一化学物质铜的氧化电位值相反。因此,我们可以建立标准氧化电位和还原电位之间的关系,如下所示:
E00(SRP)=-E00(标准操作规程)
氧化电位(oxidation potential)和还原电位(reduction potential)的区别
氧化电位和还原电位是化学物质在标准条件下以伏特表示的两种电极电位值。氧化电位和还原电位的关键区别在于氧化电位表示化学元素被氧化的倾向,而还原电位则表示化学元素被还原的趋势。由于这些电位值是在标准条件下测得的,我们应将其命名为标准氧化电位和标准还原电位。
此外,我们将它们表示为SOP和SRP。此外,这两个项之间存在关系;标准氧化电位是完全相同的值,但符号与标准还原电位的符号不同。
下面的信息图总结了氧化电位和还原电位之间的区别。

总结 - 氧化电位(oxidation potential) vs. 还原电位(reduction potential)
氧化电位和还原电位是化学物质在标准条件下以伏特表示的两种电极电位值。氧化电位和还原电位的关键区别在于氧化电位表示化学元素被氧化的倾向,而还原电位则表示化学元素被还原的趋势。