氧化和还原的关键区别在于氧化是指电子的损失,而还原是指电子的获得。
不同化合物之间的化学反应称为氧化还原反应,如果反应物的氧化状态不同于产物的氧化状态。氧化还原是还原氧化的简称,是任何化学反应中发生的。氧化是指电子的损失,还原是指电子重新获得的地方。这些反应可以是简单的,也可以是复杂的,这取决于过程和所涉及的原子。
目录
1. 概述和主要区别
2. 什么是氧化
3. 什么是还原
4. 并列比较-表格形式的氧化与还原
5. 摘要
什么是氧化(oxidation)?
氧化可以描述为氧化数的增加。因此,氧化可以定义为原子、分子或离子失去电子。这种电子损失导致化学物质的氧化状态增加。因为氧化反应释放电子,所以应该有一个接受电子的物种。因此,氧化反应是一个主要反应的半反应。一种化学物质的氧化反应是其氧化状态的变化。氧化态是一个带有正(+)或负(-)符号的数字,表示特定原子、分子或离子失去或获得电子。

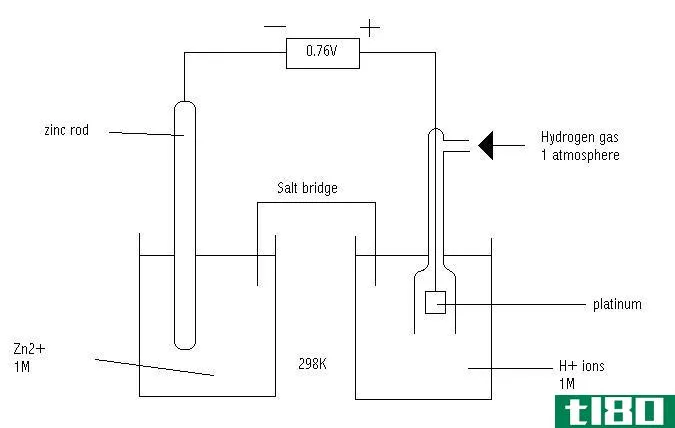
图01:两个半反应的例子:氧化和还原
在过去,氧化剂的定义是“氧化剂”。然而,这个定义不再准确,因为在缺氧的情况下会发生更多的氧化反应。例如,镁(Mg)与盐酸(HCl)之间的反应不含氧,但它是一种氧化还原反应,包括将Mg氧化成Mg2+。
什么是减少(reduction)?
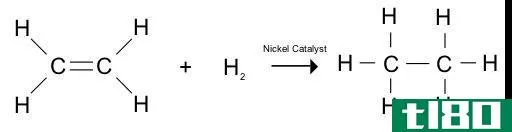
还原可以描述为氧化数的减少。因此,我们可以将还原定义为从原子、分子或离子获得的电子。这种电子的增加导致化学物质的氧化状态降低。因为还原反应得到电子,所以应该有一个给电子的物种。因此,还原反应是一个主要反应的半反应。一种化学物质的还原是随着其氧化状态的变化而变化的。
过去,还原一词的定义是“从化合物中除去氧气”,这是因为当时氧是唯一已知的氧化剂。然而,这个定义不再准确,因为在缺氧的情况下会发生更多的氧化反应。
氧化(oxidation)和减少(reduction)的区别
Reduction and oxidation are chemical processes involved in every chemical reaction. These are two opposite reacti***. The key difference between oxidation and reduction is that oxidation refers to the loss of electr*** while reduction refers to the gain of electr***. While oxidation increases the value of positive (+) sign, reduction increases the value of negative (-) sign.
总结 - 氧化(oxidation) vs. 减少(reduction)
还原和氧化是每一种化学反应都涉及的化学过程。氧化与还原的关键区别在于氧化指的是电子的损耗,而还原指的是电子的增益。
引用
1赫尔曼斯汀,安妮·玛丽。“化学中氧化的定义和例子”,ThoughtCo,2020年2月12日,可在此处查阅。赫尔曼斯汀,安妮·玛丽。“化学还原定义”,ThoughtCo,2020年2月11日,可在此处查阅。
2赫尔曼斯汀,安妮·玛丽。“化学还原定义”,ThoughtCo,2020年2月11日,