经典和非经典碳正离子的主要区别在于,经典碳正离子有一个碳原子,在三个化学键中有六个电子,而非经典碳正离子具有三中心双电子结构。
碳正离子是一种化学物质,是有机分子的一部分。它在碳原子上带正电荷。碳正离子的一个简单例子是CH3+。有些碳正离子在同一个碳原子或不同的碳原子上有一个以上的正电荷。此外,碳正离子是有机反应中由于正电荷的存在而起反应的中间产物;碳原子中有六个电子,这使得它不稳定(八个电子的存在保证了稳定性);因此它倾向于寻找电子。
目录
1. 概述和主要区别
2. 什么是经典碳阳离子
3. 什么是非经典碳阳离子
4. 并列比较-经典与非经典碳阳离子的表格形式
5. 摘要
什么是经典碳阳离子(classical carbocation)?
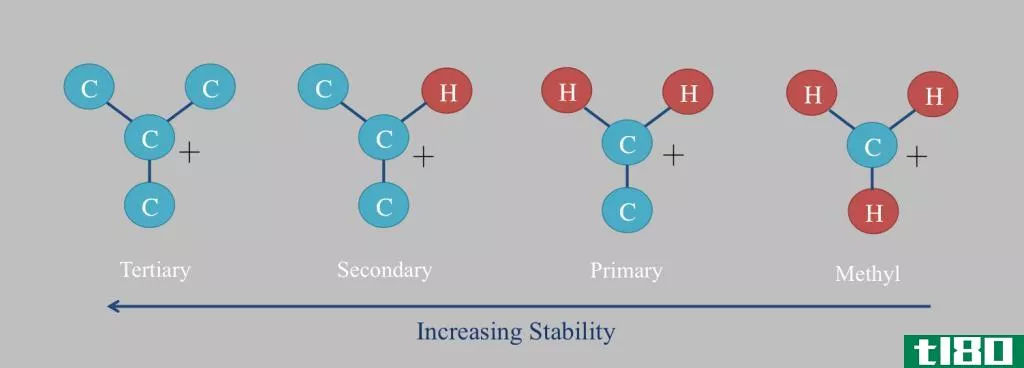
经典的碳正离子是一个带正电荷的碳原子的离子,它有六个电子参与三个化学键。我们可以把这个碳原子命名为三坐标正碳。

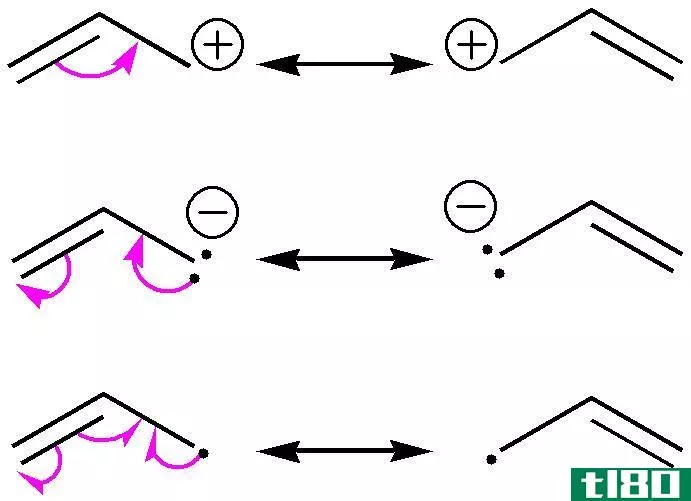
图01:经典碳阳离子的形成
为了保证最大的稳定性,碳原子应该有八个价电子。但是在碳阳离子中,碳原子中只有六个带正电荷的电子。因此,它倾向于从一个电负性物种多分享两个电子。这使碳原子稳定并中和正电荷。这就是经典碳阳离子反应性高的原因。然而,与相应的非经典碳阳离子相比,经典碳阳离子的能量较低。但是他们的能量差别很小。
什么是非经典碳阳离子(nonclassical carbocation)?
非经典碳正离子是一种在三中心双电子中心含有带正电荷的碳的离子。这意味着,在这些碳阳离子中有三个原子共享两个电子。这种电子共享称为电子离域。
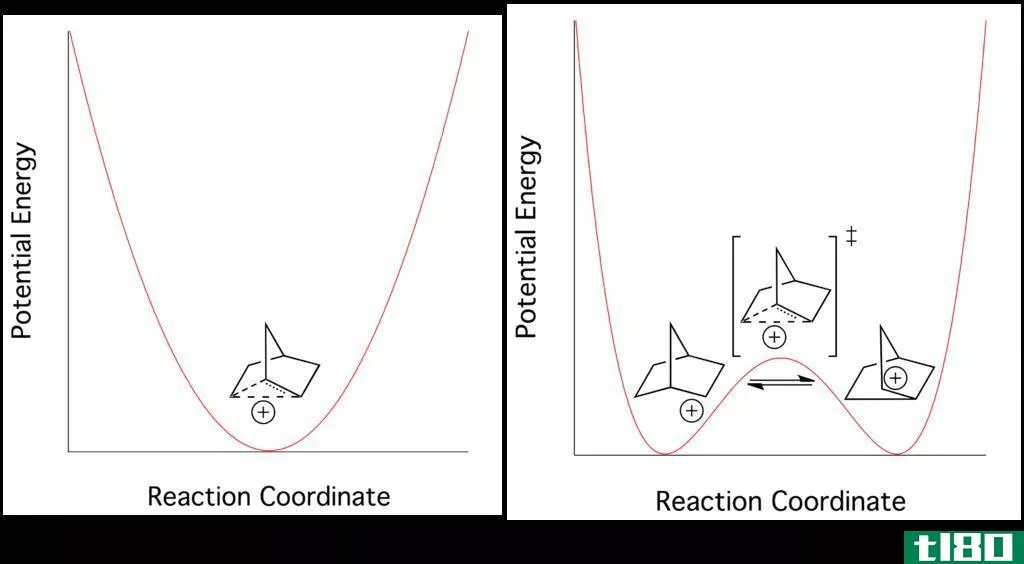
图02:经典和非经典碳阳离子之间的能量差
非经典碳阳离子最常见的例子是2-降冰片基阳离子。它存在于一个不太对称的三中心双电子结构中。经典和非经典碳阳离子之间的能量差别很小。因此,在实验上很难区分它们。
古典的(classical)和非经典碳阳离子(nonclassical carbocation)的区别
根据碳阳离子的化学结构,我们可以将碳阳离子分为经典和非经典两类。经典和非经典碳正离子的主要区别在于,经典碳阳离子有一个碳原子,在三个化学键中有六个电子,而非经典碳阳离子具有三个中心两个电子结构。非经典碳正离子的能量比经典碳阳离子的能量高,但这些能量之间的差别很小,因此很难区分经典结构和非经典结构之间的区别。
此外,经典碳阳离子转化为非经典碳阳离子或反之亦然的活化能非常小。除此之外,经典碳正离子在碳原子上带正电荷,碳原子周围有nod电子对,但在非经典碳阳离子中,电子在碳原子周围离域。经典碳正离子的一个实例是甲基离子,而非经典碳阳离子的示例是2-降冰片基离子。

总结 - 古典的(classical) vs. 非经典碳阳离子(nonclassical carbocation)
根据碳阳离子的化学结构,我们可以将碳阳离子分为经典碳阳离子和非碳碳阳离子两大类。经典和非经典碳正离子的主要区别在于,经典碳阳离子有一个碳原子,在三个化学键中有六个电子,而非经典碳阳离子具有三个中心两个电子结构。经典碳正离子的一个实例是甲基离子,而非经典碳阳离子的示例是2-降冰片基离子。
引用
1《碳离子》,化学libretext,2019年6月5日,可在此处查阅。“碳离子”维基百科.Org2019年,此处提供。
2“碳离子”维基百科.Org2019年,