平衡方程和骨架方程的关键区别在于平衡方程给出了参与化学反应的每种反应物和产物的实际分子数,而骨架方程只给出了反应物的数量。
化学方程式是化学反应的表示。也就是说,化学方程式给出了反应的反应物,最终产物和反应的方向。方程分为平衡方程和骨架方程两类。
目录
1. 概述和主要区别
2. 什么是平衡方程式
3. 什么是骨架方程
4. 并列比较-平衡方程与表格形式的骨架方程
5. 摘要
什么是平衡方程式(a balanced equation)?
一个平衡的化学方程式给出了每种反应物相互反应的实际数量和形成的产物分子的数量。这是一个详细的方程,给出了反应物和产物之间的比率。当计算一个参数,比如我们从反应中得到的产物的量,我们必须使用平衡的化学方程式;否则,我们就不知道反应物反应了多少,得到了多少产物。
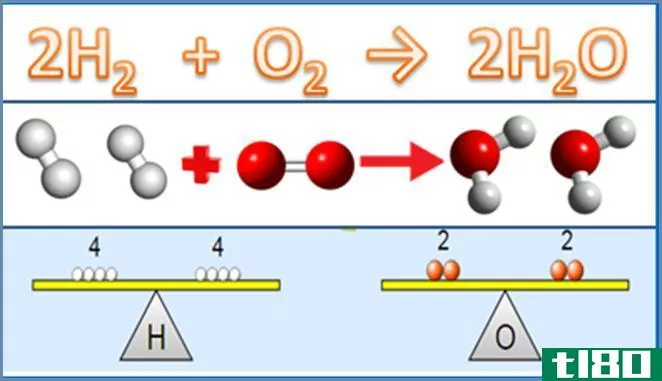
然而,在热力学计算中,这个方程在确定反应级数时是行不通的,因为我们必须通过实验方法来确定反应级数。在平衡化学方程式中,分子前面的值称为“化学计量系数”;化学计量是反应物和产物之间的数值关系。
2Na2O⟶4Na+O2
上述反应是平衡化学方程式的一个例子。它能分解氧化钠(Na2O)。该反应的正规方程或骨架方程为Na2O⟶Na+O2。平衡方程时,可采用两种方法:检验法和氧化数法。
检验方法包括通过观察反应物和产物来平衡化学方程式。在这个反应中,氧化钠是反应物,每个分子有两个钠原子和一个氧原子。但是在产物方面,有一个钠原子和两个氧原子。因此,首先,我们可以在反应物侧加一个化学计量系数,它是2。在反应物一侧,有四个钠原子和两个氧原子。由于产品侧也有两个氧原子,我们可以在产品侧加上“4”作为钠的化学计量系数,以平衡这个方程。现在两边的原子数相等,所以我们得到了一个平衡的化学方程式。
什么是基本方程(a skeleton equation)?
骨架方程给出了参与化学反应的反应物类型和最终产物。然而,这并不能给出反应物和产物之间的确切比例。因此,从骨架方程中可以得到的重要细节是反应的反应物,反应的产物和反应的方向。对于上述反应,骨架反应如下:;
Na2O⟶Na+O2
平衡方程(balanced equation)和骨架方程(skeleton equation)的区别
平衡方程和骨架方程的关键区别在于平衡方程给出了参与化学反应的每种反应物和产物的实际分子数,而骨架方程只给出了反应的反应物。此外,平衡方程可以包含也可以不包含化学计量系数,而骨架方程没有化学计量系数。例如,氧化钠分解的平衡化学方程为2Na2O⟶4Na+O2,骨架方程为Na2O⟶Na+O2。
下面的信息图总结了平衡方程和骨架方程之间的区别。

总结 - 平衡方程(balanced equation) vs. 骨架方程(skeleton equation)
平衡方程和骨架方程是一个特定化学反应的两种写法。综上所述,平衡方程和骨架方程的关键区别在于平衡方程给出了参与化学反应的每个反应物和产物的实际分子数,而骨架方程只给出了反应的反应物。
引用
1赫尔曼斯汀,安妮·玛丽。“平衡方程的定义和示例”,ThoughtCo,2019年9月17日,可在此处查阅。