pH值和缓冲液之间的关键区别在于,pH值是对数标度,而缓冲液是水溶液。
我们可以用液体的pH值来判断它是酸还是碱。它也有助于确定缓冲区的缓冲容量。缓冲溶液含有弱酸及其共轭碱的混合物,反之亦然。因此,它倾向于抵抗溶液pH值的变化。
目录
1. 概述和主要区别
2. 什么是pH
3. 什么是缓冲区
4. 并列比较——pH值与缓冲液的表格形式
5. 摘要
什么是酸碱度(ph)?
pH是一个对数标度,我们用来测定水溶液的酸碱度。它是氢离子浓度的负底10对数,单位为摩尔/升。如果我们更精确地表示它,我们应该使用氢离子的活性而不是浓度。pH标度有0到14之间的数字。pH值小于7的溶液是酸性的,如果pH值高于7,则为碱性溶液。pH7表示中性溶液,即纯水。
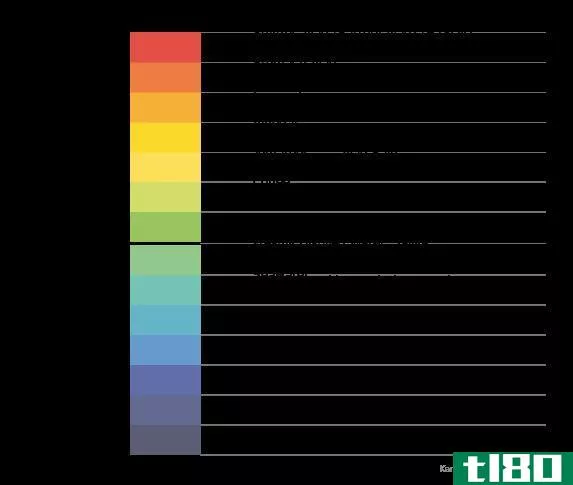
图01:不同组分的pH值
测定pH值的方程式如下:
pH=log10(aH+)
这里“a”是氢离子(H+)的活性。pH值取决于溶液的温度,因为温度可以改变化学物质的活性。因此,当给出水溶液的pH值时,我们应该指出精确测量pH值的温度。我们用pH标度来测定水、土壤等的质量。
什么是缓冲器(buffer)?
缓冲液是一种能抵抗pH值变化的水溶液。这种溶液含有弱酸及其共轭碱的混合物,反之亦然。加入强酸或强碱后,这些溶液的pH值会略有变化。
弱酸(或碱)与其共轭碱(或共轭酸)相互平衡。然后,如果我们在这个体系中加入一些强酸,平衡就会转向酸,它会利用加入的强酸释放出的氢离子形成更多的酸。所以,虽然我们预计在加入强酸后氢离子会增加,但不会增加太多。同样地,如果我们加入一个强碱,氢离子浓度的降低量小于预期的碱添加量。我们可以测量这种对pH值随缓冲容量变化的电阻。缓冲容量测量缓冲液对添加OH-离子(碱)后pH值变化的抵抗力。我们可以用如下公式给出:
β=dn/d(pH值)
其中β是缓冲容量,dn是添加碱基的微乎其微的量,d(pH)是pH的微小变化。
当考虑缓冲液的应用时,这些溶液对于保持生物体内酶活性的正确pH值是必要的。此外,它们还被用于工业发酵过程,为染料设置正确的条件,用于化学分析,校准pH计等。
酸碱度(ph)和缓冲器(buffer)的区别
pH是一个对数标度,我们用它来测定水溶液的酸碱度,而缓冲液是一种能够抵抗pH值变化的水溶液。这是pH值和缓冲液之间的关键区别。此外,pH值是化学中一个非常重要的刻度。我们可以用pH计或通过实验方法测量溶液的pH值。此外,我们使用pH标度来确定水、土壤等的质量。另一方面,缓冲溶液的使用是为了保持酶活性的正确pH值,在工业发酵过程中,在为染料设置正确的条件,在化学分析,校准pH计时,我们用化学分析法测量缓冲液的缓冲容量。

总结 - 酸碱度(ph) vs. 缓冲器(buffer)
pH是化学中用来测量溶液酸碱度的基本刻度。缓冲液是能够抵抗pH值变化的化学溶液。因此,pH值和缓冲液的区别在于pH值是对数刻度,而缓冲液是水溶液。
引用
1“博士”,维基百科,维基媒体基金会,2018年8月3日。在这里可以买到2。“缓冲解决方案”,维基百科,维基媒体基金会,2018年7月27日。可在此处查阅
2“缓冲解决方案”,维基百科,维基媒体基金会,2018年7月27日。