fda授权恢复期血浆治疗covid-19
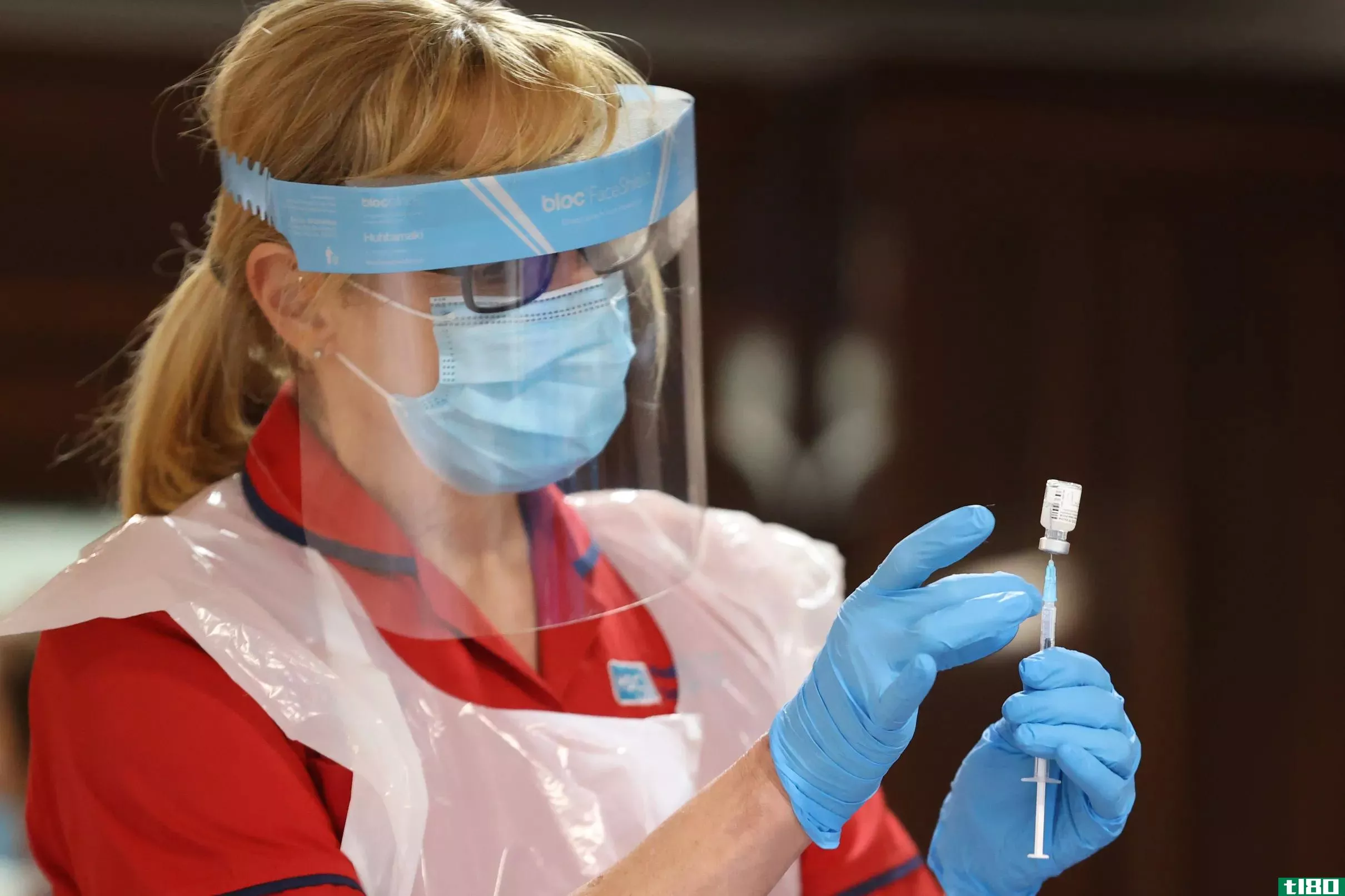
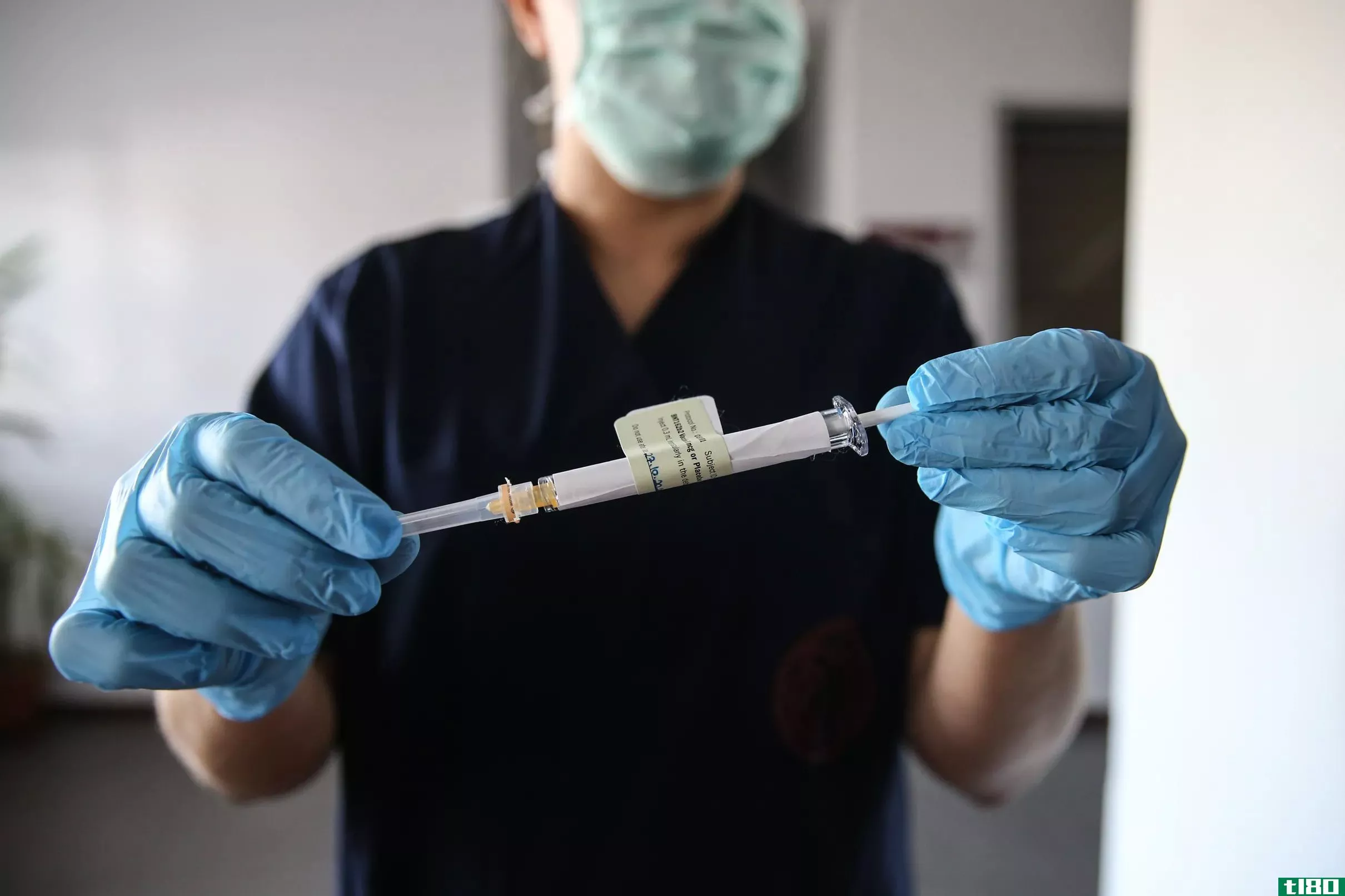
美国食品和药物管理局(Food and Drug Administration)授权紧急使用COVID-19幸存者的血浆作为对病人的治疗。此前,美国总统特朗普公开向该机构施压,要求其加快药物和疫苗的研发。
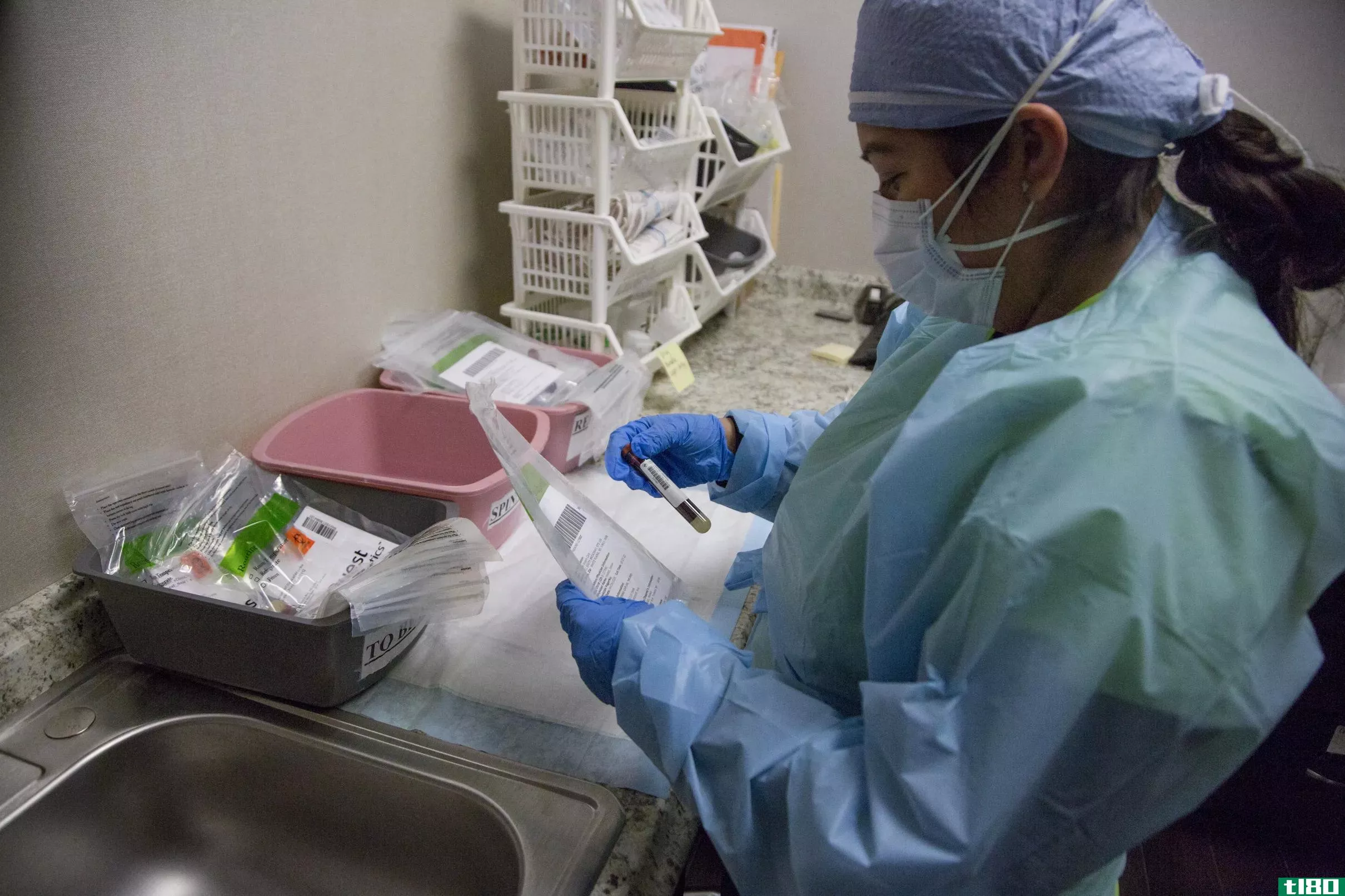
该机构在一份声明中说,血浆不应成为COVID-19治疗的新标准。但是,它可以缩短或降低住院患者的病情严重程度。专员斯蒂芬·哈恩在声明中说:“我们对早期看到的关于恢复期血浆的有希望的数据感到鼓舞。
初步研究表明,含有抗冠状病毒抗体的血浆有助于提高该病住院患者的存活率。然而,这种治疗方法只在一小部分COVID-19患者中进行了试验,而没有在能够给出明确答案的大型安慰剂对照临床试验中进行试验。
该机构指出,支持批准血浆的决定的证据并不是来自其关于医护人员恢复期血浆的情况说明书中的金标准随机临床试验。FDA在声明中说:“促进患者参与任何正在进行的随机临床试验,对于最终证明COVID-19恢复期血浆的安全性和有效性至关重要。”。
据《****》报道,美国食品和药物管理局(FDA)曾计划在8月初发布一份血浆紧急授权书,但由于卫生官员担心没有足够有力的数据支持该疗法,因此搁置了这些计划。一项大型血浆研究的数据发现,如果患者在确诊后三天内接受血浆治疗,其死亡率比之后接受血浆治疗的患者要低,但这些患者没有与安慰剂组进行比较。官员们决定更仔细地审查这些数据。
在上周的记者招待会上,美国总统唐纳德·特朗普(Donald Trump)在没有证据的情况下表示,推迟是出于政治动机。他说:“人们都快死了,如果它好的话,我们应该得到批准。”。他随后指责FDA在Twitter上拖延了COVID-19药物和疫苗的研发。
紧急授权并不是FDA的完全批准,但它表明FDA相信这种疗法的好处大于风险。另一种治疗方法,抗病毒药物remdesivir,被授权治疗COVID-19。
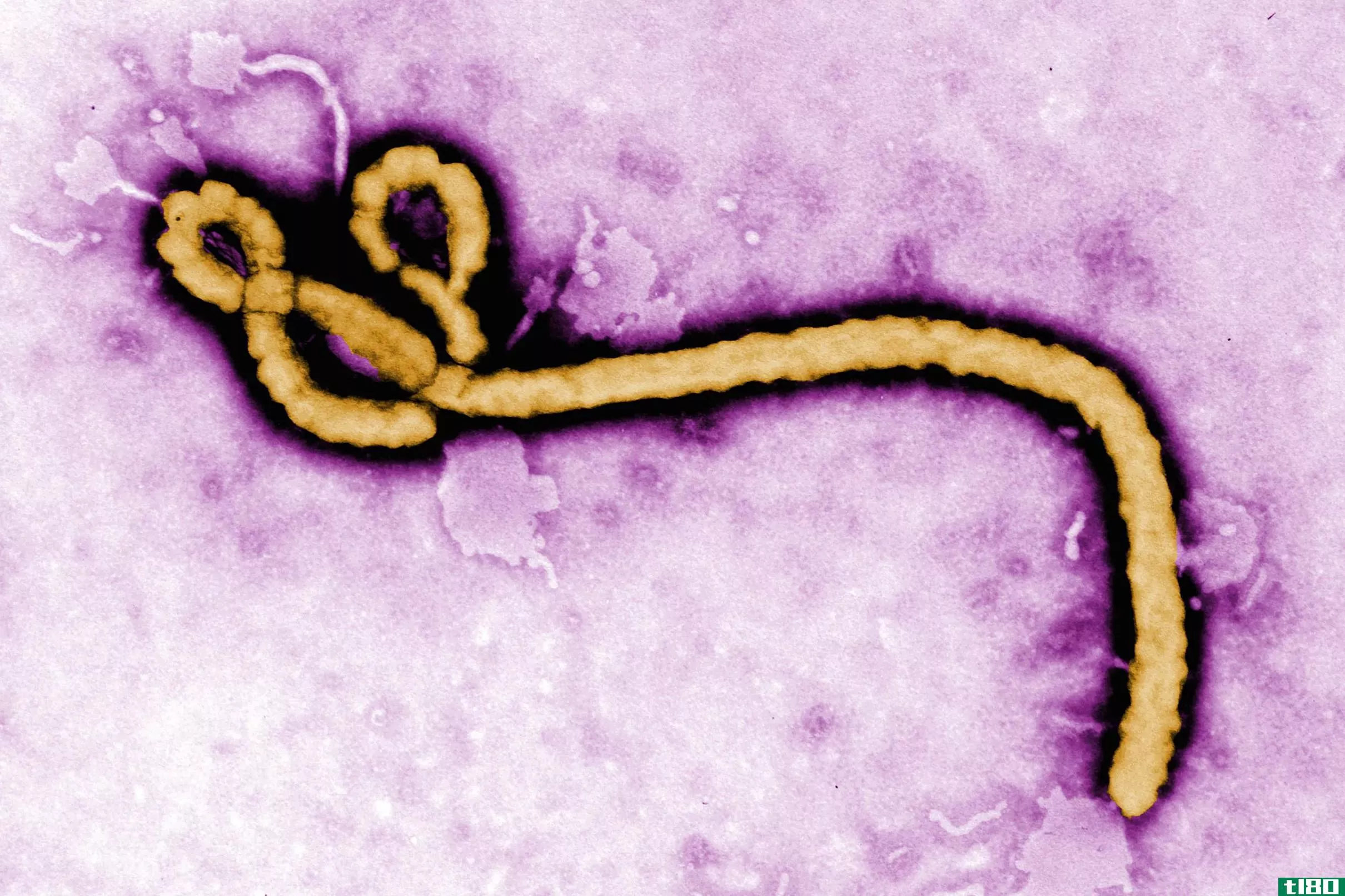
恢复期血浆是治疗传染病的一种老派方法;自19世纪90年代以来,它被用于治疗白喉、流感大流行和水痘。
埃利奥特·贝内特·格雷罗(Elliott Bennett Guerrero)今年4月在接受《边缘》杂志采访时说:“使用血浆,我们利用了人体产生抗体和对病原体免疫的惊人能力。”。“我们把这些保护性因素转移到那些生病的人身上,他们还不能产生免疫反应。”
美国数千名COVID-19患者已经通过临床试验和紧急访问计划接受了血浆治疗。自3月份以来,FDA一直在帮助协调这些努力。不过,新的授权将打破一些后勤障碍,使患者更容易获得治疗。
血浆治疗COVID-19的临床试验仍在进行中。科学家们也在研究输注血浆是否能像医护人员一样保护感染病毒的高危健康人群不生病。
美国卫生与公众服务部(Department of Health and Human Services)正在通过一系列公益广告(PSA)鼓励从COVID-19中康复的人捐献血浆,FDA也有一个网站指导人们前往捐献地点。
更新时间:美国东部时间8月23日下午5:46:FDA信息更新。
- 发表于 2021-04-18 03:33
- 阅读 ( 203 )
- 分类:互联网
你可能感兴趣的文章
亚马逊获得美国食品和药物管理局(fda)的授权,在家使用covid-19检测试剂盒
... Drug Administration)对其子公司STS-Lab-Holdco进行COVID-19检测的授权,并计划将其用于冠状病毒现场检测项目。 这项测试是用鼻自拭子来完成的,可以在卫生保健提供者的监督下完成,也可以作为家庭药箱的一部分,病人...
- 发布于 2021-04-16 05:54
- 阅读 ( 181 )
fda官员正在进行为期三周的冲刺,以审查强生covid-19疫苗的数据
...大大缩短了时间。从辉瑞公司和BioNTech公司申请该疫苗的授权到获得FDA的批准,花了21天的时间。哈恩去年12月在接受《华尔街日报》采访时表示,机构专家们在夜间和周末轮班工作,以便尽可能彻底、快速地浏览数据。 这种疫...
- 发布于 2021-04-16 08:16
- 阅读 ( 183 )
fda批准美国首例covid-19疫苗
...辉瑞生物技术公司(Pfizer BioNTech)COVID-19疫苗的紧急使用授权有可能改变美国流感大流行的进程。”。 这种疫苗在美国被批准用于16岁以上的人。在临床试验中发现它对预防症状性COVID-19有95%的有效性。“这是非同寻常的,”国...
- 发布于 2021-04-17 00:55
- 阅读 ( 157 )
美国第二个获得fda批准的moderna-covid-19疫苗
...。 与辉瑞/BioNTech疫苗一样,Moderna疫苗也将获得紧急使用授权,这一授权允许FDA在大流行等紧急情况下比正常审查过程更快地签署产品。 与辉瑞公司和BioNTech公司的疫苗相比,Moderna疫苗的储存要求不那么繁重,后者必须在超低温...
- 发布于 2021-04-17 03:54
- 阅读 ( 165 )
fda批准和授权有什么区别?
在大多数情况下,交替使用“批准”和“授权”是完全可以接受的。但在食品和药物管理局(FDA)就不行了,在COVID-19疫苗方面也绝对不行。如果这个话题是在你的Zoom假日聚会上提出来的,这里有一张关于这些类似术语具体用法...
- 发布于 2021-04-17 04:20
- 阅读 ( 154 )
制造商报告说,covid-19疫苗非常有效
... 在使用疫苗之前,它需要得到包括FDA在内的监管机构的授权,FDA将研究疫苗的安全性和有效性。目前还没有关于这种疫苗的严重安全问题的报道。但是今天公布的信息不包括有多少人患上了更严重的疾病,有多少人患上了更轻...
- 发布于 2021-04-17 07:01
- 阅读 ( 128 )
摩德纳说,其covid-19疫苗在早期分析中的有效率为94.5%
...辉瑞都表示,他们计划在几周内向食品和药物管理局申请授权。 这些数据还没有公布,也没有经过外部专家的审查。不过,这些疗效读数比许多专家预期的要高。FDA说他们正在寻找至少50%有效的疫苗。 “雄心勃勃地...
- 发布于 2021-04-17 08:19
- 阅读 ( 207 )
最新分析显示辉瑞疫苗的有效率为95%
...经收集了两个月的后续安全数据,这是FDA要求在公司申请授权前查看的数据。试验中没有出现严重的安全问题。最常见的副作用是疲劳和头痛。 辉瑞和BioNTech表示,他们计划向FDA申请疫苗的紧急使用授权(EUA),这与完全批准并...
- 发布于 2021-04-17 09:06
- 阅读 ( 203 )
摩德纳将向fda申请covid-19疫苗授权
...全性和94%的有效性后,Moderna计划于今天申请COVID-19疫苗的授权。这是继辉瑞(Pfizer)和生物科技(BioNTech)本月早些时候提交疫苗数据后,第二家向美国食品和药物管理局提交疫苗数据的公司。 在一份新闻稿中,Modern...
- 发布于 2021-04-17 11:10
- 阅读 ( 183 )
特朗普的covid-19经验证明不了什么
...ere! 抗体治疗可能是治疗COVID-19的好方法。该策略类似于恢复期血浆,含有恢复期患者产生的冠状病毒抗体。不过,这些药物不是血液中不可预测的抗体混合物,而是由一些似乎特别擅长阻断病毒的特定抗体组成的浓缩***。另一...
- 发布于 2021-04-17 13:52
- 阅读 ( 150 )