关键区别——冰点降低与沸点升高
由于添加了溶质,凝固点降低导致溶液在低于纯溶剂冰点的温度下冻结。由于溶质的加入,使溶液在比纯溶剂沸点更高的温度下沸腾。因此,冰点降低和沸点升高之间的关键区别在于,冰点降低降低了溶液的冰点,而沸点升高则增加了溶液的沸点。
冰点降低和沸点升高是物质的综合性质。这意味着它们只取决于溶质的数量,而不取决于溶质的性质。
目录
1. 概述和主要区别
2. 什么是冰点降低
3. 沸点升高是多少
4. 并列比较-冰点降低与沸点升高的表格形式
5. 摘要
什么是冰点降低(freezing point depression)?
冰点降低是指由于向溶剂中添加溶质而使溶剂的冰点降低。它是一个综合性质。这意味着冰点降低仅仅取决于溶质的数量,而不是溶质的性质。当凝固点降低时,溶剂的冰点降低到比纯溶剂低的值。冰点降低是海水即使在0°C(纯水的冰点)下仍保持液态的原因。冰点降低值如下所示。
ΔTf=Tf(溶剂)–Tf(溶液)
或者
ΔTf=Kfm
在这件事上,
- ΔTf是冰点下降,
- 溶剂的冰点是纯溶剂
- Tf(溶液)是溶液(溶剂+溶质)的冰点
- Kf是冰点下降常数
- m是溶液的摩尔浓度。
但是,添加的溶质应该是不挥发的溶质,否则溶质不影响溶剂的冰点,因为它很容易挥发。不仅是溶液,这个概念也可以用来解释固体混合物凝固点的变化。当存在杂质时,细粉固体化合物的冰点低于纯固体化合物(固体-固体混合物)。
凝固点是溶剂的蒸汽压和固体形式的蒸汽压相等的温度。如果向该溶剂中添加非挥发性溶质,则纯溶剂的蒸汽压降低。这样,即使在比正常凝固点更低的温度下,溶剂的固体形式也能与溶剂保持平衡。
什么是沸点升高(boiling point elevation)?
沸点升高是由于向溶剂中添加溶质而使溶剂的沸点升高。在这里,溶液的沸点(加入溶质后)比纯溶剂的沸点高。因此,溶液开始沸腾的温度高于通常的温度。
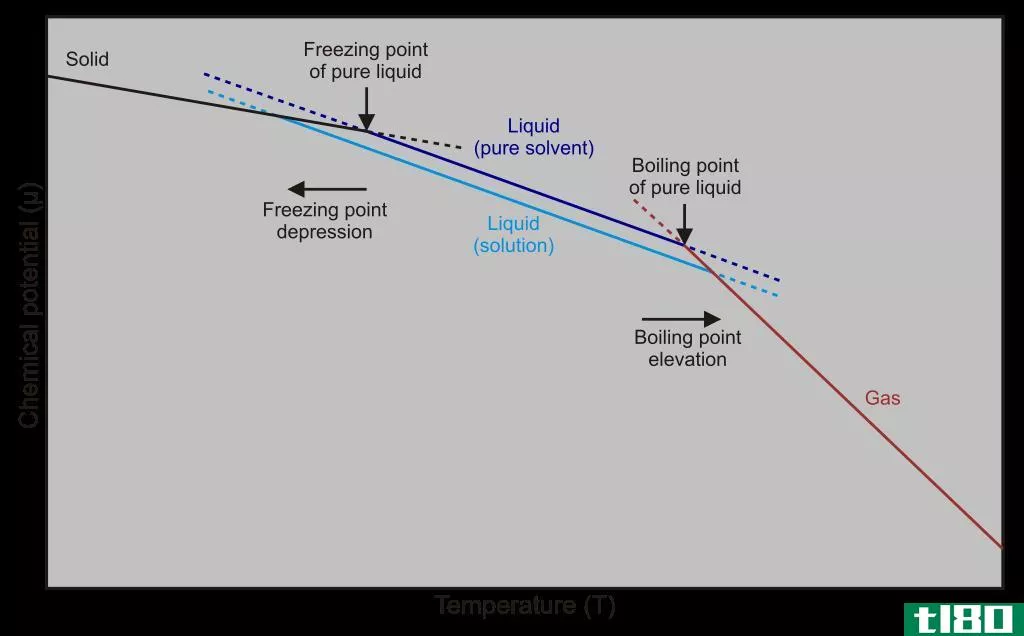
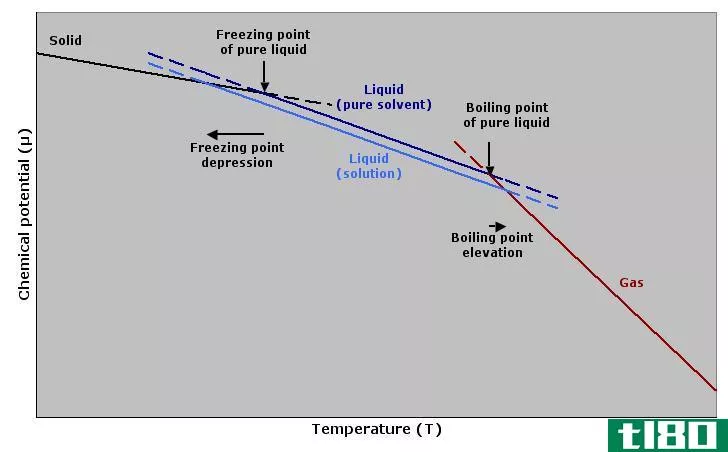
图01:纯溶剂和溶液(溶剂+溶质)的冰点和沸点差
但是,添加的溶质应该是不挥发的溶质,否则溶质会挥发而不是溶解在溶剂中。沸点升高也是一个综合性质,因此它只取决于溶质的数量(而不是溶质的性质)。
ΔTb=Tb(溶剂)–Tb(溶液)
或者
ΔTb=Kbm
在这件事上,
- ΔTb是沸点升高
- Tb(溶剂)是纯溶剂的沸点
- Tb(溶液)是溶液(溶剂+溶质)的沸点
- Kb是沸点上升常数
- m是溶液的摩尔浓度
这种现象的一个常见例子是水盐溶液的沸点。盐溶液在高于100℃的温度下沸腾(纯水的沸点)。
冰点降低(freezing point depression)和沸点升高(boiling point elevation)的区别
| 凝固点与沸点升高 | |
| 冰点降低是指由于向溶剂中添加溶质而使溶剂的冰点降低。 | 沸点升高是由于向溶剂中添加溶质而使溶剂的沸点升高。 |
| 温度 | |
| 冰点降低降低溶液的冰点。 | 沸点升高增加溶液的沸点。 |
| 原则 | |
| 凝固点降低导致溶液在比纯溶剂更低的温度下冻结。 | 沸点升高使溶液在比纯溶剂更高的温度下沸腾。 |
| 方程式 | |
| 冰点下降由ΔTf=Tf(溶剂)–Tf(溶液)或ΔTf=Kfm得出。 | 沸点升高ΔTb=Tb(溶剂)–Tb(溶液)或ΔTb=Kbm。 |
总结 - 冰点降低(freezing point depression) vs. 沸点升高(boiling point elevation)
冰点降低和沸点升高是物质的两个主要综合性质。凝固点降低和沸点升高的区别在于,凝固点降低降低了溶液的冰点,而沸点升高则增加了溶液的沸点。
引用
1.赫尔曼斯汀,安妮·玛丽。“沸点升高是什么以及它是如何工作的。”ThoughtCo.可在此处查阅2.“沸点升高”,维基百科,维基媒体基金会,2018年3月13日。此处提供3.“冰点降低”,化学剧本,歌词,2018年2月19日。可在此处获取
2.“沸点升高”,维基百科,维基媒体基金会,2018年3月13日。
3.“冰点降低”,化学剧本,歌词,2018年2月19日