蒸馏(distillation)和提取(extraction)的区别
尽管蒸馏和萃取是两种最常用的物理分离方法,在工业中对获得许多应用的纯化学品具有同等重要的作用,但蒸馏和萃取在其程序上存在差异。蒸馏和萃取的关键区别在于,蒸馏是在液体混合物加热后,在沸点处收集液体的蒸汽,然后将蒸汽冷凝,得到纯物质,而在萃取过程中,分离过程使用合适的溶剂。
什么是蒸馏(distillation)?
蒸馏法是一种最古老的,但仍然是最常用的分离液体混合物的方法,基于它们的沸点不同。它包括逐渐加热液体混合物,以达到混合物中液体的沸点,以获得不同沸点的蒸汽,然后冷凝蒸汽以获得液体形式的纯物质。
The liquids with lower boiling points (the most volatile substances) are boiled off first as the mixture is heated while less volatile substances remain in the mixture until the temperature in the mixture reaches to their boiling points. A specially design set of apparatus is used for the distillation process.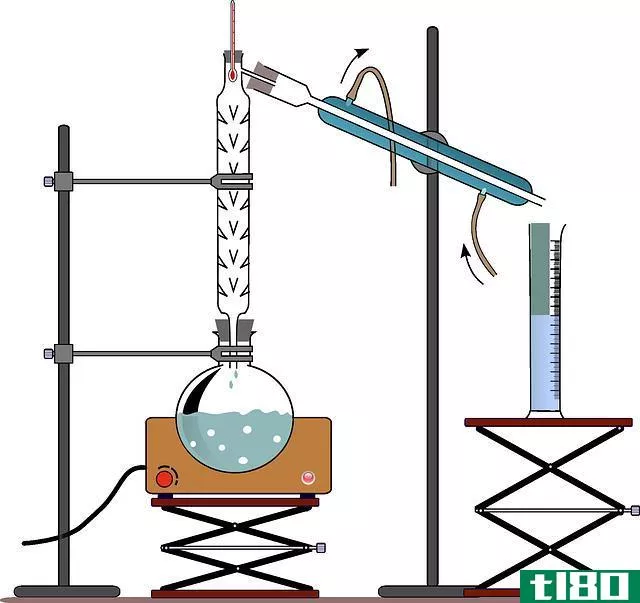
什么是提取(extraction)?
萃取过程包括使用适当的溶剂从固体或液体混合物中提取活性剂或废物。溶剂不完全或部分与固体或液体混溶,但可与活性剂混溶。活性剂通过与固体或液体的强烈接触从固体或液体混合物转移到溶剂中。溶剂中的混合相通过离心或重力分离方法分离。
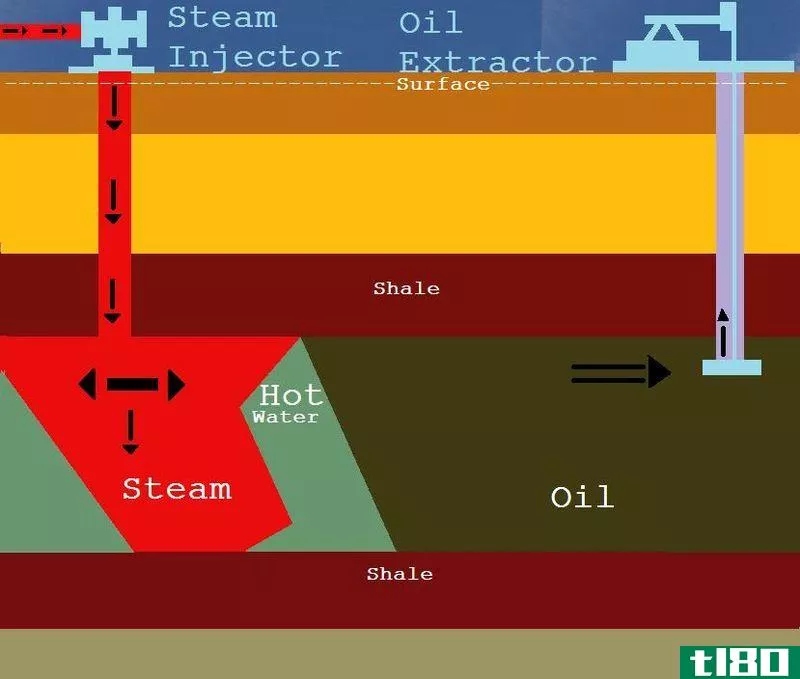
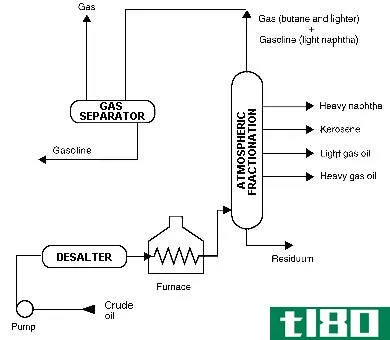
石油开采
蒸馏(distillation)和提取(extraction)的区别
蒸馏和萃取方法
蒸馏法
考虑一种由四种液体a、B、C和D组成的液体混合物。
沸点:B液体A(TA)>;B液体B(TB)>;B液体C(TC)>;B液体D(TD)
(挥发性最低的化合物)(挥发性最高的化合物)
混合物温度=Tm
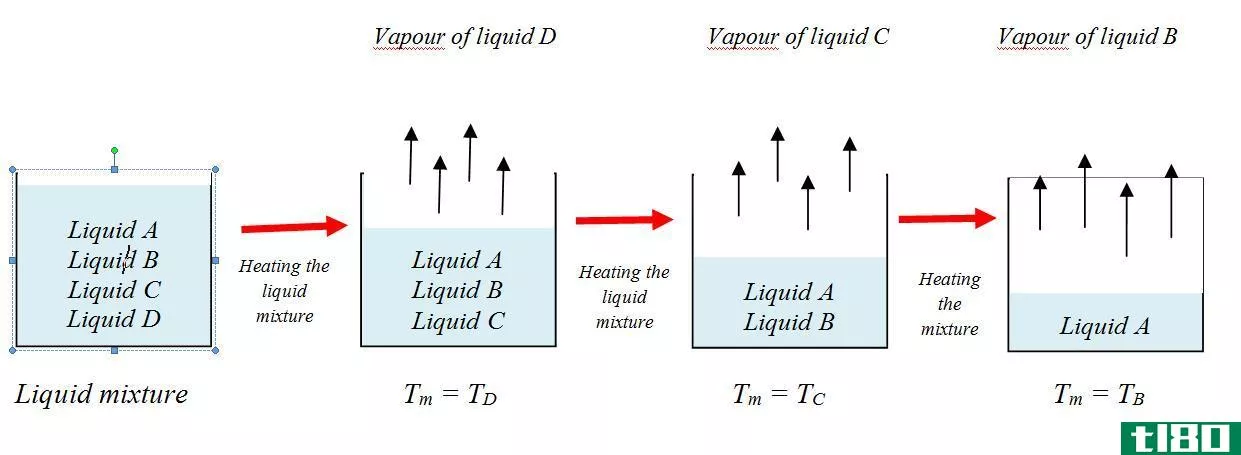
加热液体混合物时,当混合物的温度等于其沸点(Tm=TD)时,最易挥发的液体(D)首先离开混合物,而其他液体仍留在混合物中。液体D的蒸汽被收集并冷凝得到纯液体D。
当液体被进一步加热时,其他液体也会在沸点处沸腾。随着蒸馏过程的继续,混合物的温度升高。
萃取法
考虑活性物质A在液体B中,它们完全可混溶。溶剂C用于分离A和B。液体B和液体C不混溶。
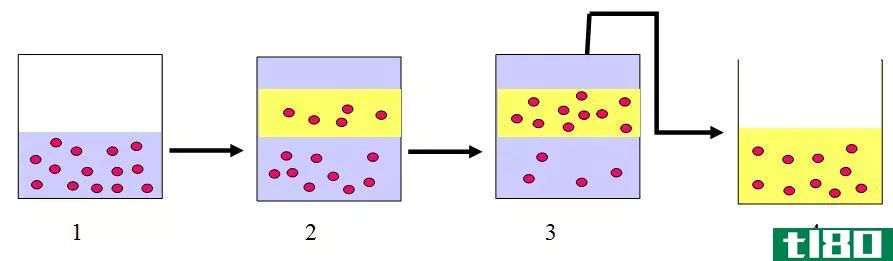
1: 物质A溶解在液体A中
2: 加入溶剂C后,液体A中的一些分子进入溶剂C
3: 随着时间的推移,更多的分子进入溶剂C(A在溶剂中的溶解度大于在液体A中的溶解度)
4: 溶剂C与液体A分离,因为它们是不混溶的。另一种方法是从溶剂中分离出A。
通过多次萃取使A和溶剂B完全分离。在此过程中温度是恒定的。
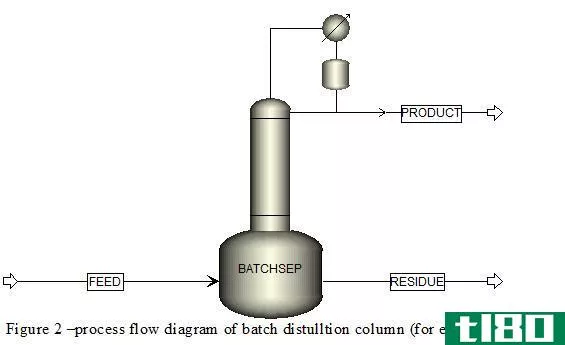
蒸馏和萃取类型
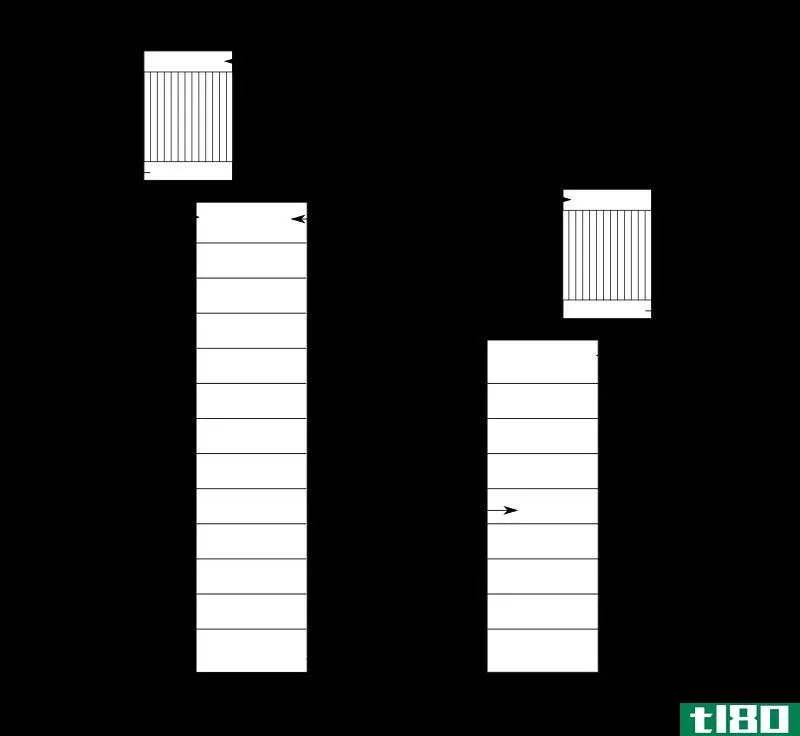
蒸馏:最常用的蒸馏方法是“简单蒸馏”和“分馏”。当要分离的液体沸点相差很大时,使用简单蒸馏。当要分离的两种液体具有几乎相同的沸点时,采用分馏法。
萃取:最常见的萃取类型是“固-液萃取”和“液-液萃取”。固-液萃取包括使用溶剂将物质从固体中分离出来。液体-液体萃取是指用溶剂从液体中分离出一种物质。
蒸馏和萃取的应用
蒸馏:这种分离方法用于原油生产、化工和石油工业的分馏。例如,从甲苯中分离苯,从水中分离乙醇或甲醇,从丙酮中分离醋酸。
萃取:用于从水中分离苯酚、苯胺和硝化芳香族化合物等有机化合物。它还可用于提取精油、药品、香料、香料和食品。
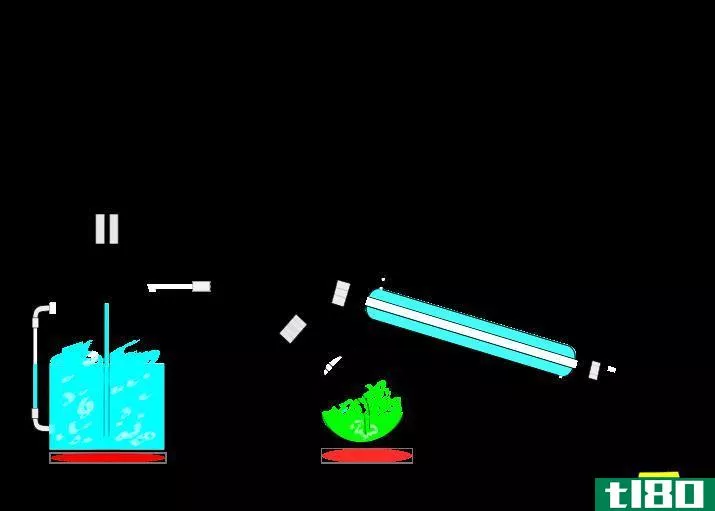
Image Courtesy: “The extraction of Oil using steam” by Micov at English Wikipedia. (CC BY-SA 3.0) via Comm***