绝热过程和等熵过程的关键区别在于绝热过程可以是可逆的,也可以是不可逆的,而等熵过程是可逆的。
在化学中,我们把宇宙分成两部分。我们感兴趣的部分是一个系统,其余部分是周围环境。一个系统可以是一个有机体,一个反应容器,甚至是一个细胞。我们可以根据系统之间的相互作用或发生的交换类型来区分它们。有时,物质和能量通过系统边界交换。交换的能量可以有光能、热能、声能等几种形式。如果一个系统的能量因温差而改变,我们称之为存在热量流动。然而,有些过程涉及温度变化,但没有热流;这些过程被称为绝热过程。等熵过程是一种绝热过程。
目录
1. 概述和主要区别
2. 什么是绝热过程
3. 什么是等熵过程
4. 并列比较-绝热过程与等熵过程的表格形式
5. 摘要
什么是绝热过程(adiabatic processes)?
绝热变化是指没有热量进入或流出系统的变化。主要有两种方法可以停止传热。或者说一个不能用热的边界进入。例如,在杜瓦瓶中发生的反应是绝热的。绝热过程发生的另一种方法是,当一个过程发生得非常快时,就没有时间将热量进出。
在热力学中,我们用dQ=0表示绝热变化。在这些情况下,压力和温度之间存在一种关系。因此,在绝热条件下,系统由于压力而发生变化。这就是在云形成和大尺度对流中发生的情况。在高海拔地区,大气压力较低。当空气变热时,它会上升。因为外界空气压力低,上升的空气包会试图膨胀。当膨胀时,空气分子会工作,这会影响它们的温度。这就是温度上升时温度降低的原因。
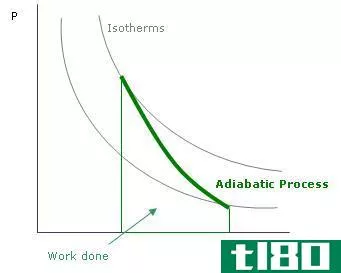
图01:图中的绝热过程
根据热力学,包裹体中的能量保持不变,但它可以被转换来做膨胀功或保持其温度。与外界没有热交换。同样的现象也适用于空气压缩(例如活塞)。在这种情况下,当空气包压缩时,温度升高。这些过程被称为绝热加热和冷却。
什么是等熵过程(isentropic processes)?
自发过程增加了宇宙的熵。当这种情况发生时,系统熵或周围的熵都可能增加。当系统熵保持不变时,就会发生等熵过程。
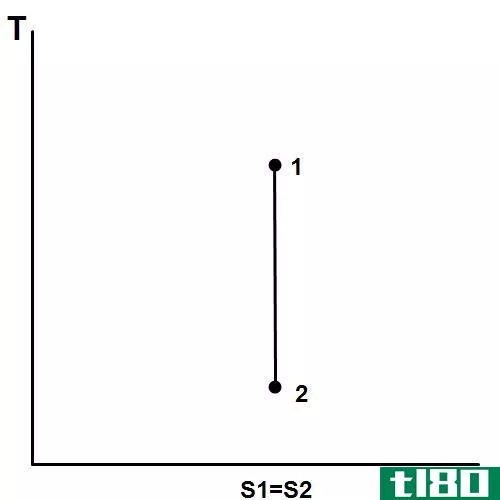
图02:等熵过程
可逆绝热过程是等熵过程的一个例子。此外,等熵过程中的常数参数是熵、平衡和热能。
绝热的(adiabatic)和等熵过程(isentropic processes)的区别
绝热过程是不发生传热的过程,而等熵过程是理想化的既绝热又可逆的热力学过程。因此,绝热过程和等熵过程的关键区别在于绝热过程可以是可逆的,也可以是不可逆的,而等熵过程是可逆的。此外,绝热过程发生在系统与周围环境之间没有任何热传递,而等熵过程发生时没有不可逆性,也没有热传递。
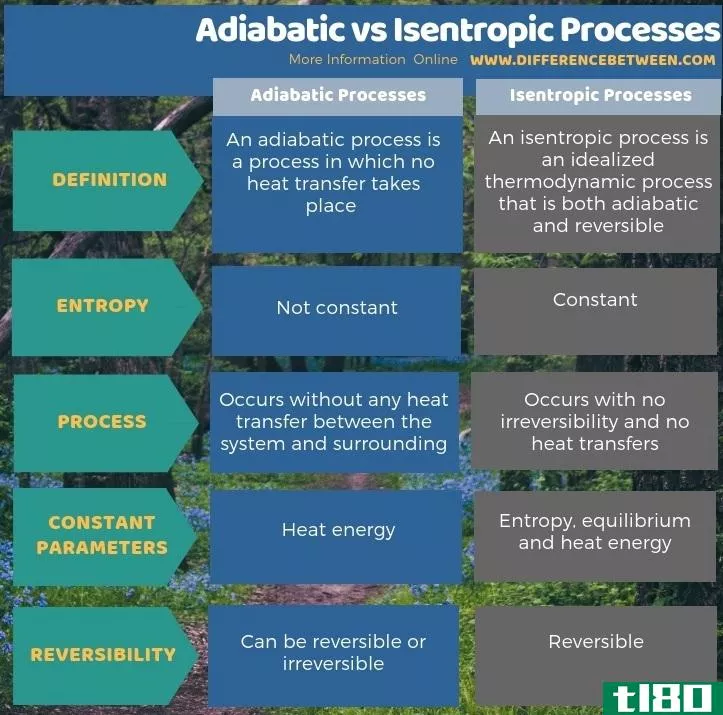
总结 - 绝热的(adiabatic) vs. 等熵过程(isentropic processes)
绝热过程是指不发生传热的过程。等熵过程是一个理想化的既绝热又可逆的热力学过程。因此,绝热过程和等熵过程的关键区别在于绝热过程可以是可逆的,也可以是不可逆的,而等熵过程是可逆的。
引用
1“热力学定律I”,《热力学与统计力学导论》,2005年,第14-31页。,doi:10.1002/047168175x.ch3。