主要区别
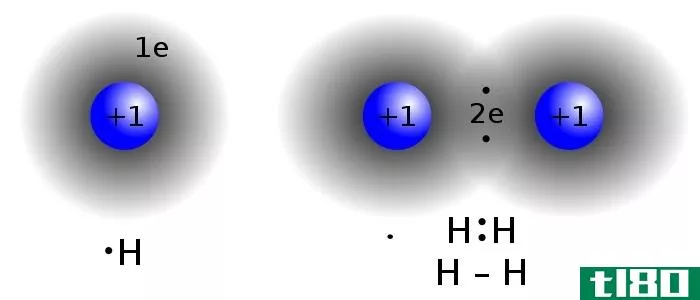
原子是一种元素中最小的粒子,它可能独立存在,也可能不独立存在;它的化学性质与元素相似。另一方面,这个分子是由另外两个原子通过化学键结合在一起组成的。分子可以以自由状态存在,并且可以进一步分成由它们组成的原子。例如,水分子由两个氢原子和一个氧原子结合而成。水分子在分裂时分裂成氢和氧的组成原子。
比较图
什么是分子(molecules)?
分子是物质的小单位,它总是以自由状态存在。它由两个或两个以上相似或不同的原子组成。分子的形成涉及到它们之间的化学键合。形成分子的键有几种类型;单键、双键和三键是原子通过化学键结合在一起的类型。分子可以进一步分成单个原子。尽管与原子相比,分子是更大的粒子,但肉眼还是看不见它们。像放大显微镜这样的科学装置被用来观察分子。分子不仅仅是单位,它们还描述物体的设置和物理状态。固体是绝对形状的,因为没有太大的空间让分子自由移动,所以被认为是紧密堆积的分子。另一方面,液体在分子之间有自由空间,并且不那么紧密地堆积,这就导致了液体可以形成任何被注入物体的形状的物理状态。在气态下,分子足够自由漂浮而不发生碰撞。我们知道分子是原子的结合体,对相同和不同原子结合的误解一直存在。当相同的原子结合形成分子时,它被称为元素的分子。与此相反,当不同元素的原子结合形成自由存在的分子时,它被称为化合物的分子。
什么是原子(atoms)?
原子是单位中最小的粒子,可以独立存在,也可以不独立存在;每个原子都具有与其元素相似的性质。它不能进一步分为亚原子粒子。在这里提到原子是生物体细胞的组成部分,宇宙中的一切都是由这些原子组成的。原子结合形成分子的比例很重要,就像它的不同可以产生不同的分子一样。仅仅是原子数量的变化就可以产生完全不同的分子。例如,两个氧原子结合形成氧分子,而当三个氧原子结合时,形成臭氧。原子不能通过显微镜或肉眼看到;它太小了,不能再分成它所组成的粒子。原子核是原子的中心部分,原子中间有质子和中子。质子带正电荷,而中子不带电荷。电子是原子的另一个重要粒子,带负电,它绕着原子核旋转。质子和中子是由夸克和胶子等化学成分组成的,在化学中没有太多的描述。
分子(molecules) vs. 原子(atoms)
- 原子是元素中最小的粒子,可以独立存在也可以不独立存在。另一方面,分子是化合物中最小的基本单位,总是以自由状态存在。
- 原子由亚原子粒子组成,如中子、质子和电子。与此相反,分子由两个或两个以上的原子组成。
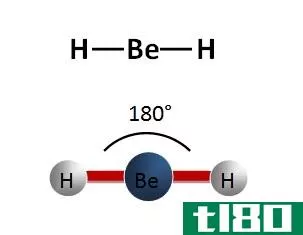
- 原子是球形的,而分子则是角的、线性的或矩形的。
- 分子是在化学键抓住原子后形成的。化学键可以有各种类型,单键、双键或三键。