vsepr公司(vsepr)和价键理论(valence bond theory)的区别
主要差异vsepr(main difference vsepr) vs. 价键理论(valence bond theory)
VSEPR和价键理论是化学中用来解释共价化合物性质的两种理论。VSEPR理论解释了分子中原子的空间排列。这个理论利用孤电子对和键电子对之间的排斥作用来预测某个分子的形状。价键理论解释了原子间的化学键。这个理论解释了轨道的重叠以形成sigma键或pi键。VSEPR和价键理论的主要区别在于,VSEPR描述了分子的几何结构,而价弯曲理论描述了分子中的化学键。
覆盖的关键领域
1.什么是VSEPR理论-定义、解释、实例应用2.什么是价键理论-定义、解释、实例应用3.VSEPR和价键理论的区别是什么-关键区别的比较
Key Terms: Covalent Bond, Geometry, Hybridization, Pi Bond, Sigma Bond, Valence Bond Theory, VSEPR Theory
什么是vsepr理论(vsepr theory)?
价壳层电子对排斥理论是预测分子几何结构的理论。利用VSEPR理论,我们可以提出具有共价键或配位键的分子的空间排列。这个理论是基于原子价层中电子对之间的排斥作用。电子对有键对和孤对两种类型。在这些电子对之间有三种类型的排斥作用。
- 键对-键对排斥
- 键对-孤对排斥
- 孤对-孤对排斥
产生这些排斥是因为所有这些对都是电子对;因为它们都带负电,所以彼此排斥。值得注意的是,这些排斥力并不相等。孤对产生的排斥比键对产生的排斥高。换句话说,孤对比键对需要更多的空间。
- 孤对排斥> 键对排斥
VSEPR理论可以用来预测电子几何和分子几何。电子几何结构是分子的形状,包括孤对。分子几何是只考虑键电子对的分子形状。
以下形状是利用VSEPR理论可以得到的分子的基本形状。

Figure 1: Table of Molecular Geometry
分子的几何结构是由中心原子周围的键对和孤对的数目决定的。中心原子通常是分子中其他原子中电负性最小的原子。然而,确定中心原子的最精确方法是计算每个原子的相对电负性。让我们考虑两个例子。
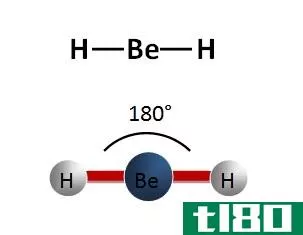
- BeCl2 (Beryllium Chloride)
The central atom is Be. It has 2 valence electr***. Cl atom can share one electron per atom. Therefore, the total number of electr*** around the central atom = 2 (from Be) + 1×2 (from cl atoms) = 4 Therefore, the number of electron pairs around the Be atom = 4 / 2 = 2 Number of single bonds present = 2 Number of lone pairs present = 2 – 2 = 0 Therefore, the geometry of BeCl2 molecule is linear.

Figure 2: Linear Structure of BeCl2分子
- H2O分子
中心原子是O。O周围的价电子数是6。每个原子H共享的电子数是1。因此,O=6(O)+1 x 2(H)=8,O=8的电子对数/2=4,O=2,O=2,O=2的单键数,H2O的几何形状是角形的。

Figure 3: Geometry of H2氧分子
当看上面两个例子时,两个分子都由3个原子组成。两个分子都有两个共价键。但是它们的几何形状是不同的。原因是H2O有2个孤对,而BeCl2没有孤对。O原子上的孤对排斥键电子对。这种排斥作用使两个键彼此靠近。但是由于两个键对之间的排斥作用,它们不能非常接近。也就是说,O原子周围的电子对之间存在净排斥。这就产生了一个角形分子而不是线性分子。在BeCl2分子中,由于没有孤对,所以没有孤对产生排斥作用。因此,只有键对发生排斥,并且键位于发生最小排斥的最远位置。
什么是价键理论(valence bond theory)?
价键理论是解释共价化合物中化学键的理论。共价化合物由通过共价键相互结合的原子组成。共价键是由于两个原子共享电子而形成的一种化学键。这些原子共享电子以填满它们的轨道并变得稳定。如果一个原子中有未配对的电子,那么它就不如一个有成对电子的原子稳定。因此,原子形成共价键以使所有电子配对。
原子的壳层中有电子。这些壳层由s、p、d等子壳层组成,除s子壳层外,其它子壳层由轨道组成。每个子壳中的轨道数如下所示。
| 子壳 | 轨道数 | 轨道名称 |
| s | 0 | – |
| p | 三 | 像素,像素,像素 |
| d | 5 | dxz、dxy、dyz、dx2y2、dz2 |
每个轨道最多能容纳两个自旋相反的电子。价键理论表明,电子的共享是通过轨道重叠而发生的。由于电子被原子核吸引,电子不能完全离开原子。因此,这些电子在两个原子之间是共享的。
有两种共价键被称为sigma键和pi键。这些键是由于轨道的重叠或杂化而形成的。杂交之后,两个原子之间形成了一个新的轨道。新的轨道是根据杂交的类型命名的。sigma键总是由于两个s轨道的重叠而形成的。当两个p轨道重叠时形成π键。
但当s轨道与p轨道重叠时,它不同于s-s轨道重叠和p-p轨道重叠。为了解释这种键合,科学家莱纳斯·鲍林发现了轨道杂化。杂化导致杂化轨道的形成。杂化轨道主要有以下三种类型。
sp3杂化轨道
这个轨道是在s轨道和3p轨道杂交时形成的(S轨道是球形的,p轨道是哑铃形的。因此,原子现在有4个杂化轨道。
sp2杂化轨道
这个轨道是由一个s轨道和两个p轨道杂交而成的。它的形状不同于s轨道和p轨道。原子现在有3个杂化轨道和一个非杂化的p轨道。
sp杂化轨道
这个轨道是s轨道和p轨道杂交形成的。它的形状不同于s轨道和p轨道。现在原子有2个杂化轨道和2个非杂化p轨道。

Figure 04: Shapes of Hybrid Orbitals
vsepr公司(vsepr)和价键理论(valence bond theory)的区别
定义
VSEPR:VSEPR理论是预测分子几何结构的理论。
价键理论:价键理论是解释共价化合物中化学键的理论。
基础
VSEPR:VSEPR理论是基于孤电子对和键电子对之间的排斥作用。
价键理论:价键理论是基于轨道重叠形成化学键。
轨道
VSEPR:VSEPR理论没有给出分子中原子轨道的细节。
价键理论:价键理论给出了分子中原子轨道的细节。
几何学
VSEPR:VSEPR理论给出了分子的几何结构。
价键理论:价键理论没有给出分子的几何结构。
化学键合
VSEPR:VSEPR理论没有指出原子间存在的键的类型。
价键理论:价键理论指出原子间存在的键的类型。
结论
VSEPR理论和价键理论都是为了理解化学物种的形状和成键而发展起来的基本理论。这些理论适用于具有共价键的化合物。VSEPR和价键理论的区别在于,VSEPR理论解释了分子的形状,而价键理论解释了分子中原子间化学键的形成。
引用
1.杰西A。凯和大卫W。“球。”化学导论-加拿大第一版。“价键理论和杂化轨道”化学导论-加拿大第一版。N.p.,N.d.网站。这里有。2017年7月28日。 2.《价键理论解释——无限开放教科书》,无限。2016年8月19日。网络。这里有。2017年7月28日。 2.《价键理论解释——无限开放教科书》,无限。2016年8月19日。网络。
- 发表于 2021-06-29 09:45
- 阅读 ( 680 )
- 分类:科学
你可能感兴趣的文章
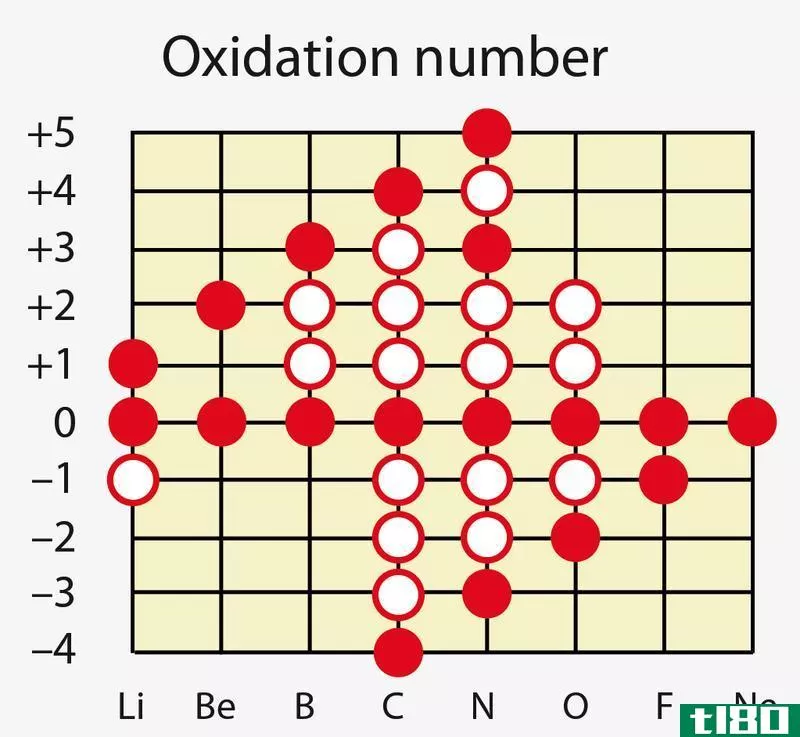
价(valency)和氧化值(oxidation number)的区别
...另一个原子形成键而可以失去或获得的电子数。 氧化数和价电子与原子的价电子有关。价电子是占据原子最外层轨道的电子。这些电子对原子核的吸引力很弱;因此,原子可以很容易地移除或与其他原子共享这些电子。这种电...
- 发布于 2020-10-15 12:44
- 阅读 ( 301 )
分子轨道理论(molecular orbital theory)和杂交理论(hybridization theory)的区别
...确定分子的电子结构和轨道结构。VSEPR理论、Lewis理论、价键理论、杂化理论和分子轨道理论是这些重要的理论。其中最能被接受的理论是分子轨道理论。 目录 1. 概述和主要区别 2. 什么是分子轨道理论 3. 什么是杂交理论 4. 并列...
- 发布于 2020-10-15 22:50
- 阅读 ( 835 )
激进的(radical)和价(valency)的区别
自由基和价态的关键区别在于,自由基是一种具有不成对电子的化学物种,而价是一个化学概念,它描述了一种化学元素与另一种化学元素结合的能力。 自由基是一种非常活泼的化学物质,因为它有一个不成对的电子。价是...
- 发布于 2020-10-17 02:38
- 阅读 ( 399 )
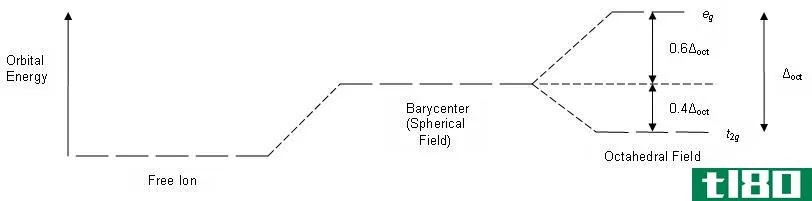
晶体场理论(crystal field theory)和配位场理论(ligand field theory)的区别
...作用。配体场理论(LFT)将金属与配体的相互作用视为共价键的相互作用,并依赖于金属与配体上d-轨道的取向和重叠。这是晶体场理论和配体场理论的关键区别。 什么是晶体场理论(crystal field theory)? 晶体场理论(CFT)由物理...
- 发布于 2020-10-24 03:34
- 阅读 ( 742 )
形状(shape)和分子几何学(geometry of a molecule)的区别
...几何结构的理论。我们可以用这个VSEPR模型来提出具有共价键或配位键的分子的空间排列。这个理论的基础是原子价壳层中电子对之间的斥力。在这里,我们可以找到两种类型的电子对,即键对和孤对。在这些电子对之间有三种...
- 发布于 2020-11-02 15:58
- 阅读 ( 507 )
分子轨道理论(molecular orbital theory)和价键理论(valence bond theory)的区别
分子轨道理论和价键理论的主要区别在于,分子轨道理论描述的是分子轨道的形成,而价键理论描述的是原子轨道的形成。 不同的分子具有不同的化学和物理性质,不同的原子连接起来形成这些分子。为了了解原子和分子性...
- 发布于 2020-11-03 20:05
- 阅读 ( 455 )
配价(valency)和价电子(valence electrons)的区别
...子。正是价的概念导致了与化学键有关的现代理论,如;价键理论,路易斯结构,分子轨道理论,价壳电子对排斥理论。主族元素通常表现为一价,而过渡金属则以多价著称。 Valence bond theory: Two p-orbitals forming a π-bond. 什么是价...
- 发布于 2021-06-27 10:49
- 阅读 ( 594 )
离子共价(ionic covalent)和金属键(metallic bonds)的区别
...子结合在一起的力。主要有三种类型的键,即离子键、共价键和金属键。二次键包括色散键、偶极键和氢键。一次键具有较高的键能,与二次力相比,它更稳定。离子共价键与金属键的主要区别在于它们的形成;当一个原子向另...
- 发布于 2021-06-28 11:41
- 阅读 ( 808 )
晶场理论(crystal field theory)和配位场理论(ligand field theory)的区别
....Bothara,K。G(2008). 无机药物化学。普拉加蒂图书私人有限公司。。 Image Courtesy:1.”Octahedral crystal-field splitting.”By English Wikipedia user YanA (CC BY-SA 3.0) via Comm*** Wikimedia2. “LFTi(III)”By Smokefoot at English Wikipedia – Transferred from en.*********...
- 发布于 2021-06-28 14:30
- 阅读 ( 650 )
配价(valency)和共价性(covalency)的区别
...电子数,而共价态是原子利用其空轨道可以形成的最大共价键数。 覆盖的关键领域 1.什么是价-定义、性质、示例2.什么是共价-定义、性质、示例3.价和共价之间的区别是什么-关键区别的比较 Key Terms: Atom, Covalency, Covalent Bond, Elect...
- 发布于 2021-06-29 08:25
- 阅读 ( 357 )