分子和晶格的关键区别在于,分子中含有相互结合的原子,而晶格包含相互结合的原子、分子或离子。
原子结合在一起形成各种化学物质。根据它们的排列,它们的性质会发生变化。原子相互结合时最简单的单位是分子。如果大量的原子、离子或分子相互结合,那么结果就是晶格。晶格具有高度有序的结构和非常高的摩尔质量。
目录
1. 概述和主要区别
2. 什么是分子
3.什么是格子
4. 并列比较-分子与晶格的表格形式
5. 摘要
什么是分子(a molecule)?
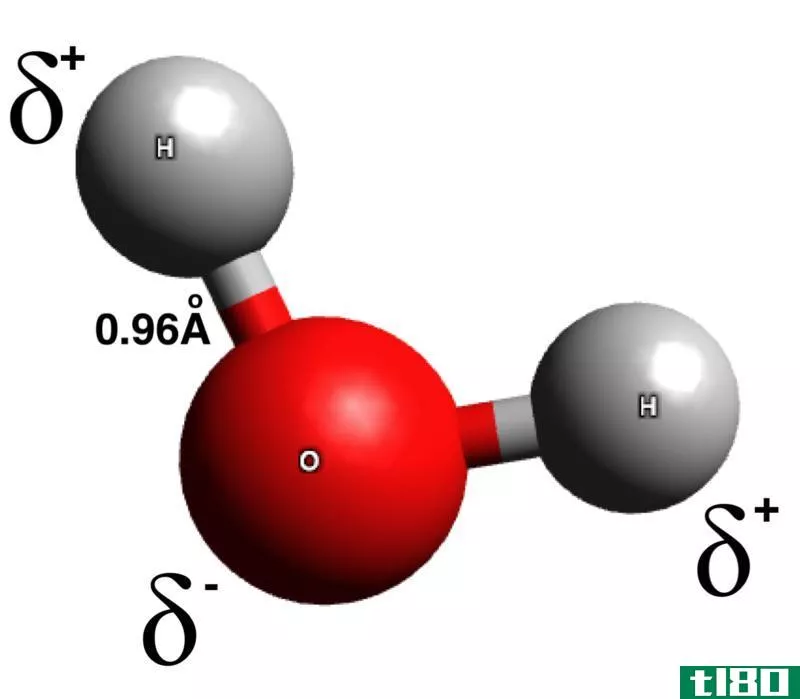
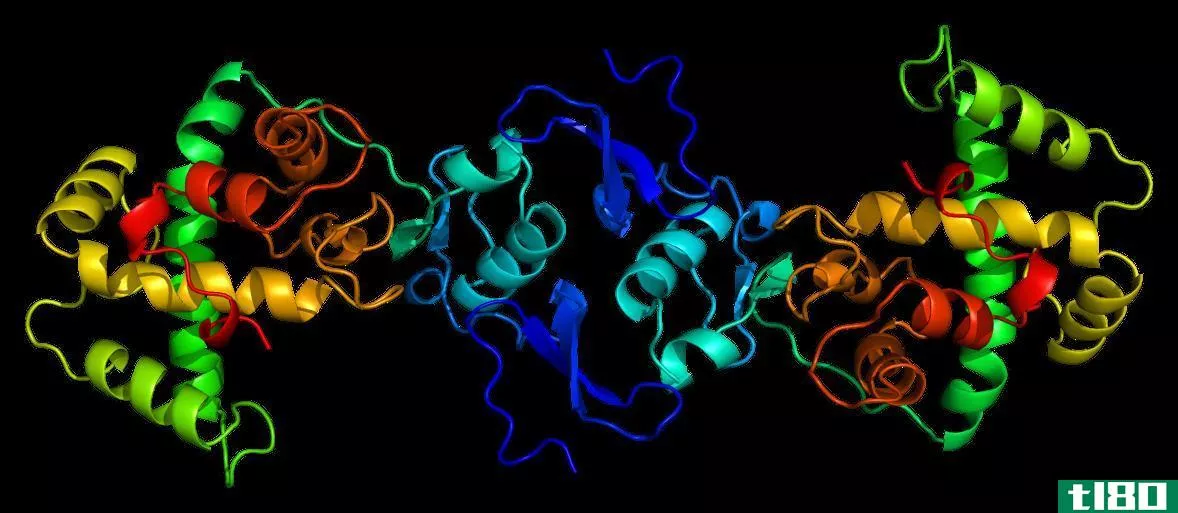
分子是由同一元素(例如,O2、N2)或不同元素(H2O、NH3)的两个或多个化学结合的原子组成。分子没有电荷,原子通过共价键相互结合。此外,它们可以非常大(血红蛋白)或非常小(H2),这取决于相互连接的原子数。

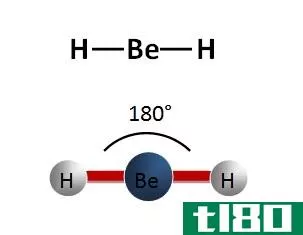
图01:水分子
分子式表示分子中原子的种类和数量。经验公式给出了分子中原子的最简单整数比。例如,C6H12O6是葡萄糖的分子式,CH2O是经验式。分子质量是我们考虑分子式中原子总数而计算的质量。此外,每个分子都有自己的几何结构。此外,分子中的原子以最稳定的方式排列,具有特定的键角和键长,以使排斥力和应变力最小化。
什么是格子(a lattice)?
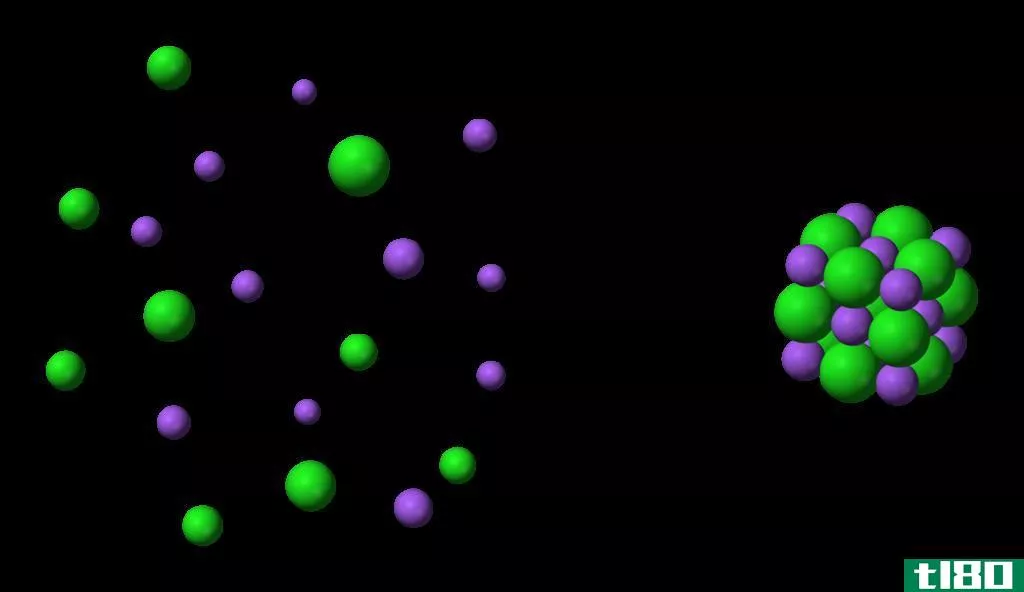
晶格是一个原子网络,具有有序结构。在化学中,我们可以看到不同类型的离子晶格和共价晶格。我们可以把晶格定义为具有基本单元三维有序排列的实体。基本单位可以是原子、分子或离子。因此,晶格是具有这些重复基本单位的晶体结构。
此外,如果这个网络包含离子键连接的离子,我们称之为离子晶体。例如,氯化钠是一种离子晶格。钠是一种1族金属,因此形成一个+1带电荷的阳离子作为它最稳定的阳离子。氯是一种非金属物质,具有形成a-1负离子的能力。在晶格中,六个氯离子围绕着每个钠离子,反之亦然。由于离子间的静电吸引,晶格结构非常稳定。晶格中存在的离子数随晶格的大小而变化。晶格能或晶格焓是晶格中离子键强度的量度。通常晶格焓是放热的。
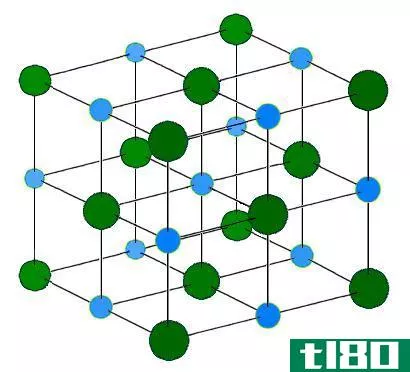
图02:氯化钠晶格结构
金刚石和石英是三维共价晶格的两个例子。金刚石只由碳原子组成,每个碳原子与另外四个碳原子共价结合形成晶格结构。所以每个碳原子都有四面体排列。由于这种结构,金刚石具有很高的稳定性。(钻石是地球上最强的矿物之一)石英或二氧化硅也有共价键,但这些键存在于硅和氧原子(不同原子的晶格)之间。这两种共价晶格都有很高的熔点,它们不能导电。
分子(molecule)和格子(lattice)的区别
两个或两个以上的原子通过共价化学键或离子键相互结合而形成的分子。另一方面,当大量的原子、分子或离子相互结合形成规则的网络结构时,就会形成晶格。因此,分子和晶格的关键区别在于,分子包含相互结合的原子,而晶格包含相互结合的原子、分子或离子。
作为分子和晶格的另一个重要区别,我们可以说分子可以是固体、液体或气体,而晶格只作为固体物质存在。此外,与晶格相比,分子的质量非常低,因为晶格中原子的数量相对较高。
分子和晶格的差异信息图如下所示。
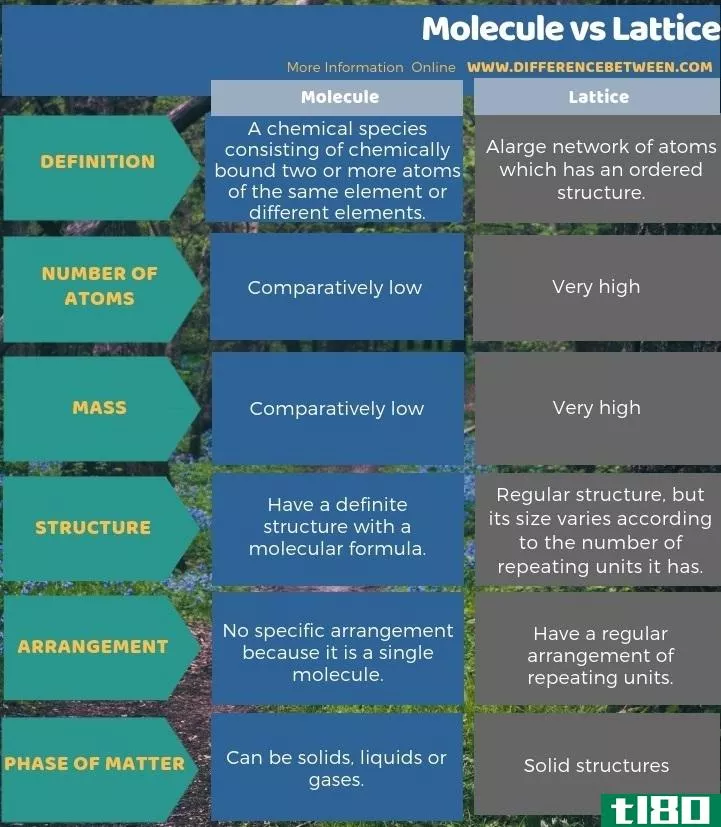
总结 - 分子(molecule) vs. 格子(lattice)
分子和晶格是化学中两个重要的化学术语。它们彼此不同,因此我们不能互换使用。分子和晶格的关键区别在于,分子包含相互结合的原子,而晶格包含相互结合的原子、分子或离子。
引用
1歌词。“离子结构”,化学剧本,国家科学基金会,2017年6月19日。在这里可以买到2。赫尔曼斯汀,安妮·玛丽博士,“什么是分子?“ThoughtCo,2018年6月11日。可在此处获取
2赫尔曼斯汀,安妮·玛丽博士,“什么是分子?“ThoughtCo,2018年6月11日