主要区别
摩尔浓度和当量浓度之间的主要区别在于,摩尔浓度被认为是化合物混合物中存在的摩尔数,而当量浓度被认为是化合物混合物中存在的化合物的克当量数。
摩尔浓度(molarity) vs. 正态性(normality)
摩尔浓度被认为是一种化合物在一升溶液中的摩尔数,而当量浓度是一公升溶液中以克当量表示的溶液量。摩尔浓度的单位是摩尔/升;另一方面,当量浓度的单位是eq/L或meq/L。溶液中摩尔浓度的依赖性并不取决于溶质所经历的反应类型;相反,溶液中正态性的依赖性取决于溶质所经历的反应类型。
溶液的摩尔浓度可以通过增加体积来改变温度的变化;另一方面,溶液的当量浓度不受温度变化的影响。溶液的摩尔浓度通常取决于体积、温度、溶质的溶解度以及溶液中更多溶质的添加量;另一方面,溶液的当量浓度通常取决于正态溶液中通常存在的活性组分。摩尔浓度用“M”表示,而当量浓度通常用“N”表示
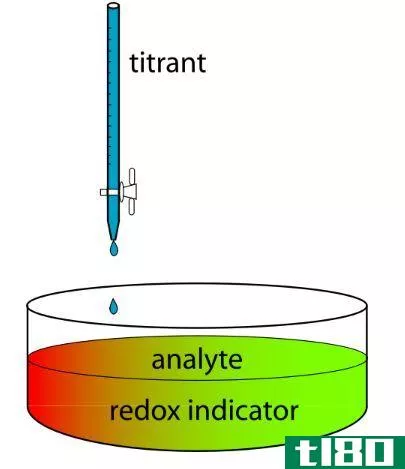
摩尔浓度被视为浓度单位,用于通过实验计算温度变化,而当量浓度通常用于滴定计算。摩尔浓度示例描述为1M H2SO4溶液,通常每升溶液含有1摩尔H2SO4;相反,正态性示例为1M H2SO4含有2 N摩尔摩尔浓度,因为每升溶液中通常存在2摩尔H+离子。
摩尔浓度可通过N=M*N转换为当量浓度,其中“N”被视为1升溶液中的当量数。计算摩尔浓度的公式写为“摩尔浓度=溶质摩尔数/溶液升”;另一方面,计算当量浓度的公式写为“当量摩尔数/1升溶液”。
比较开图表
什么是摩尔浓度(molarity)?
摩尔浓度一词定义为每升溶液中一种化合物在溶质中的摩尔数。摩尔浓度用“M”来表示。摩尔浓度也被称为摩尔浓度,因为它通常通过摩尔每升给出化合物的浓度。摩尔浓度的单位是摩尔/升,通常用于计算溶液的摩尔浓度。
然而,摩尔浓度的测量是以升为单位的,所以溶液的摩尔浓度是根据溶液(如液体)来测量的。溶液由溶质和溶剂组成,其中溶质通常溶解在溶剂中,这种溶剂和溶质的混合物称为溶液。
以摩尔浓度为浓度单位,通过实验计算温度变化。溶液的摩尔浓度可以通过增加体积来改变温度。溶液中摩尔浓度的依赖性并不取决于溶质所经历的反应类型,但溶液的摩尔浓度通常取决于体积、温度、溶质的溶解度以及溶液中更多溶质的加入。
一公升溶液中存在的溶质量称为溶液的摩尔浓度。所以摩尔浓度是用溶液中的摩尔数除以特定溶液的体积来计算的。摩尔浓度可通过N=M*N转换为当量浓度,其中“N”被视为1升溶液中的当量数。
摩尔浓度的一个例子是1M H2SO4溶液,每升溶液通常含有1摩尔H2SO4。溶液的摩尔数为摩尔数。
什么是正态性(normality)?
术语正态性的定义是溶液中存在的摩尔数,这些摩尔数相当于每升溶液的重量。因此,当量浓度也被称为溶液的当量浓度。正态性的单位计算为eq/L或meq/L,通常用“N”表示
对于较小规模的计算,使用单位meq/L,它代表“毫当量”。正态性通常用于描述酸碱反应中存在的羟基离子(OH-)和氢离子(H3O+)的浓度。
正态性方程为正态性=摩尔当量数/1L溶液。正态性的例子是1M H2SO4含有2N的摩尔浓度,因为每升溶液中通常存在2摩尔H+离子。但是,当硫酸用于沉淀反应时,作为反应物的硫化物通过硫酸沉淀,然后硫酸的当量浓度变为1N,因为从反应中释放出一个硫酸根离子。
主要区别
- 一种化合物在一升溶液中的摩尔量称为摩尔浓度,而以克为单位的溶液量(对应于一升溶液中重量的溶质)称为当量浓度。
- 摩尔浓度的单位是摩尔/升;另一方面,当量浓度的单位是eq/L或meq/L。
- “摩尔浓度=溶质摩尔数/溶液升”是计算摩尔浓度的公式;另一方面,“当量浓度=摩尔当量数/1升溶液”是计算当量浓度的公式。
- 存在于溶液中的摩尔浓度依赖于溶质所经历的反应形式;相反,溶液中存在的正态性依赖于溶质所经历的反应类型。
- 通过温度的变化,溶液的摩尔浓度也会随着体积的增加而改变;另一方面,温度的变化不会影响溶液的当量浓度。
- 溶液的摩尔浓度通常受体积、温度、溶质溶解度和溶液中添加更多溶质的影响;另一方面,溶液的当量浓度通常受正态溶液中通常存在的活性物质的影响。
- 摩尔浓度用“M”表示,而当量浓度通常用“N”表示
- 1M H2SO4溶液通常每升含有1摩尔H2SO4溶液是摩尔浓度的例子;相反,1M H2SO4含有2N的摩尔浓度,因为每升溶液中通常存在2摩尔的H+离子,这是正态性的例子。
- 当N=M*N时,摩尔浓度可变为当量浓度,其中“N”为1升溶液中对应物的数量。
结论
上述讨论得出结论,摩尔浓度和当量浓度的值彼此不同,因为摩尔浓度用于计算温度变化,而当量浓度通常用于滴定计算。摩尔浓度是指化合物混合物中存在的摩尔数,而当量浓度是指化合物混合物中存在的一种化合物的克数。