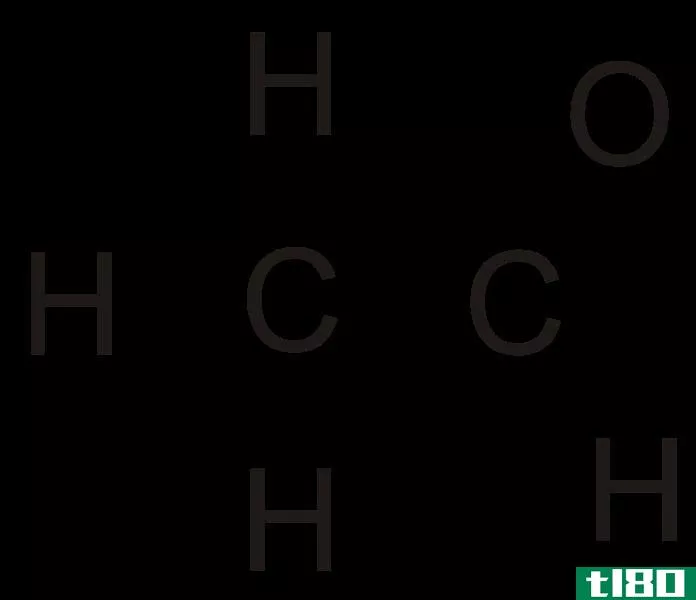
甲烷(methane)和乙烷(ethane)的区别
甲烷和乙烷是烷烃家族中最小的成员。这两种有机化合物的分子式分别为CH4和C2H6。甲烷和乙烷的主要区别在于它们的化学结构;一个乙烷分子可以看作是两个作为甲基二聚体相连的甲基。其他的化学和物理差异主要是由这种结构差异引起的。
什么是甲烷(methane)?
甲烷是烷烃家族中最小的成员,化学式为CH4(四个氢原子与一个碳原子结合)。它被认为是天然气的主要成分。甲烷是一种无色、无味、无味的气体,也被称为卡宾、沼气、天然气、四氢碳和碳化氢。它很容易被点燃,而且它的蒸气比空气轻。
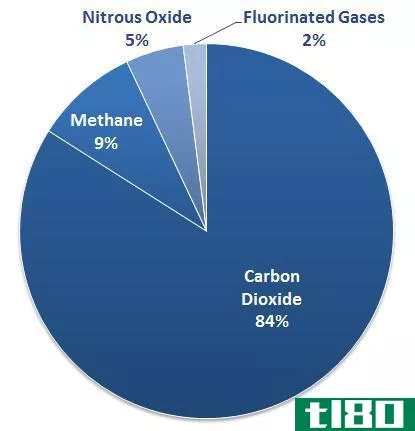
Methane is naturally found under the ground and under the sea floor. The atmospheric methane is c***idered as a greenhouse gas. Methane breaks down into CH3– with water in the atmosphere.
什么是乙烷(ethane)?
Ethane is a colourless, odorless gaseous compound at standard temperature and pressure. Its molecular formula and molecular weight are C2H6 and 30.07 g·mol−1 respectively. It is isolated from natural gas, as a byproduct from petroleum refining process. Ethane is very important in ethylene production. 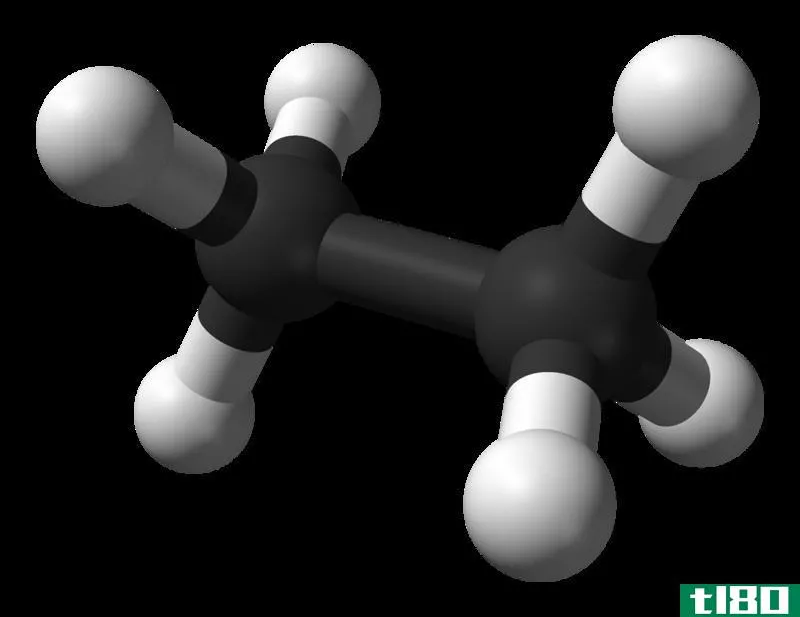
甲烷(methane)和乙烷(ethane)的区别
甲烷和乙烷的特性
结构:
Methane: The molecular formula of methane is CH4, and it is an example of a tetrahedral molecule with four equivalent C–H bonds (sigma bonds). Bond angle between H-C-H atoms is 109.50 and all the C-H bonds are equivalent, and it is equal to108.70 pm.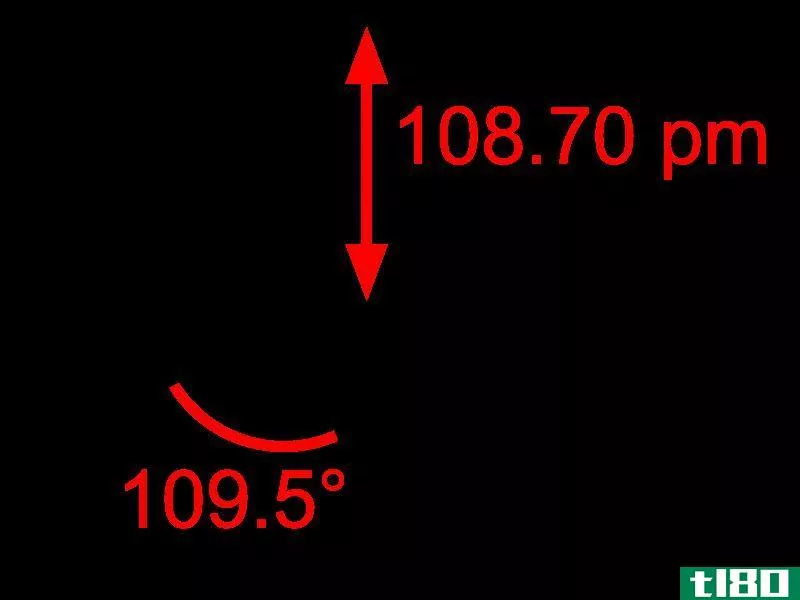
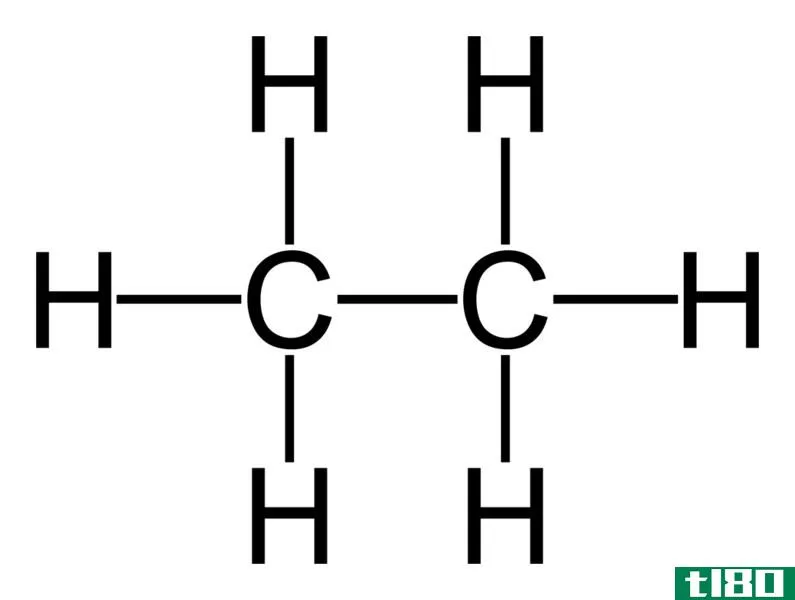
Ethane: The molecular formula of ethane is C2H6, and it is a saturated hydrocarbon since it does not contain multiple bonds.
化学性质:
甲烷:
稳定性:甲烷是一种化学性质非常稳定的分子,在正常条件下不会与KMnO4、K2Cr2O7、H2SO4或HNO3发生反应。
燃烧:在空气或氧气过量的情况下,甲烷燃烧时产生淡蓝色的不发光火焰,产生二氧化碳和水。它是一种高度放热的反应;因此,它被用作优良的燃料。在空气或氧气不足的情况下,它会部分燃烧成一氧化碳(CO)气体。
取代反应:甲烷与卤素发生取代反应。在这些反应中,一个或多个氢原子被等量的卤素原子取代,称为“卤化”,它在阳光下与氯(Cl)和溴(Br)反应。
与蒸汽的反应:当甲烷和蒸汽的混合物通过氧化铝表面上的加热(1000 K)镍时,它可以产生氢气。
热解:当甲烷被加热到1300 K左右时,它被分解成炭黑和氢气。
乙烷:
反应:乙烷气体(CH3CH3)在光的存在下与溴蒸气反应生成溴乙烷(CH3CH2Br)和溴化氢(HBr)。这是一种取代反应,乙烷中的氢原子被溴原子取代。
ch3ch3+br2=ch3ch2br+hbr
燃烧:乙烷完全燃烧产生1559.7kJ/mol(51.9kJ/g)的热量、二氧化碳和水。
2 C2H6+7 O2→4二氧化碳+6 H2O+3120千焦
它也可以在没有过量氧气的情况下发生,产生无定形碳和一氧化碳的混合物。
2 C2H6+3 O2→4 C+6 H2O+能量
2 C2H6+5 O2→4 CO+6 H2O+能量
2 C2H6+4 O2→2 C+2 CO+6 H2O+能量等。
定义:
取代反应:取代反应是指化合物中一个官能团被另一个官能团取代的化学反应。
使用:
甲烷:甲烷用于许多工业化学过程(作为燃料、天然气、液化天然气),并作为冷冻流体运输。
乙烷:乙烷用作发动机的燃料和极低温系统的制冷剂。它是用钢瓶在自身蒸汽压力下作为液化气运输的。
References: “Ethane”. Wikipedia. N.p., 2016. Web. 7 June 2016. Khanna, Bhishm. “What Are The Chemical Properties Of Methane ?”. Preservearticles.com. N.p., 2016. Web. 7 June 2016. “Methane | CH4 – Pubchem”. Pubchem.ncbi.nlm.nih.gov. N.p., 2016. Web. 7 June 2016. “Methane”. Wikipedia. N.p., 2016. Web. 7 June 2016. Image Courtesy: “Ball-and-stick model of methane molecule” by (Public Domain) via Comm*** Wikimedia “Ball-and-stick model of ethane molecule”y Ben Mills – Own work (Public Domain) via Comm*** Wikimedia “Methane” By Jynto – Own work, based on File:Methane-CRC-MW-dimensi***-2D.png, (Public Domain) via Comm*** Wikimedia “Ethane” (Public Domain) via Comm*** Wikimedia