分馏与简单蒸馏
蒸馏是一种物理分离方法,用于从混合物中分离化合物。它是基于混合物中成分的沸点。当混合物具有不同沸点的不同组分时,它们在加热时的不同时间蒸发。这一原理用于蒸馏技术。假设混合物中有两种物质A和B,A的沸点较高。在这种情况下,当沸腾时,A的蒸发速度比B慢,因此蒸汽中B的含量比A高,所以A和B在气相中的比例不同于在液体混合物中的比例。结论是,大部分挥发性物质将从原始混合物中分离出来,而挥发性较小的物质将保留在原始混合物中。
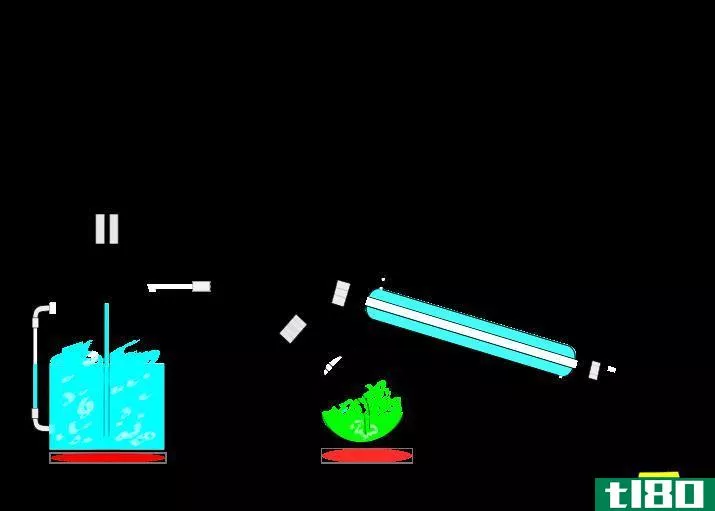
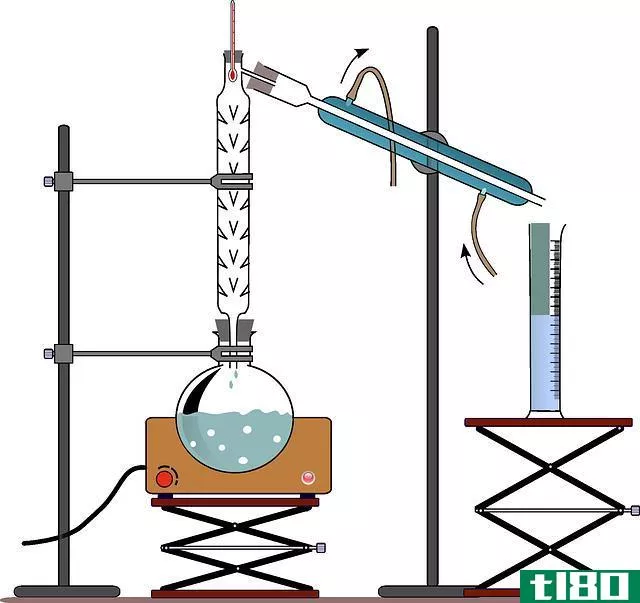
在实验室里,可以进行简单的蒸馏。准备仪器时,应将圆底烧瓶连接到柱上。塔的末端与冷凝器相连,冷水应该在冷凝器中循环,这样当蒸汽通过冷凝器时,它就被冷却了。水应该以与蒸汽相反的方向流动,这样可以获得最大的效率。冷凝器的端部开口与烧瓶相连。整个设备应进行空气密封,以便蒸汽在过程中不会逸出。可使用加热器向圆底烧瓶提供热量,该烧瓶含有要分离的混合物。加热时,蒸汽沿柱上升进入冷凝器。当它在冷凝器内流动时,它变冷并液化。这种液体被收集在保存在冷凝器末端的烧瓶中。
简单蒸馏
简单蒸馏是如上所述的蒸馏方法。在这种方法中,产生的蒸汽直接进入冷凝器,而不经过高柱。因此,冷凝发生得很快。然而,这种方法的缺点可能是产生纯度较低的馏出物。由于所有挥发性化合物在加热时都会蒸发,因此蒸汽中含有挥发性化合物的混合物。混合物中化合物的比例可以根据它们在原始混合物中的比例来确定。根据拉乌尔定律,混合物的成分将与给定温度和压力下的蒸汽成分相同。
如果我们想在简单蒸馏法中获得良好的分离效果,使用沸点变化很大的混合物是有益的。否则,混合物中的成分应该是非挥发性的(固体),除了我们需要分离的成分。在这种情况下,只有预期的成分会蒸发并完全分离出来。
分馏
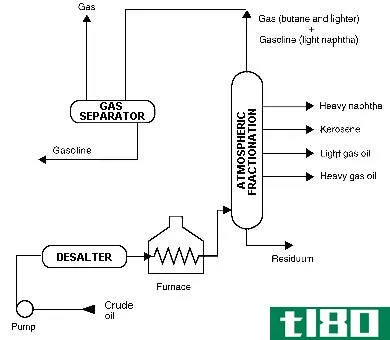
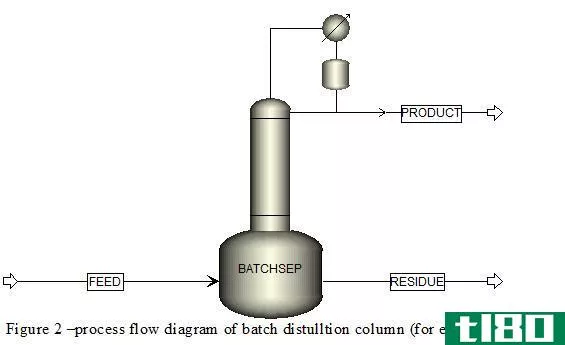
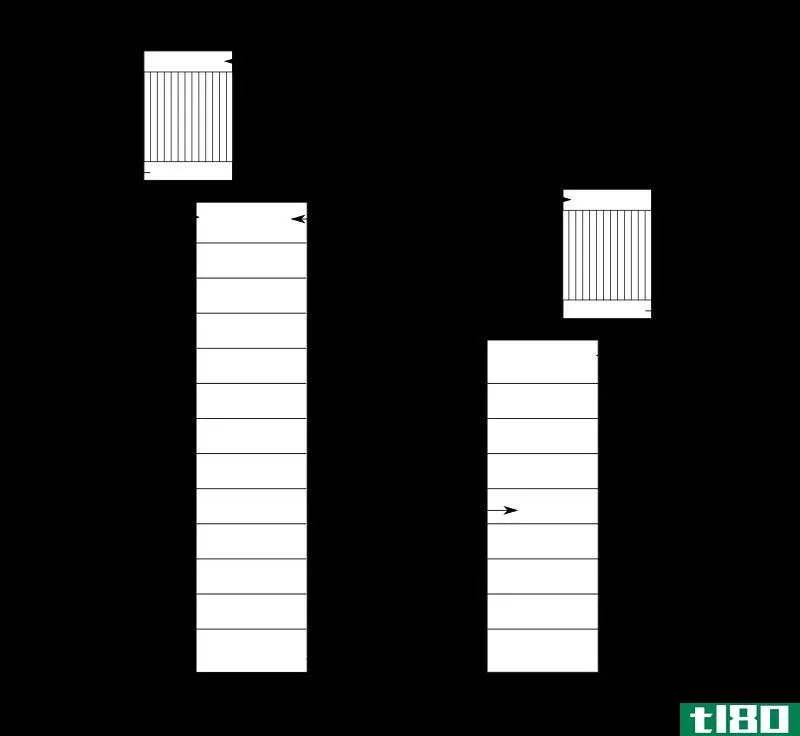
当混合物中的组分沸点较近时,可用分馏法分离。此方法使用小数列。在分馏塔的每一级,温度都是不同的,因此与该温度有关的组分将作为蒸汽留在该部分,而其他组分则冷凝回圆底烧瓶。
| 简单蒸馏和分馏有什么区别?•在分馏法中,与简单蒸馏法相比,使用分馏塔。•当混合物中的组分具有更接近的沸点时,使用分馏法。当它们的沸点相差很大时,可以采用简单蒸馏法。•拉乌尔定律在简单蒸馏法中可以忽略,但在分馏过程中,它被考虑在内。 |