硫酸与盐酸
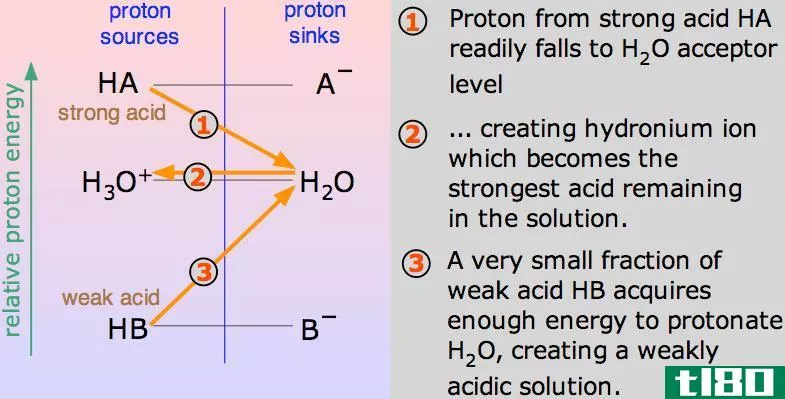
我们通常认为酸是质子供体。酸有酸味。酸橙汁和醋是我们在家里遇到的两种酸。它们与产生水的碱反应,并与金属反应生成氢气;因此,增加了金属腐蚀速率。根据酸分解和产生质子的能力,酸可以分为两类。强酸在溶液中完全电离产生质子。弱酸部分离解,产生更少的质子。Ka是酸分解常数。它表明了弱酸失去质子的能力。为了检查一种物质是否是酸,我们可以使用石蕊试纸或pH试纸等几种指示剂。在pH标度中,代表1-6种酸。一种pH值为1的酸被认为是非常强的,随着pH值的增加,酸度降低。此外,酸会把蓝色石蕊变成红色。所有酸根据其结构可分为有机酸和无机酸。硫酸和盐酸是常用的强无机酸。这些也被称为矿物酸,它们来自矿物来源。无机酸溶解在水中时会释放质子。
硫酸
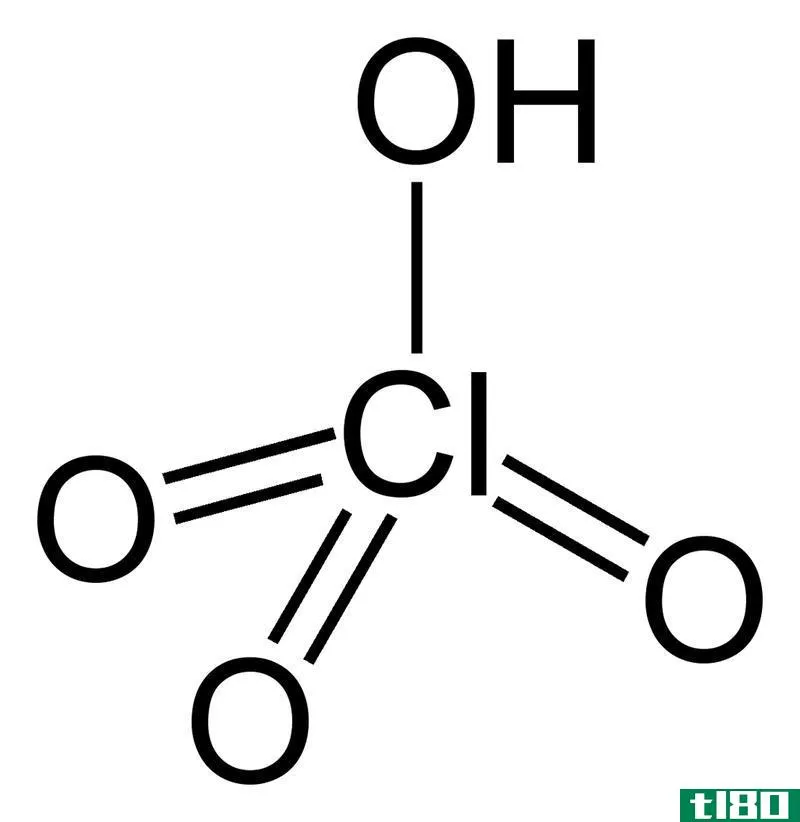
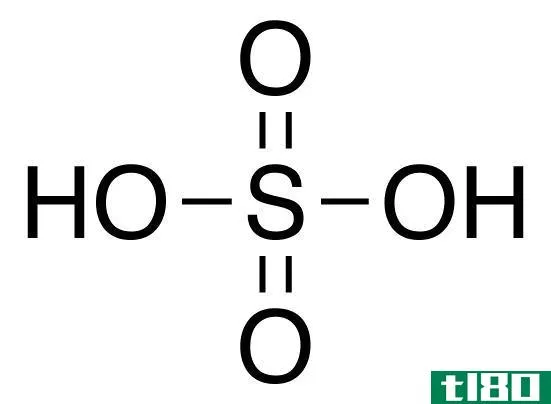
硫酸的分子式是硫酸。硫是分子的中心原子,与两个OH基团和两个氧原子(用双键)结合。分子呈四面体排列。硫酸是一种强腐蚀性的粘性液体。它是一种极性液体,介电常数大,易溶于水。硫酸的电离反应如下。
H2SO4→HSO4–+H+
HSO4–→SO4 2-+H+
硫酸是一种强大的质子供体;因此,在溶液中,它完全分解并产生两个质子。它是一种中等强度的氧化剂。由于硫处于+6氧化状态(这是硫的最高氧化状态),它可以还原到+4状态并起氧化剂的作用。在稀溶液中,硫酸可以形成两个板条,硫酸氢盐和硫酸盐。硫酸也可以作为脱水剂:因此,用于有机缩合反应,如酯化反应。
盐酸
盐酸,表示为HCl,是一种矿物酸,非常强,腐蚀性很强。这是一种无色,不可燃的液体。它是稳定的,但很容易与碱和金属反应。它有电离的能力,只提供一个质子。以下是盐酸在水介质中的解离反应。
HCl+H2O→H3O++Cl-
由于盐酸是一种强酸,它的酸离解常数很大。盐酸用于化肥、橡胶、纺织和染料**业。它是一种在实验室中广泛使用的酸,用于碱滴定,或提供酸性介质,或中和碱性溶液等。
| 硫酸和盐酸有什么区别?•HCl有一个氢原子和一个氯原子。硫酸是H2SO4,有两个氢原子、一个硫原子和四个氧原子。 |