原子半径与离子半径
我们可以定义圆或球的半径。在这种情况下,我们说半径是圆心到圆周上一点之间的距离。原子和离子也被认为具有类似于球的结构。因此,我们也可以为它们定义一个半径。在一般定义中,对于原子和离子,我们说半径是中心和边界之间的距离。
原子半径
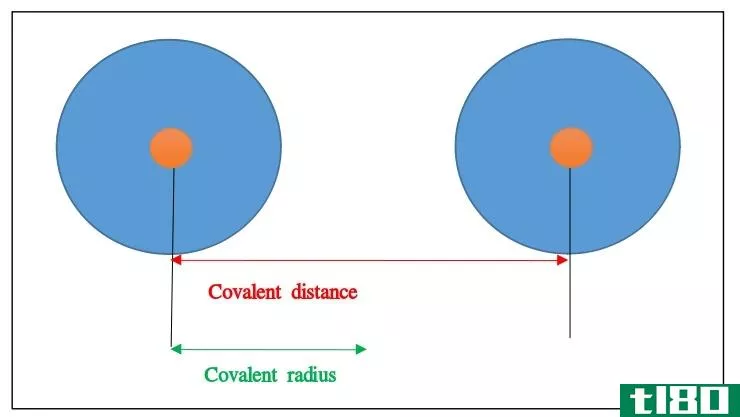
原子半径是原子核中心到电子云边界的距离。原子半径是埃级的。虽然我们定义了单个原子的原子半径,但是很难测量单个原子的半径。因此,通常取两个接触原子核之间的距离除以二,得到原子半径。根据两个原子之间的键合,半径可分为金属半径、共价半径、范德华半径等。原子半径随着周期表中某一列的下降而增大,因为新的电子层正在增加。原子半径从左到右连续减小(稀有气体除外)。
离子半径
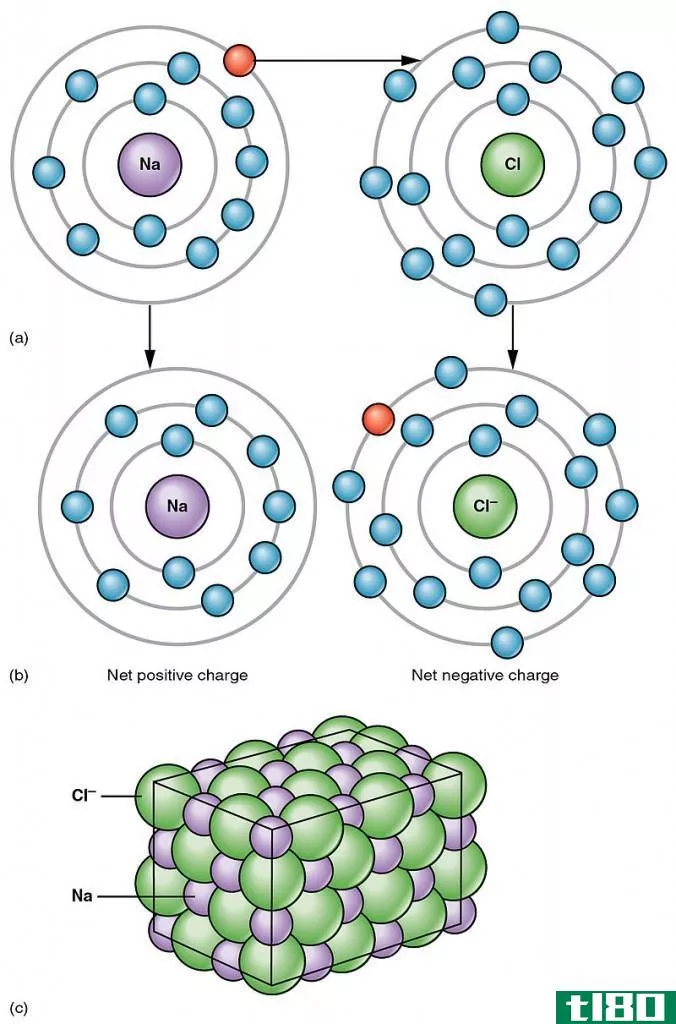
原子可以获得或失去电子,并分别形成负电荷或正电荷粒子。这些粒子叫做离子。当中性原子除去一个或多个电子时,就会形成带正电荷的阳离子。当中性原子吸收电子时,它们形成带负电荷的阴离子。离子半径是原子核中心到离子外缘的距离。然而,大多数离子不是单独存在的。它们要么与另一个反离子结合,要么与其他离子、原子或分子发生相互作用。因此,单个离子的离子半径在不同的环境中是不同的。因此,在比较离子半径时,应比较相似环境中的离子。元素周期表中的离子半径有变化趋势。当我们进入一个柱状结构时,附加的轨道被加到原子上;因此,相应的离子也有额外的电子。因此,从上到下,离子半径增大。当我们从左到右穿过一排时,有一种离子半径变化的特殊模式。例如,在第三排,钠、镁和铝分别生成+1、+2和+3阳离子。三者的离子半径逐渐减小。由于质子数大于电子数,原子核倾向于把电子越来越多地拉向中心,导致离子半径减小。然而,与阳离子半径相比,第三行中的阴离子具有更高的离子半径。从P3-开始,离子半径减小到S2-和Cl-。阴离子中离子半径大的原因可以通过在外轨道中加入电子来解释。
| 原子半径和离子半径有什么区别?•原子半径表示原子的大小。离子半径是一个离子大小的指示。•阳离子离子半径小于原子半径。阴离子半径大于原子半径。 |