关键区别-晶格能与水化能
晶格能和水化能是热力学中两个相关的术语。晶格能是晶格形成时释放的能量。水化能是晶格在水中溶解时释放的能量。晶格的形成和水合都会释放能量,因为这两个过程都涉及化学键(或化学相互作用)的形成。晶格能和水化能的关键区别在于晶格能是由无限分离的离子形成一摩尔晶格时释放的能量,而水化能是晶格在水中溶剂化分解成离子时释放的能量。
目录
1. 概述和主要区别
2. 什么是晶格能
3.什么是水化能
4. 晶格能与水化能的关系
5. 并列比较-晶格能与水化能的表格形式
6. 摘要
什么是晶格能(lattice energy)?
晶格能是化合物晶格中所含能量的量度,它等于组成离子从无穷远处**时释放的能量。换句话说,晶格能是由完全分离的离子形成晶体所需的能量。实验测量晶格能是非常困难的。因此,从理论上推导了它。
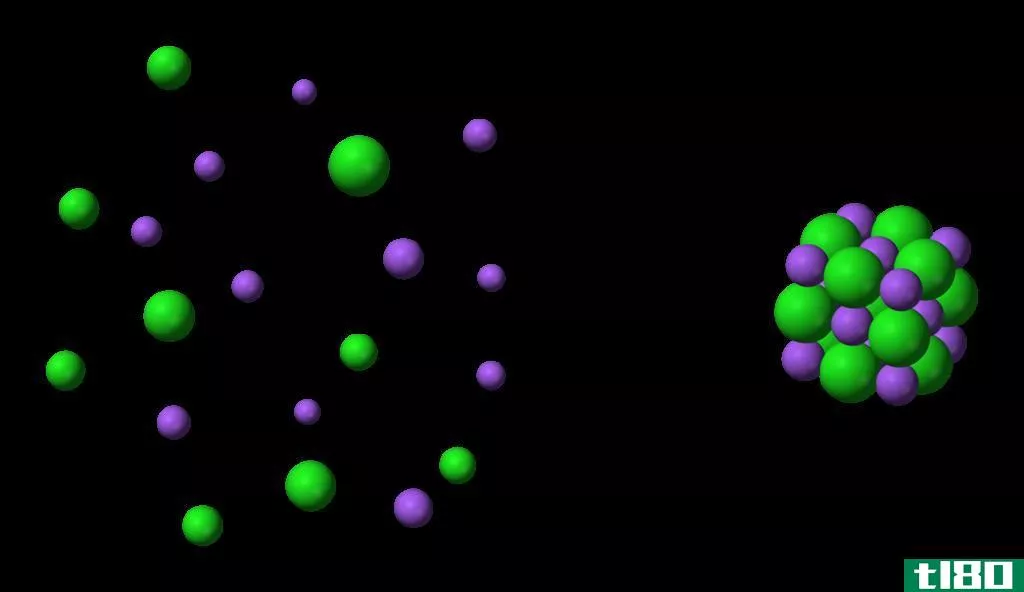
图01:晶格能
晶格能的值总是负值。这是因为晶格的形成涉及化学键的形成。化学键的形成是放热化学反应,释放能量。晶格能的理论值确定如下。
ΔGU=ΔGH–p.ΔVm
式中,ΔGU为摩尔晶格能,ΔGH摩尔晶格焓,ΔVm为每摩尔体积的变化。P是外部压力。因此,晶格能也可以定义为在外压p作用下所做的功。
什么是水化能(hydration energy)?
水化能(或水化焓)是指当一摩尔离子发生水化时释放的能量。水化是离子在水中溶解的一种特殊形式。离子可以是带正电荷或带负电荷的化学物质。当一种固体离子化合物溶于水时,该固体最外层的离子就会离开固体而溶解在水中。在那里,释放的离子被邻近的水分子覆盖。
离子化合物的水合作用包括分子内的相互作用。这些是离子-偶极相互作用。水化焓或水化能是当离子溶解在水中时释放的能量。因此,水化是一种放热反应。这是因为离子的溶解在离子和水分子之间产生了相互作用。相互作用的形成释放能量,因为水合作用使水溶液中的离子稳定。
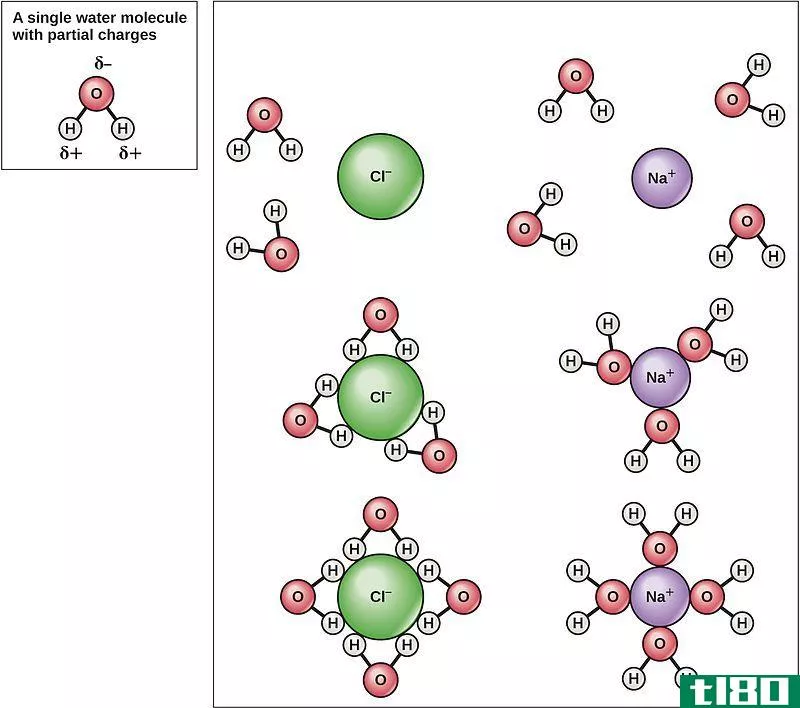
图02:Na+和Cl-离子的水合作用
水化能表示为Hhyd。当考虑不同离子的水化能时,水化能随离子粒径的增大而减小。这是因为,当离子尺寸增大时,离子的电子密度降低。然后离子和水分子之间的相互作用也会减少,导致水化能降低。
什么是晶格能与水化能的关系(the relati***hip between lattice energy and hydration energy)?
- 溶解能等于晶格能和水化能之和。这是因为,为了使晶格溶解在水中,晶格必须经历解离和水合作用。晶格中的离解能可以提供给晶格。这等于晶格能。
晶格能(lattice energy)和水化能(hydration energy)的区别
| 晶格能与水化能 | |
| 如果在晶格中释放出的能量等于晶格中离子的能量。 | 水合(或水合焓)是指当一摩尔离子水合时释放的能量。 |
| 能量 | |
| 晶格能是由无限分离的离子形成一摩尔晶格时释放的能量。 | 水化能是晶格在水溶液中溶解成离子时释放的能量。 |
| 过程 | |
| 晶格能与晶格的形成有关。 | 水化能与晶格的破坏有关。 |
总结 - 晶格能(lattice energy) vs. 水化能(hydration energy)
晶格能与晶格的形成有关,而水化能与晶格的破坏有关。晶格能和水化能的区别在于晶格能是由无限分离的离子形成一摩尔晶格时释放的能量,而水化能是晶格在水中溶剂化分解成离子时释放的能量。
引用
2018年2月1日,维基百科能源基金会。此处提供2.“晶格能量:玻恩哈伯循环”(Lattice Energy:The Born-Haber cycle),《化学文摘》,歌词,2017年2月15日。可在此处查阅
2.“晶格能量:玻恩哈伯循环”,《化学歌词》,歌词,2017年2月15日