关键区别-溶剂化能与晶格能
溶剂化能是溶质溶解在溶剂中时,其吉布斯能的变化。晶格能要么是离子在晶格形成过程中释放的能量,要么是分解晶格所需的能量。溶剂化能和晶格能的关键区别在于,溶剂化能给出溶质在溶剂中溶解时的焓变化,而晶格能给出晶格形成(或破裂)时的焓变化。
目录
1. 概述和主要区别
2. 什么是溶剂化能
3. 什么是晶格能
4. 并列比较-溶剂化能与晶格能的表格形式
5. 摘要
什么是溶剂化能(solvation energy)?
溶剂化能是离子或分子从真空(或气相)转移到溶剂时吉布斯能的变化。溶剂化是溶剂与溶质分子或离子之间的相互作用。溶质是溶解在溶剂中的化合物。有些溶质是由分子组成的,而有些则含有离子。
溶剂和溶质粒子之间的相互作用决定了溶质的许多性质。溶解度、反应性、颜色等在溶剂化过程中,溶质颗粒被溶剂分子包围形成溶剂化络合物。当参与溶剂化的溶剂是水时,这个过程称为水合作用。
在溶剂化过程中形成了不同类型的化学键和相互作用:氢键、离子偶极相互作用和范德华力。溶剂和溶质的互补性质决定了溶质在溶剂中的溶解度。例如,极性是决定溶质在溶剂中溶解度的一个主要因素。极性溶质在极性溶剂中溶解良好。非极性溶质在非极性溶剂中溶解良好。但极性溶质在非极性溶剂中的溶解度很差(反之亦然)。

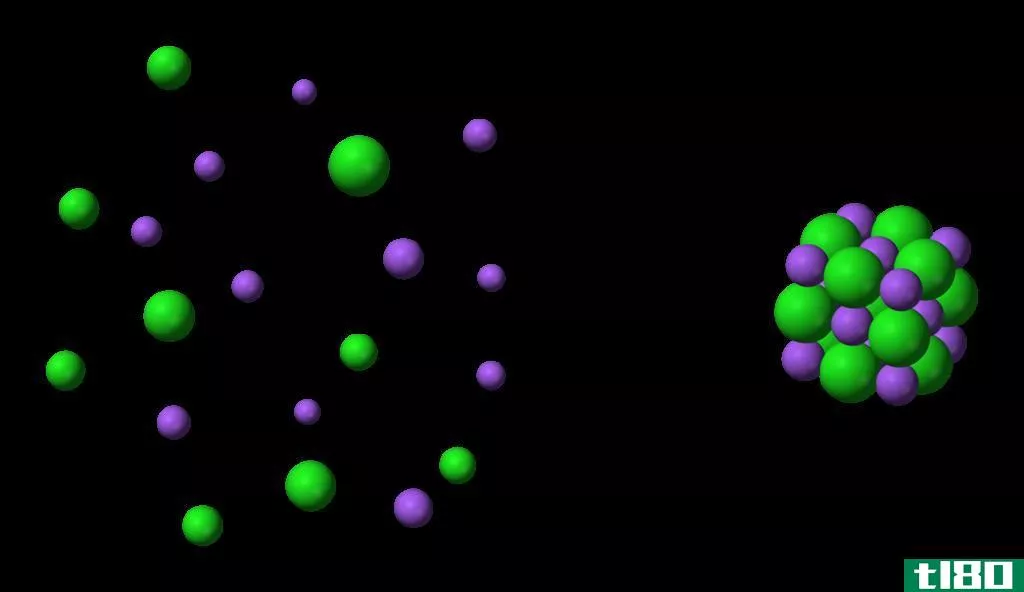
图01:钠离子在水中的溶剂化
在热力学方面,只有当最终溶液的吉布斯能低于溶剂和溶质的吉布斯能时,溶剂化才是可能的(自发的)。因此,Gibbs自由能应为负值(溶液形成后体系的Gibbs自由能应降低)。溶剂化包括不同的步骤和不同的能量。
- Formation of a cavity of solvent to make space for solutes. This is thermodynamically unfavourable because when the interacti*** between solvent molecule are decreased, and the entropy is decreased.
- Separation of the solute particle from the bulk is also thermodynamically unfavourable. That is because the solute-solute interacti*** are decreased.
- The solvent-solute interacti*** take place when solute enters the solvent cavity is thermodynamically favourable.
溶剂化能也称为溶剂化焓。这有助于解释某些晶格在溶剂中的溶解,而有些晶格则不溶解。溶液的焓变是溶质从本体中释放出来和溶质与溶剂结合的能量之差。如果一个离子的溶液焓变为负值,则表明该离子更有可能溶解在该溶剂中。高正值表示离子不太容易溶解。
什么是晶格能(lattice energy)?
晶格能是化合物晶格中所含能量的量度,等于组成离子从无穷远处**时释放的能量。化合物的晶格能也可以定义为将离子固体分解成气态原子所需的能量。
离子固体是非常稳定的化合物,由于离子分子的形成焓以及固体结构的晶格能的稳定性。但是晶格能不能用实验测量。因此,用Born-Haber循环来确定离子固体的晶格能。在绘制一个Born-Haber循环之前,需要理解几个术语。
- Ionization energy – The amount of energy required to remove an electron from a neutral atom in the gaseous
- Electron affinity – The amount of energy that is released when an electron is added to a neutral atom in the gaseous
- Dissociation energy – The amount of energy required to break apart a compound into atoms or i***.
- Sublimation energy – The amount of energy required to convert a solid into its vapour
- The heat of formation – The change in energy when a compound is formed from its elements.
- Hess’s law – A law which states that the overall change in the energy of a certain process can be determined by breaking the process into different steps.
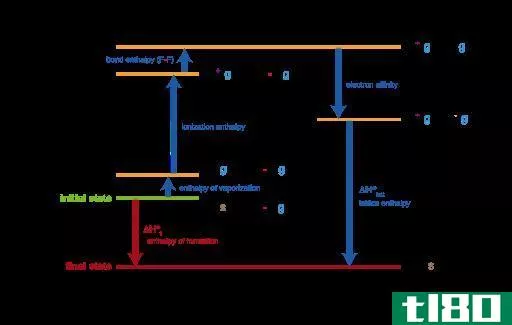
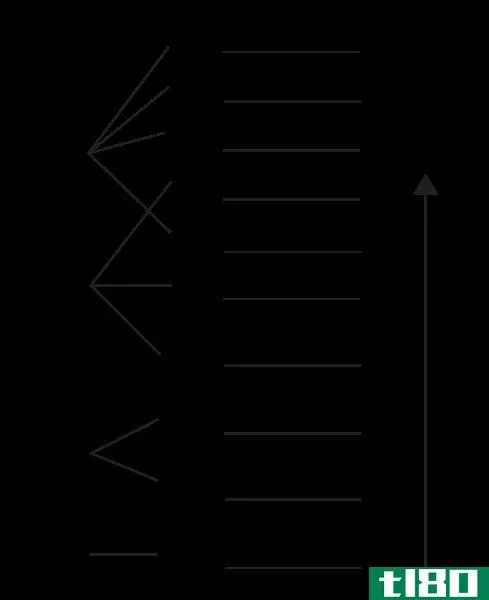
图02:氟化锂(LiF)形成的Born-Haber循环
Born-Haber循环可由以下方程给出。
生成热=原子化热+离解能+电离能之和+电子亲和力之和+晶格能
然后通过重新排列这个方程,可以得到化合物的晶格能,如下所示。
晶格能=生成热–{原子化热+离解能+电离能之和+电子亲和力之和}
溶剂化能(solvation energy)和晶格能(lattice energy)的区别
| 溶剂化能与晶格能 | |
| 溶剂化能是离子或分子从真空(或气相)转移到溶剂时吉布斯能的变化。 | 晶格能是化合物晶格中所含能量的一种测量,等于组成离子从无穷大中**在一起时释放的能量。 |
| 原则 | |
| 溶剂化能是指溶质在溶剂中溶解时焓的变化。 | 晶格能量给出了晶格形成(或破裂)时焓的变化。 |
总结 - 溶剂化能(solvation energy) vs. 晶格能(lattice energy)
溶剂化能是溶质在溶剂中溶剂化时系统焓的变化。晶格能是晶格形成过程中释放的能量,或是分解晶格所需的能量。溶剂化能和晶格能的区别在于,溶剂化能给出溶质在溶剂中溶解时的焓的变化,而晶格能给出晶格形成(或分解)时焓的变化。
引用
1.“晶格能”化学普渡大学。可在这里查阅2。国际纯与应用化学联合会。“溶剂化能源”,IUPAC金典-溶剂化能源。可在此处查阅3。“溶剂化”,维基百科,维基媒体基金会,2018年3月5日。可在此处查阅
2.国际纯与应用化学联合会。“溶剂化能”,IUPAC金典-溶剂化能
3.“溶剂化”,维基百科,维基媒体基金会,2018年3月5日