强酸定义和示例
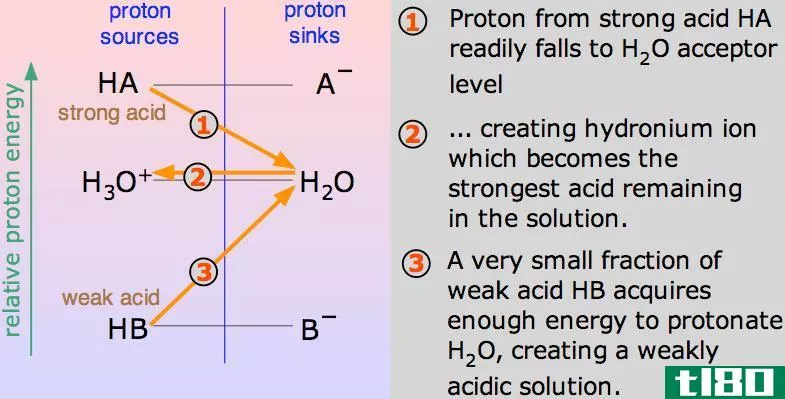
强酸是在水溶液中完全解离或电离的酸。它是一种化学物质,具有很高的失去质子H+的能力。在水中,强酸会失去一个质子,该质子被水捕获,形成氢离子:


HA(aq)+H2O→ H3O+(aq)+A−(aq)
二元酸和多元酸可能损失不止一个质子,但“强酸”pKa值和反应仅指第一个质子的损失。
强酸具有较小的对数常数(pKa)和较大的酸离解常数(Ka)。
大多数强酸具有腐蚀性,但一些超强酸则不具有腐蚀性。相比之下,一些弱酸(如氢氟酸)具有很强的腐蚀性。
随着酸浓度的增加,解离能力减弱。在正常条件下,强酸在水中完全解离,但极浓的溶液则不解离。
强酸的例子
虽然弱酸很多,但强酸很少。常见的强酸包括:
- 盐酸(盐酸)
- H2SO4(硫酸)
- 硝酸
- HBr(氢溴酸)
- HClO4(高氯酸)
- HI(氢碘酸)
- 对甲苯磺酸(一种有机可溶性强酸)
- 甲烷磺酸(一种液态有机强酸)
以下酸在水中几乎完全解离,因此通常被认为是强酸,尽管它们的酸性并不比氢离子H3O+强:
- 硝酸
- HClO3(氯酸)
一些化学家认为氢离子、溴酸、周期酸、过溴酸和周期酸是强酸。
如果将提供质子的能力用作酸强度的主要标准,则强酸(从最强到最弱)将为:
- H[SbF6](氟锑酸)
- FSO3HSbF5(神奇酸)
- H(CHB11Cl11)(碳硼烷超强酸)
- FSO3H(氟硫酸)
- CF3SO3H(三氟磺酸)
这些是“超强酸”,定义为比100%硫酸酸性更强的酸。超强酸使水永久质子化。
决定酸强度的因素
你可能想知道为什么强酸能很好地离解,或者为什么某些弱酸不能完全离解。有几个因素起作用:
- 原子半径:随着原子半径的增大,酸度也随之增大。例如,HI是一种比HCl强的酸(碘原子比氯原子大)。
- 电负性:在周期表的同一周期内,共轭碱的电负性越强(a-),其酸性越强。
- 电荷:原子上的电荷越正,其酸度越高。换句话说,从中性物质中提取质子比从带负电荷的物质中提取质子更容易。
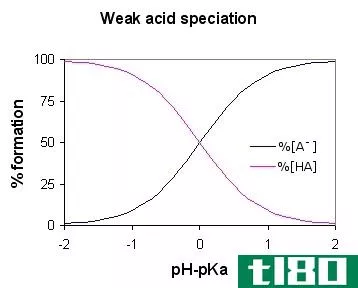
- 平衡:当酸离解时,与其共轭碱达到平衡。在强酸的情况下,平衡非常有利于产物,或者是在化学方程式的右边。强酸的共轭碱作为碱比水弱得多。
- 溶剂:在大多数应用中,强酸与水作为溶剂有关。然而,酸度和碱度在非水溶剂中有意义。例如,在液氨中,乙酸完全电离,可以认为是强酸,即使它在水中是弱酸。
- 发表于 2021-10-20 16:00
- 阅读 ( 267 )
- 分类:法律
你可能感兴趣的文章
浓酸(concentrated acid)和强酸(strong acid)的区别
关键区别-浓酸与强酸 酸是一种化合物,它可以通过酸分子的离子化将氢离子(质子)释放到其所在的介质中。酸有两种主要类型,即强酸和弱酸。强酸是在水溶液中完全离解,释放H+离子的酸。强碱是在水溶液中完全离解形...
- 发布于 2020-10-19 14:49
- 阅读 ( 380 )
虚弱的(weak)和强酸(strong acid)的区别
弱酸和强酸的关键区别在于弱酸在水中部分电离,而强酸则完全电离。 酸的强度是它在水溶液中与水发生反应时电离或提供氢离子的能力。酸离子化得越多,它就越强,氢离子的生成越少,说明酸是弱酸。这就是强酸和弱酸...
- 发布于 2020-10-23 09:57
- 阅读 ( 341 )
坚强的(strong)和弱酸(weak acid)的区别
...酸释放出的质子的数量实际上决定了酸的强度——无论是强酸还是弱酸。为了了解酸的强度,我们需要比较它们向类似的碱(主要是水)提供质子的倾向。强度由一个称为pKA的数字表示。 什么是强酸(a strong acid)? 如果一种...
- 发布于 2021-06-25 16:37
- 阅读 ( 410 )
坚强的(strong)和弱酸(weak acids)的区别
...反应中提供质子或接受电子对的分子或其他物质。酸分为强酸和弱酸两类。强酸和弱酸的主要区别在于强酸在水溶液中完全解离,而弱酸在水溶液中部分解离。 覆盖的关键领域 1.什么是强酸-定义、性质、示例2。什么是弱酸-定...
- 发布于 2021-06-28 19:21
- 阅读 ( 1032 )
盐酸(hydrochloric acid)和硫酸(sulfuric acid)的区别
... 酸是能够将质子或H+离子提供给水溶液的分子。酸主要有强酸和弱酸两种。盐酸和硫酸是两种强酸。盐酸和硫酸的主要区别在于盐酸是一元的,而硫酸是二元的。 覆盖的关键领域 1.什么是盐酸-定义、性质2。什么是硫酸-定义、...
- 发布于 2021-06-28 19:31
- 阅读 ( 674 )
一元二元酸(monobasic dibasic)和三元酸(tribasic acids)的区别
...与碱反应形成盐和水的化学物质。酸有两种主要类型,即强酸和弱酸。酸也可分为三类:一元酸、二元酸和三元酸。酸是按照质子的数量来分组的,以便与碱反应。二元酸和三元酸统称为多元酸。这些一元酸和多元酸可以是强酸...
- 发布于 2021-06-29 12:53
- 阅读 ( 611 )
坚强的(strong)和弱电解质(weak electrolytes)的区别
...ong Acids and Strong Bases are Strong Electrolytes 常见的强电解质有强酸、强碱和离子盐。然而,有些电解质不完全溶于水,但被认为是强电解质。这是因为溶解的量被完全电离成它的离子。 例如,强酸如HCl、HNO3是强电解质。这些被完全...
- 发布于 2021-06-29 14:13
- 阅读 ( 285 )
矿物酸(mineral acids)和有机酸(organic acids)的区别
...与碱反应形成盐和水的化学物质。酸有两种主要类型,即强酸和弱酸。根据化学成分的不同,酸也可分为矿物酸和有机酸。矿物酸和有机酸的主要区别在于,矿物酸是由不同化学元素组合组成的无机化合物,而有机酸是基本上由...
- 发布于 2021-06-29 21:02
- 阅读 ( 512 )
酸的(acid)和碱性(alkaline)的区别
...的共轭碱和H+离子。根据它们的离解强度,有两种酸。 强酸 弱酸 强酸是能完全分解成离子的化合物。弱酸是部分分解成离子的化合物。因此,弱酸在水溶液中与其共轭碱和H+离子处于平衡状态。 酸的pH值总是低于7。pH值7是溶...
- 发布于 2021-07-02 08:12
- 阅读 ( 870 )
化学中ph的定义与方程
...“中性”,因为H3O+的浓度等于OH的浓度− 在纯净水中。强酸的pH值可能为负值,而强碱的pH值可能大于14。 ph方程 1909年,丹麦生物化学家Søren Peter Lauritz Sørensen提出了计算pH值的方程式: pH=-log[H+] 其中log是以10为基数的对...
- 发布于 2021-09-07 00:16
- 阅读 ( 517 )