均相平衡与非均相平衡的关键区别在于,在均相平衡中,反应物和产物处于物质的同一相,而在非均相平衡中,反应物和产物处于不同的相。
平衡是反应物和产物的浓度保持恒定的状态。平衡分为均相平衡和非均相平衡两种类型。这两种类型因反应物和平衡产物的物相不同而不同。
目录
1. 概述和主要区别
2. 什么是齐次平衡
3. 什么是非均匀平衡
4. 并列比较-表格形式的均质平衡与非均质平衡
5. 摘要
什么是均相平衡(homogeneous equilibrium)?
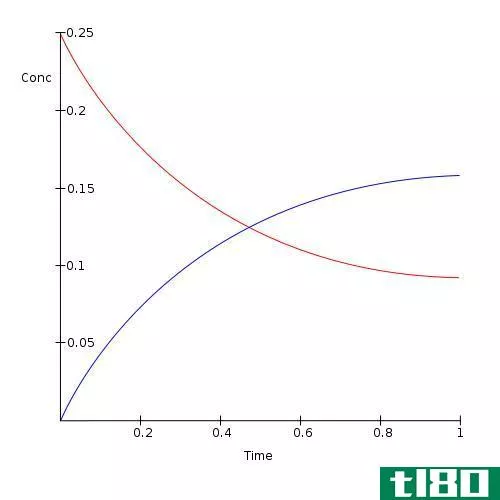
均相平衡是指反应物和产物处于物质同一相的状态。通常,反应物和产物在一个溶液中。我们称这种反应混合物为均相混合物。这种混合物中的化学物质可以是分子、离子,也可以是分子和离子的组合。此外,这类反应的平衡常数表达式包括所有反应物和产物的浓度。例如,二氧化硫气体和氧气混合产生三氧化硫气体,所有反应物和产物都处于气相。则反应和平衡常数(K)如下:
2SO2(g)+O2(g)⇌2SO3(g)
K=[SO3(g)]2/[SO2(g)]2[O2(g)]

什么是非均相平衡(heterogeneous equilibrium)?
非均相平衡是反应物和产物处于不同相的状态。在那里,相可以是固态、液态和气态的任何组合。然而,与均相平衡不同,在计算非均相平衡的平衡常数时,我们必须排除固体和纯液体的浓度。例如,将固态碳与氧气混合,就产生了一氧化碳气体。则反应和平衡常数(K)如下:
氧气(g)+2C(s)⇌2CO(g)
K=[CO(g)]2/[O2(g)]
同种类的(homogeneous)和非均相平衡(heterogeneous equilibrium)的区别
平衡是反应物和产物的浓度保持恒定的状态。平衡分为均相平衡和非均相平衡两种类型。均相平衡与非均相平衡的关键区别在于,在均相平衡中,反应物和产物处于物质的同一相,而在非均相平衡中,反应物和产物处于不同的相。
此外,在确定均相平衡的平衡常数时,我们必须包括所有反应物和产物的浓度;然而,在确定非均相平衡时,我们必须排除固体和纯液体的浓度,并且需要使用其他反应物和产物的浓度。例如,2SO2(g)+O2(g)⇌2SO3(g)是均相平衡,O2(g)+2C(s)⇌2CO(g)是非均相平衡的示例。
下面的信息图表列出了均质平衡和非均质平衡之间的差异。
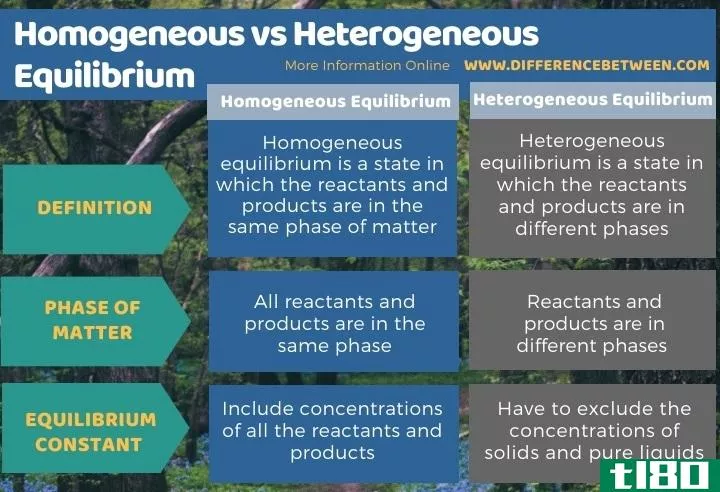
总结 - 同种类的(homogeneous) vs. 非均相平衡(heterogeneous equilibrium)
平衡是反应物和产物的浓度保持恒定的状态。平衡分为均相平衡和非均相平衡两种类型。均相平衡与非均相平衡的关键区别在于,在均相平衡中,反应物和产物处于物质的同一相,而在非均相平衡中,反应物和产物处于不同的相。此外,均相平衡的平衡常数包括所有反应物和产物的浓度,而非均相平衡的平衡常数必须排除固体和纯液体的浓度。
引用
1.“什么是均相平衡反应和非均相平衡反应”。学习网, 学习网,可在这里查阅。2.“15.4:异质平衡。”化学图书馆,图书馆,2019年9月18日,可在这里查阅。“均相与非均相溶液平衡”《无限生物学》。流明,这里有。
2.“15.4:多相平衡”,《化学图书馆》,图书馆,2019年9月18日,
三。“均相与非均相溶液平衡”《无限生物学》。流明,