化学平衡和动态平衡的关键区别在于,化学平衡描述的是反应物和产物的浓度不发生任何变化的状态,而动态平衡描述的是反应物和产物的比率不发生变化的状态,但是物质在化学物质之间的移动速度是相等的。
当一个或多个反应物转化为产物时,它们可能经历不同的修饰和能量变化。反应物中的化学键正在断裂,新的键正在形成,生成的产物与反应物完全不同。我们把这种化学修饰称为化学反应。热力学是研究能量转换的学科,它与反应中的能量和平衡位置有关。
目录
1. 概述和主要区别
2. 什么是化学平衡
3. 什么是动态平衡
4. 并列比较-化学平衡与动态平衡的表格形式
6. 摘要
什么是化学平衡(chemical equilibrium)?
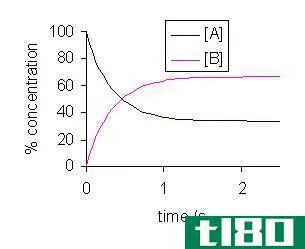
化学平衡是指反应物和产物的浓度都不随时间变化的状态。有些反应是可逆的,有些反应是不可逆的。在反应中,反应物转化为产物。在某些反应中,反应物又从产物中生成。因此,这种反应是可逆的。
在不可逆反应中,一旦反应物转化为产物,它们就不再从产物中再生。在可逆反应中,当反应物生成时,我们称之为正向反应;当产物变成反应物时,我们称之为反向反应。
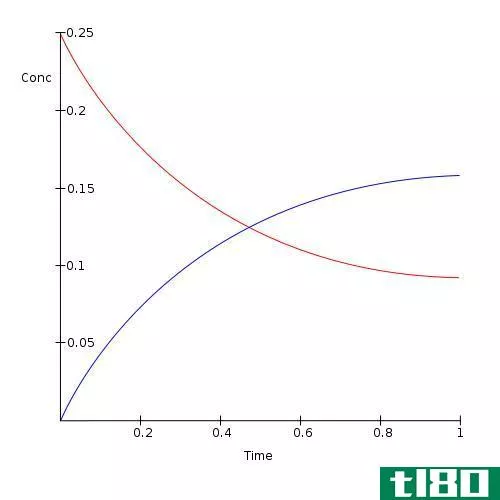
图01:化学平衡后,反应物(红色)减少,产物(蓝色)增加
反应性质
当正向和反向反应速率相等时,反应处于平衡状态。因此,在一段时间内,反应物和产物的量没有变化。可逆反应总是趋向于平衡并保持平衡。当体系处于平衡状态时,产物和反应物的量不一定相等。反应物的数量可能比产物多,反之亦然。平衡方程的唯一要求是随着时间的推移,两者的量都保持恒定。对于处于平衡状态的反应,我们可以定义一个平衡常数,其中它等于产物浓度与反应浓度之比。
K=[产物]n/[反应物]m
式中,n和m是产物和反应物的化学计量系数。对于平衡反应,如果正向反应是放热的,那么反向反应是吸热的,反之亦然。通常情况下,所有其他的正向和反向反应参数都是这样相反的。因此,如果我们想促进任何一个反应,我们只需调整参数来促进反应。
什么是动态平衡(dynamic equilibrium)?
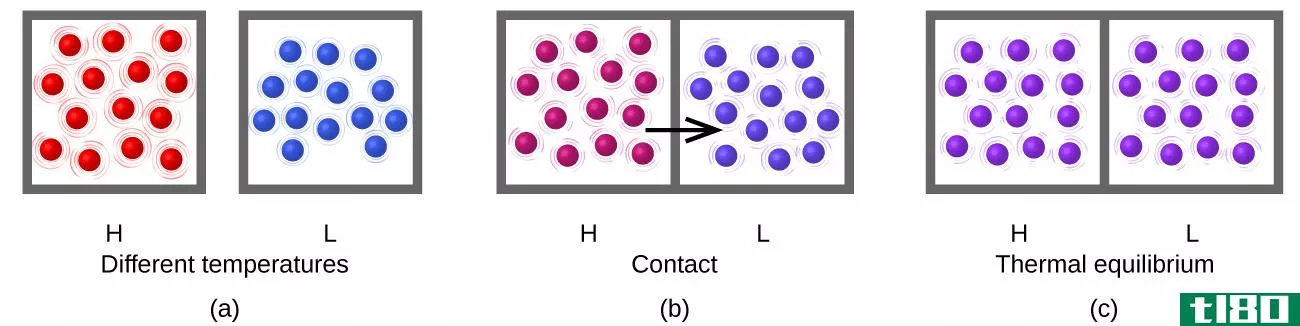
动态平衡也是一种平衡,其中产物和反应物的数量不随时间变化。然而,在动态平衡中,说量不变并不意味着反应已经停止。相反,反应是以保持数量不变的方式进行的(净变化为零)。
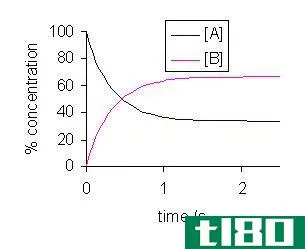
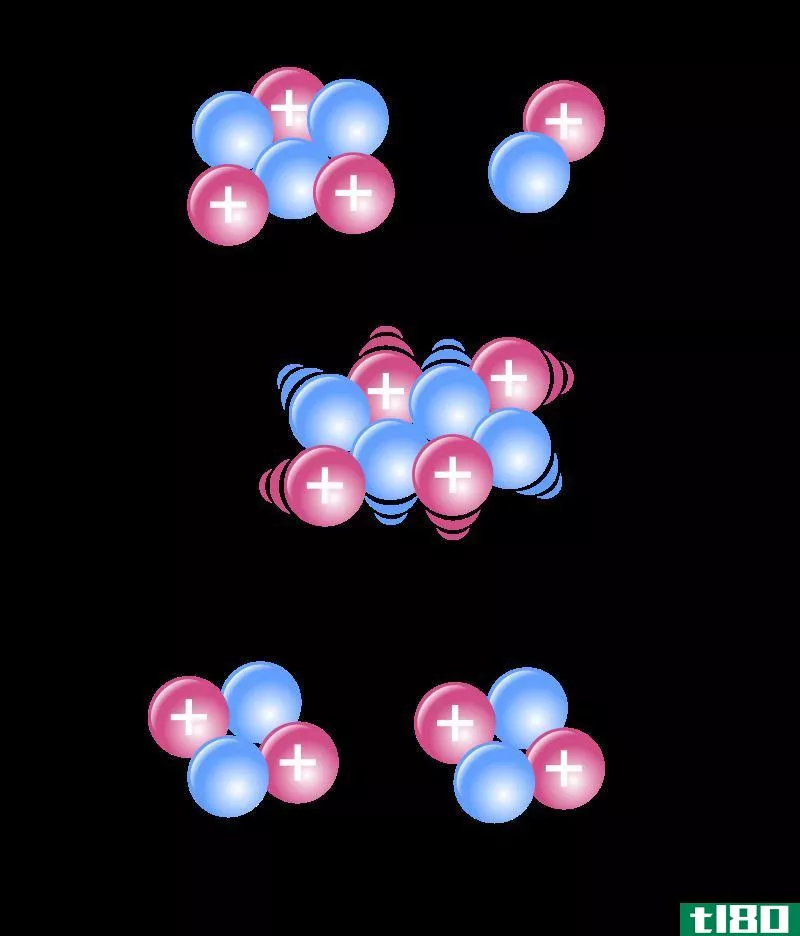
图02:动态平衡中前后反应的变化
简单地说,“动态平衡”一词意味着反应是可逆的和持续的。为了实现动态平衡,系统应该是一个封闭的系统,这样就不会有能量或物质从系统中逸出。
化学平衡(chemical equilibrium)和动态平衡(dynamic equilibrium)的区别
动态平衡是一种化学平衡。化学平衡和动态平衡的关键区别在于,化学平衡描述的是反应物和产物的浓度不发生任何变化的状态,而动态平衡描述的是反应物和产物的比率没有变化,但物质在化学物质之间移动的状态以同样的速度。
此外,在动态平衡中,反应继续进行,但由于正向反应和反向反应的速率相同,反应物和产物的数量保持不变。在化学平衡中,由于反应停止,产物和反应物的量保持不变。这也是化学平衡和动态平衡的区别。
以下关于化学平衡和动态平衡之间差异的信息图提供了关于这些差异的更多信息。

总结 - 化学平衡(chemical equilibrium) vs. 动态平衡(dynamic equilibrium)
平衡是一个系统没有净变化的状态。当反应停止时,化学平衡得到这种状态,而当正向和反向反应速率相等时,动态平衡得到这种状态。化学平衡和动态平衡的关键区别在于,化学平衡描述的是反应物和产物的浓度不发生任何变化的状态,而动态平衡描述的是反应物和产物的比例不发生变化的状态,但是物质在化学物质之间的移动速度是相等的。
引用
1“化学平衡-平衡的类型、原理和定律。”Toppr Bytes,Toppr.com网站,2018年3月16日。此处提供“动态平衡”,维基百科,维基媒体基金会,2018年12月17日。此处提供
“动态平衡”,维基百科,维基媒体基金会,2018年12月17日。