如何计算化学中的键序(calculate bond order in chemistry)
方法1 方法1之3:快速寻找债券订单
- 1知道公式。在分子轨道理论中,键序被定义为成键和反键电子数之差的一半。键序=[(成键分子的电子数)-(反键分子的电子数)]/2。
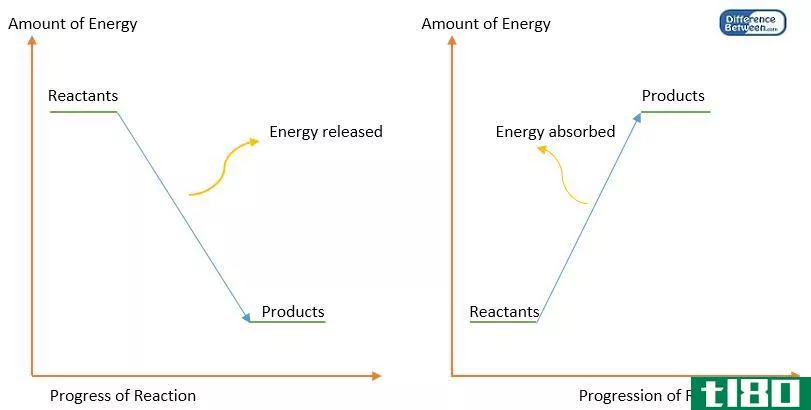
- 2知道,键序越高,分子就越稳定。每个进入成键分子轨道的电子将有助于稳定新分子。每个进入反键分子轨道的电子都会破坏新分子的稳定性。注意新的能量状态是分子的键序。如果键序为零,分子就不能形成。较高的键序表明新分子的稳定性更高。
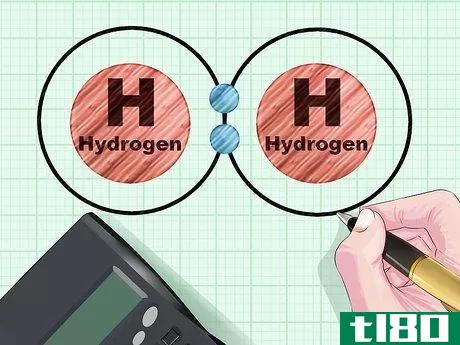
- 3考虑到一个简单的例子。氢原子的s壳里有一个电子,而s壳能够容纳两个电子。当两个氢原子结合在一起时,每个氢原子都完成了另一个氢原子的s壳。形成了两个成键的轨道。没有电子被迫移动到下一个更高的轨道,即p壳--所以没有形成反键轨道。因此,成键顺序是(2-0)/2{displaystyle(2-0)/2},等于1。这就形成了常见的分子H2:氢气。

方法2 方法2 of 3:可视化的基本债券顺序
- 1一目了然地确定键序。单一共价键的键序为1;双重共价键的键序为2;三重共价键的键序为3--以此类推。在其最基本的形式中,键序是将两个原子结合在一起的成键电子对的数量。要想更深入地了解,请查看周期表,看看你有什么样的键。
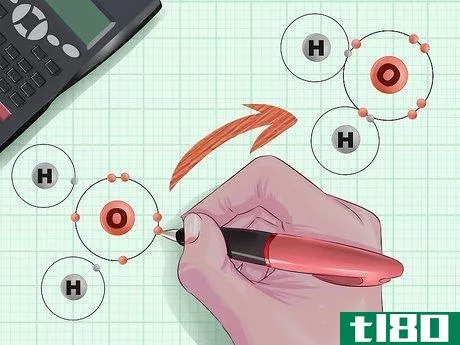
- 2考虑一下原子是如何组合成分子的。在任何给定的分子中,各组成原子都由成对的电子结合在一起。这些电子在 "轨道 "中围绕原子核旋转,每个 "轨道 "只能容纳两个电子。如果一个轨道不 "满",即它只容纳一个电子,或没有电子,那么未配对的电子可以与另一个原子上的相应自由电子结合。电子的收集在不断扩大的轨道壳中继续进行,因为大原子比小原子有更多的电子。
- 3D绘制路易斯点结构。这是一种方便的方法,可以直观地看到分子中的原子是如何相互结合的。以字母形式画出原子(例如,H代表氢,Cl代表氯)。用线条来说明它们之间的结合(例如:-代表单键,=代表双键,≡代表三键)。将未结合的电子和电子对标记为点(例如:C:)。一旦你画出了你的刘易斯点阵结构,就数一下键的数量:这就是键序。二原子氮的刘易斯点阵结构是N≡N。每个氮原子都有一个电子对和三个未结合的电子。当两个氮原子相遇时,它们的六个未结合的电子就会交织成一个强大的三价键。

方法3方法3:计算轨道理论的键序
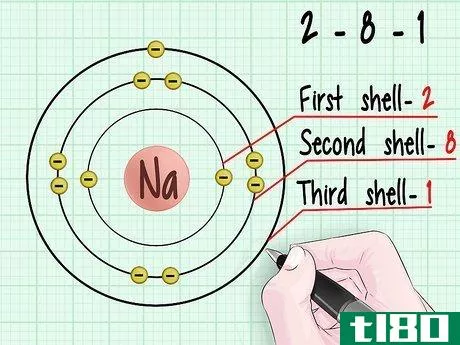
- 1请看电子轨道壳的示意图。请注意,每个壳都离原子核越来越远。根据熵的特性,能量总是寻求可能的最低秩序状态。电子将寻求填充可用的最低轨道壳。
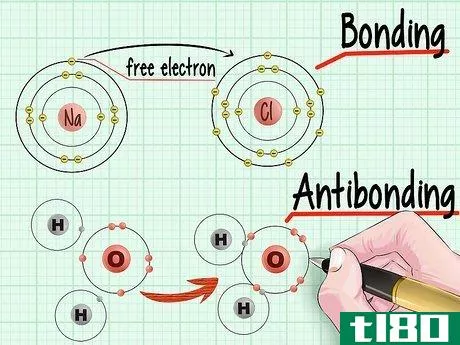
- 2知道成键轨道和反成键轨道的区别。当两个原子走到一起形成一个分子时,它们寻求利用对方的电子来填补电子轨道壳中可能的最低状态。粘合电子基本上是粘在一起并落入最低状态的电子。反键电子是 "自由 "或无键的电子,它们被推到更高的轨道状态。粘合电子。通过注意每个原子的轨道壳有多满,你可以确定有多少处于较高能量状态的电子能够填充相应原子的更稳定的低能量状态的外壳。这些 "填充电子 "被称为成键电子。反成键电子。当两个原子试图通过共享电子形成一个分子时,一些电子实际上将被驱赶到更高能量状态的轨道壳,因为低能量状态的轨道壳被填满了。这些电子被称为反键合电子。
- 发表于 2022-03-11 13:23
- 阅读 ( 382 )
- 分类:教育
你可能感兴趣的文章
键能(bond energy)和键焓(bond enthalpy)的区别
...的能量。它测量化学键的强度。所以也叫粘结强度。键能计算为气相化学物质在298K下的键离解能的平均值。键能和键焓这两个词之间没有很大的区别,但键能用“E”表示,而键焓用“H”表示。 目录 1. 概述和主要区别 2. 什么是...
- 发布于 2020-09-24 09:39
- 阅读 ( 882 )
多重性(multiplicity)和债券定单(bond order)的区别
...键序等于键电子数除以2(化学键每个键有两个电子)。计算特定分子中键级的方程如下: 键序=(成键电子数-反键电子数)/2 根据上面的方程,如果键级为零,则两个原子之间没有键合。例如,二氮分子的键级是3。此外,等电...
- 发布于 2020-10-13 16:56
- 阅读 ( 455 )
定性的(qualitative)和化学定量分析(quantitative analysis in chemistry)的区别
主要区别——化学中的定性分析与定量分析 化学中的定性和定量分析是化学中用于定性和定量测定样品化学成分的分析技术的主要类型。化学中定性分析和定量分析的关键区别在于,化学中的定性分析给出了样品中不同化学...
- 发布于 2020-10-19 08:40
- 阅读 ( 486 )
配价(valency)和价电子(valence electrons)的区别
...着非常密切的联系,但两者之间还是有细微的差别价态在化学中的文学意义是与容量有关的。用化学术语来说,元素的价态是它能形成的键的数目。价电子就是可以参与成键的电子。因此,价电子和价电子之间的主要区别在于,...
- 发布于 2021-06-27 10:49
- 阅读 ( 603 )
单双(single double)和三重债券(triple bonds)的区别
主要区别单(main difference single) vs. 双重的(double) 化学键通过建立两个原子的电子和原子核之间的力,将分子中的原子固定在一起。化学反应是由建立或打破化学键来控制的。键有多种类型,如共价键、离子键、范德瓦尔...
- 发布于 2021-06-28 10:56
- 阅读 ( 308 )
如何计算粘结顺序和粘结长度(calculate bond order and bond length)
...数。 这篇文章解释道, 1.什么是粘结顺序和粘结长度 2.如何计算债券顺序和债券长度-如何计算债券顺序-如何计算债券长度 什么是键顺序和键长(bond order and bond length)? 键长和键序是与共价键相关的两个参数。键序是两个原子之...
- 发布于 2021-06-28 11:35
- 阅读 ( 384 )
离子共价(ionic covalent)和金属键(metallic bonds)的区别
主要差异离子(main difference ionic) vs. 共价的(covalent) 债券可分为两大类;一级债券和次级债券。主键是将原子固定在分子中的化学键,而二次键则是将分子结合在一起的力。主要有三种类型的键,即离子键、共价键和金属...
- 发布于 2021-06-28 11:41
- 阅读 ( 813 )
键能(bond energy)和键离解能(bond dissociation energy)的区别
...离解能的平均值。 覆盖的关键领域 1.什么是键能-定义,计算单位,示例2.什么是键离解能-定义,示例3.键能和键离解能之间的区别-主要区别的比较 关键词:键能,离解能,化学键,原子,均裂,自由基 什么是键能(bond energy)...
- 发布于 2021-06-28 18:45
- 阅读 ( 454 )
键对(bond pair)和孤独的一对(lone pair)的区别
主差键对(main difference bond pair) vs. 孤独的一对(lone pair) 每个元素的原子中都有电子。这些电子位于原子核外的壳层中。一个壳层可以有一个或多个轨道。离原子核最近的轨道是s,p和d轨道。一个轨道可以分为几个子轨道...
- 发布于 2021-06-29 09:14
- 阅读 ( 628 )
同步(syn)和反加法(anti addition)的区别
...syn和反加法的主要区别。这些加成反应改变了反应物分子的键序和取代基的数目。 覆盖的关键领域 1.Syn添加是什么?定义、效果,示例2.什么是反加法–定义、效果,示例3.Syn与反加法之间的相似性-常见特性概述4.Syn和反加法之...
- 发布于 2021-06-30 09:27
- 阅读 ( 312 )