关键区别-离子固体与分子固体
在给定的温度下,化合物是固态的。固态意味着,物质中的原子、分子或离子被紧密地包裹起来,避免了这些化学物质的移动(不像在液体或气体中)。固体物质主要有两种类型:离子固体和分子固体。离子化合物包含通过离子化学键结合在一起的离子。离子间的相互作用力是带相反电荷的离子力。分子固体是一种固体物质,它含有通过范德华力**在一起的离散分子。离子固体和分子固体的关键区别在于,离子固体含有离子化学键,而分子固体含有范德华力。
目录
1. 概述和主要区别
2. 什么是离子固体
3. 什么是分子固体
4. 并列比较-离子和分子固体的表格形式
5. 摘要
什么是离子晶体(ionic solids)?
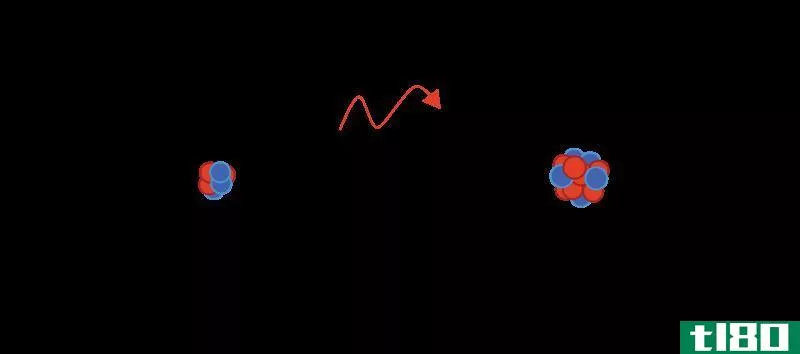
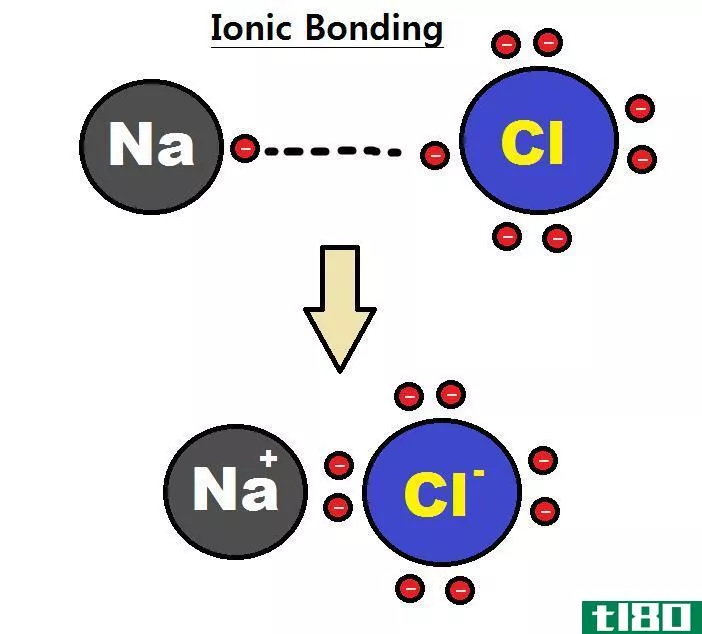
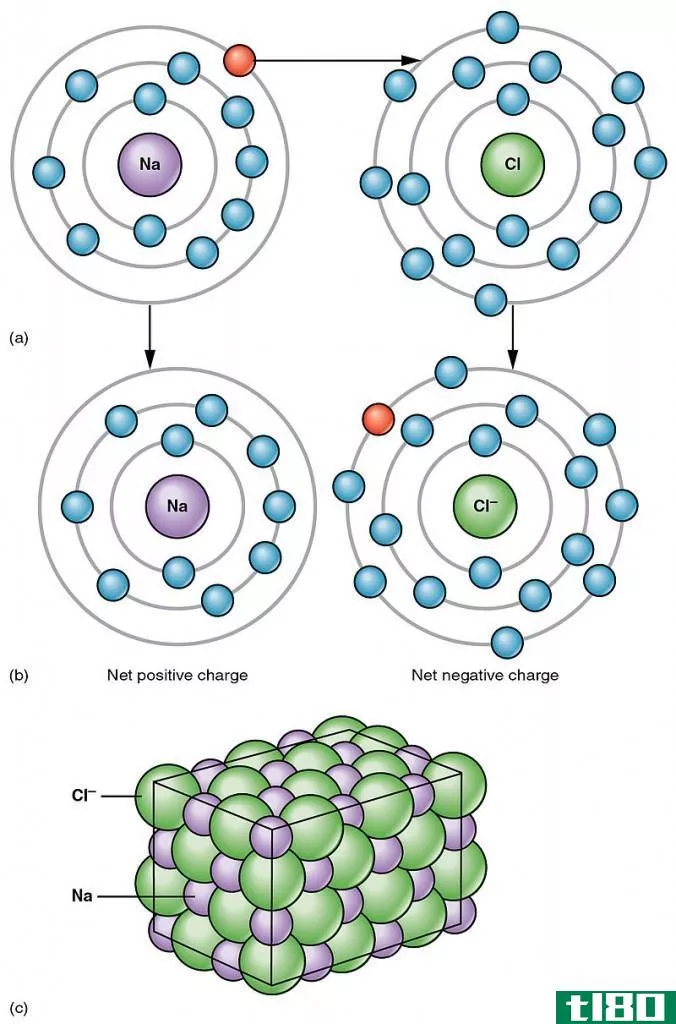
离子固体是由带相反电荷的离子通过静电吸引而结合在一起的固体化合物。这些离子是带正电荷的阳离子和带负电的离子(称为阴离子)。这些离子之间的化学键被称为离子键。离子固体的总电荷是中性的。这是因为阳离子被阴离子包围,反之亦然。
离子固体可以包含简单离子,如Na+和Cl-或复合离子,如铵离子(NH4+)。含有H+离子的离子固体被称为酸性化合物,因为这些固体溶解在水中时会释放出H+离子(这会降低水介质的pH值)。含有OH-离子的离子固体被称为碱性化合物,因为它们释放OH-离子(它会增加pH值)。
离子固体通常具有高熔点和高沸点。这些固体又硬又脆。当离子固体熔化时,由于离子化合物的熔融形式含有能导电的离子,所以它变得非常导电。离子固体可以通过蒸发、沉淀、冷冻等不同的过程形成。
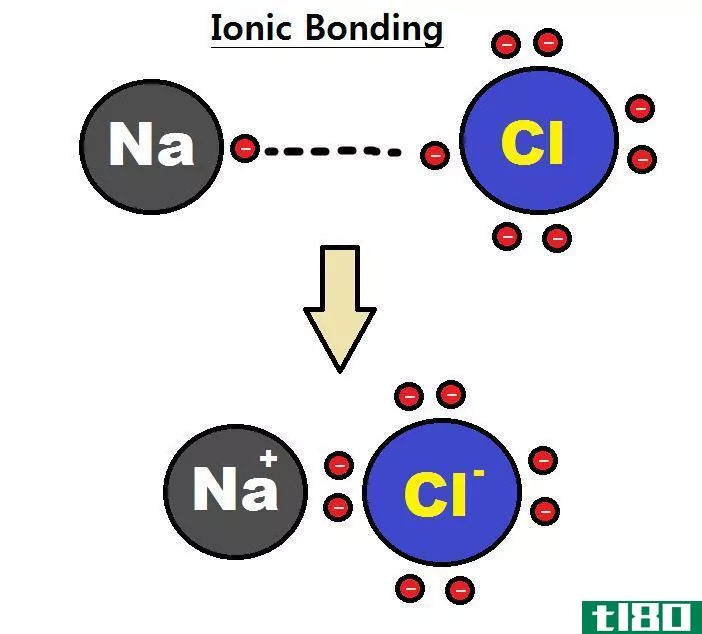
图01:离子键的形成
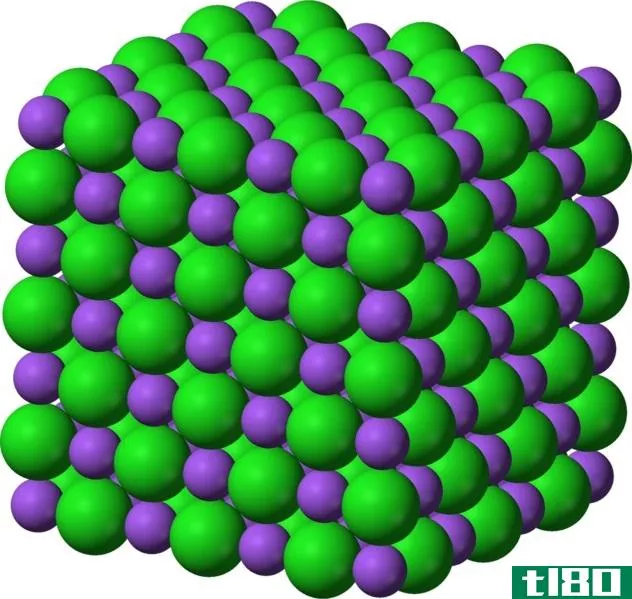
通常,离子固体具有规则的晶体结构。在那里,离子以一种使晶格能最小化的方式紧密地堆积在一起。晶格能是由完全分离的离子形成晶格所需的能量。
什么是分子固体(molecular solids)?
分子固体是指分子通过范德华力而不是离子键或共价键结合在一起的固体。分子固体包含离散分子。使这些分子相互结合的范德华力比共价键或离子键弱。这些单原子分子甚至可以存在于多原子固体中。
由于分子固体中的分子间作用力非常弱,这些固体化合物的熔点较低(通常低于300℃。而且这些分子固体相对较软,密度较低。然而,也可能存在氢键、偶极-偶极相互作用、伦敦力等(而不是范德华力)。
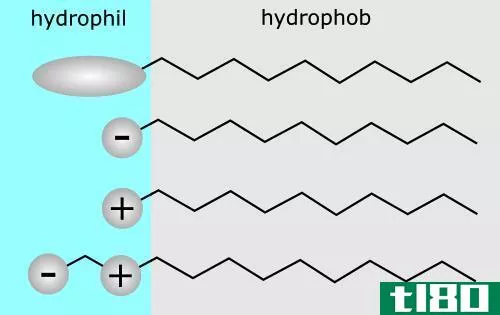
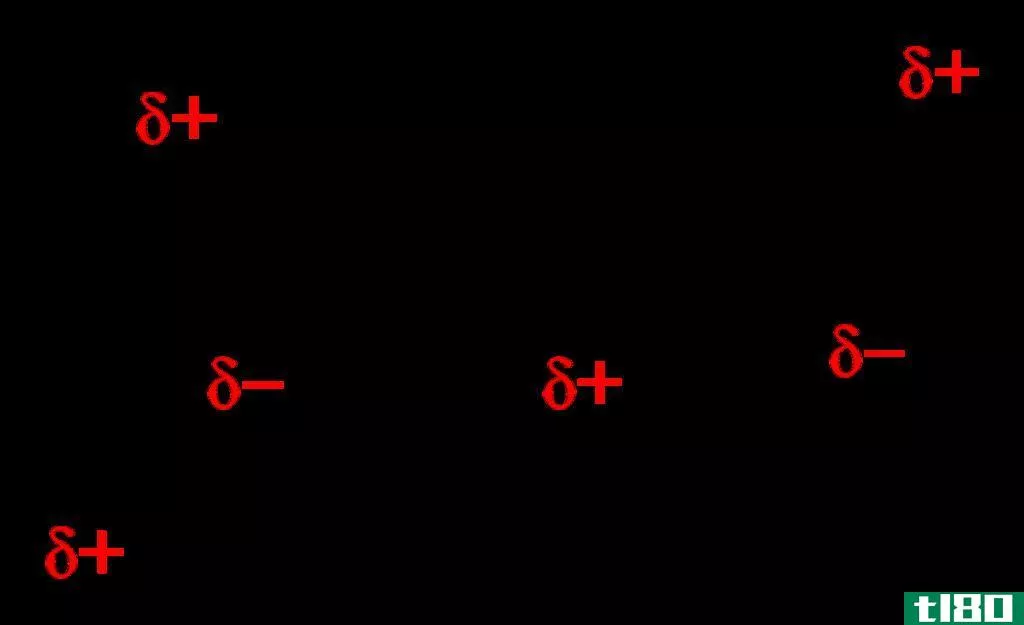
在非极性分子之间可以观察到范德华力。在极性分子中可以观察到偶极-偶极相互作用。氢键存在于含有O-H、N-H和F-H等官能团的分子之间。
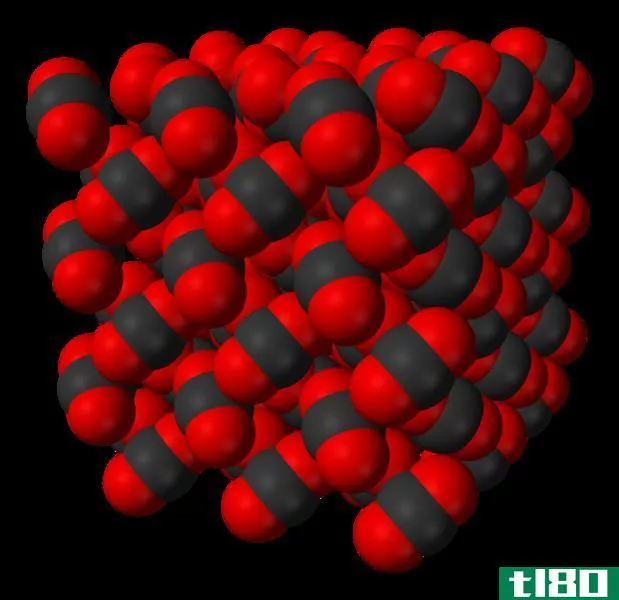
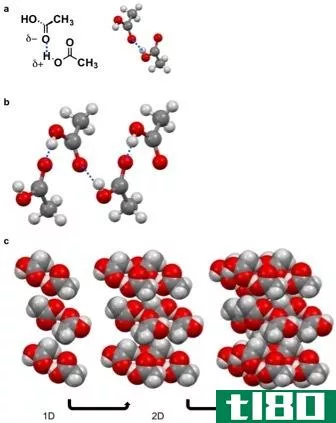
图02:显示固态二氧化碳分子的图表
分子固体中分子间的弱范德华力决定了固体的性质。其中一些特性包括熔点和沸点低、机械强度低、导电率低、导热系数低等。
离子型(ionic)和分子固体(molecular solids)的区别
| 离子与分子固体 | |
| 离子固体是由带相反电荷的离子通过静电吸引而结合在一起的固体化合物。 | 分子固体是指分子通过范德华力而不是离子键或共价键结合在一起的固体。 |
| 化学键 | |
| 离子固体有离子键。 | 分子固体主要有范德华力,也有氢键、偶极-偶极相互作用、伦敦力等。 |
| 粘结强度 | |
| 离子固体有很强的键。 | 分子固体有弱键。 |
| 组件 | |
| 离子固体有阳离子和阴离子。 | 分子固体有极性或非极性分子。 |
| 熔点和沸点 | |
| 离子固体具有高熔点和高沸点。 | 分子固体具有低熔点和低沸点。 |
| 密度 | |
| 离子固体的密度很高。 | 分子固体的密度很低。 |
| 自然 | |
| 离子固体又硬又脆。 | 分子固体相对较软。 |
总结 - 离子型(ionic) vs. 分子固体(molecular solids)
离子固体是由阳离子和阴离子组成的固体化合物。这些相反带电的离子之间有静电吸引力。分子固体中有分子,它们之间有分子间的作用力。它们是弱的化学相互作用。离子固体和分子固体的区别在于,离子固体含有离子化学键,而分子固体含有范德华力。
引用
1.Helmenstine,Anne Marie,D.“分子固体——定义和示例”,ThoughtCo,2017年2月19日。可在此处查阅2.“离子固体”,化学图书馆,图书馆,2016年7月21日。此处提供3.“分子固体”,维基百科,维基媒体基金会,2018年2月27日。此处提供
3.“分子固体”,维基百科,维基媒体基金会,2018年2月27日。