离子固体和金属固体的主要区别在于,离子固体基本上含有阳离子和阴离子,而金属固体含有金属原子和自由电子。
离子固体和金属固体都是固态的。但它们在组成和性质上是不同的。
目录
1. 概述和主要区别
2. 什么是离子固体
3. 什么是金属固体
4. 并列比较-离子和金属固体的表格形式
5. 摘要
什么是离子晶体(ionic solids)?
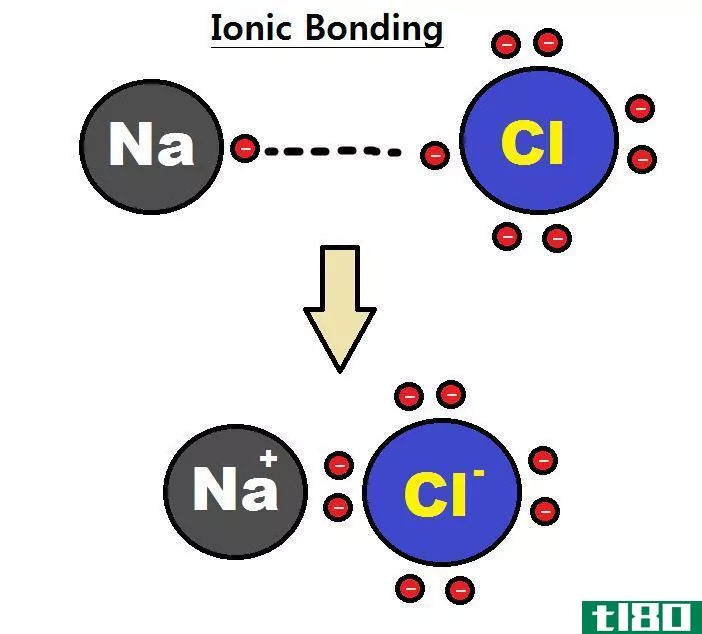
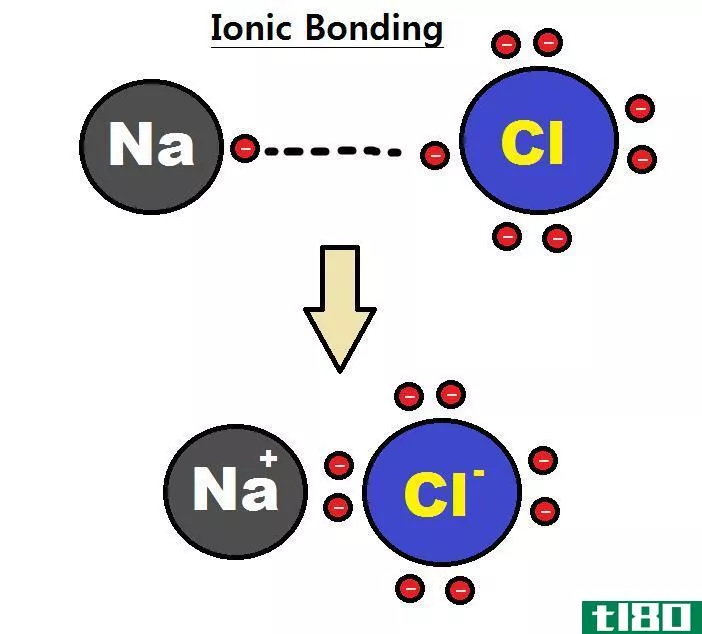
离子固体是含有阳离子和阴离子的化合物。这些离子被静电力凝聚在一起。我们把这些力称为离子键。离子相互结合的方式是整个化合物是中性的(没有负电荷或正电荷)。在这里,一个阴离子周围的阳离子数,反之亦然,取决于阳离子和阴离子的电荷量,不同固体之间的阳离子数也不同。

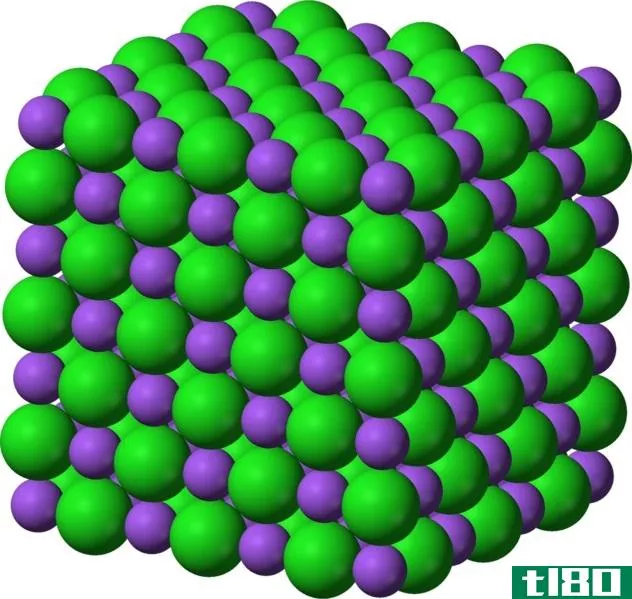
图01:离子固体的强结晶结构
固体中的离子可以是简单离子,如钠离子和氯离子(在氯化钠离子化合物或盐中),也可以是复杂离子,如多原子离子,即铵离子。这些固体以三维网络的形式存在,通常,它们具有晶体结构。
此外,含有氢离子的离子固体是酸,而含有氢离子的离子固体是碱。不含这些离子的固体称为盐。盐类化合物是由酸碱反应形成的。此外,离子固体也可以通过蒸发(除去溶剂将离子结晶成固体)、沉淀、固态反应等形成。
通常,离子固体具有很高的熔点和沸点,因为它们具有很强的三维网络结构,很难分解。这些固体通常也很坚硬和易碎。此外,当这些离子被溶解时,它们会被电性很强的离子释放出来。
什么是金属晶体(metallic solids)?
金属固体是含有金属原子和周围电子的固体化合物。金属固体是很好的例子。这些固体的金属原子通过金属键结合在一起。金属原子以带正电荷的阳离子的形式存在,这些原子浸没在电子的海洋中。在阳离子形成过程中,这些电子来自金属原子。

图02:固态镓金属
这意味着,金属原子通过释放价电子形成阳离子,这些电子以离域状态出现在金属离子周围,这些电子使金属原子结合在一起。
离子型(ionic)和金属晶体(metallic solids)的区别
离子固体和金属固体都是固态的,但它们的组成和性质不同。离子固体和金属固体的主要区别在于,离子固体基本上含有阳离子和阴离子,而金属固体则含有金属原子和自由电子。
此外,离子固体在阳离子和阴离子之间具有静电吸引力,而金属固体具有金属键。在考虑性能时,离子固体是硬的和易碎的,而金属固体是硬的,韧性和可塑性的。
下面的信息图总结了离子和金属固体之间的区别。

总结 - 离子型(ionic) vs. 金属晶体(metallic solids)
离子固体和金属固体都是固态的,但它们的组成不同,这也导致它们的性质不同。离子固体和金属固体的主要区别在于,离子固体基本上含有阳离子和阴离子,而金属固体则含有金属原子和自由电子。此外,离子固体在阳离子和阴离子之间有静电吸引力,但在金属固体中,存在金属键。
引用
1“离子固体”,化学歌词,歌词,2019年6月5日,可在这里查阅。