离子型(ionic)和共价化合物(covalent compounds)的区别
根据离子和共价化合物在水中的溶解度、电导率、熔点和沸点等宏观性质,可以注意到它们之间的许多差异。造成这些差异的主要原因是它们的结合方式不同。因此,它们的键合模式可以被认为是离子化合物和共价化合物的关键区别。(离子键和共价键的区别)当离子键形成时,电子由金属捐赠,捐赠电子被非金属接受。由于静电的吸引,它们形成了一个牢固的键。两种非金属之间形成共价键。在共价键合中,两个或多个原子共享电子以满足八位元规则。一般来说,离子键比共价键强。这就导致了它们物理性质的不同。
什么是离子化合物(ionic compounds)?
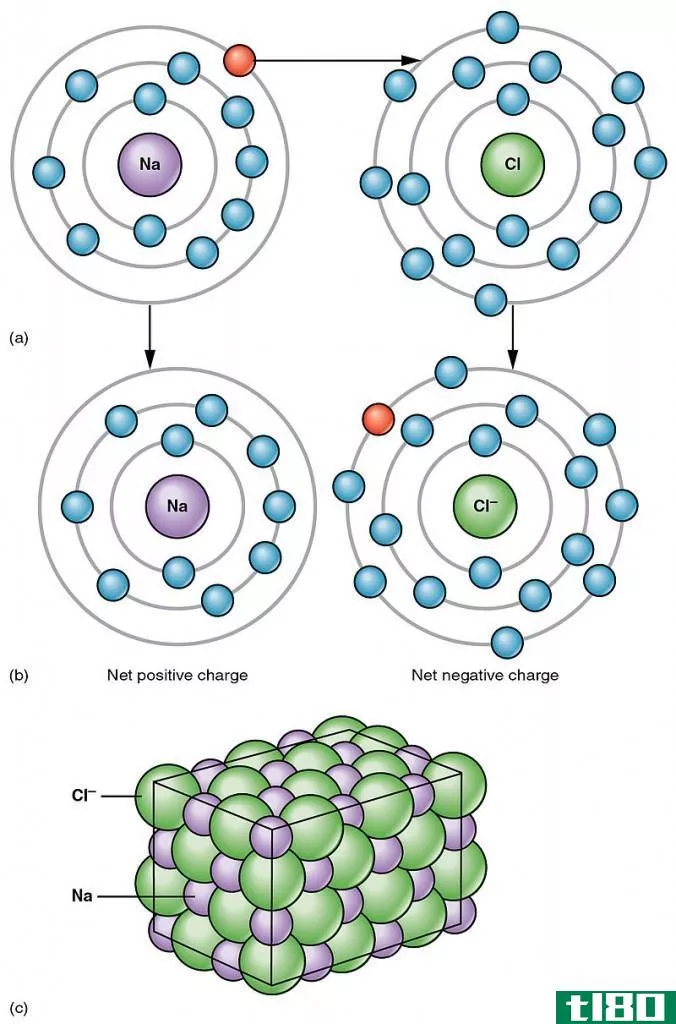
当两个原子的电负性值相差很大时,就会形成离子键。在键形成过程中,负电性越低的原子损失电子,负电荷越多的原子获得电子。因此,产生的离子是相反的带电离子,它们由于强大的静电吸引力而形成键。
离子键是在金属和非金属之间形成的。一般来说,金属在最外层的价电子并不多;然而,非金属的价壳层中有接近8个电子。因此,非金属倾向于接受电子来满足八位元规则。
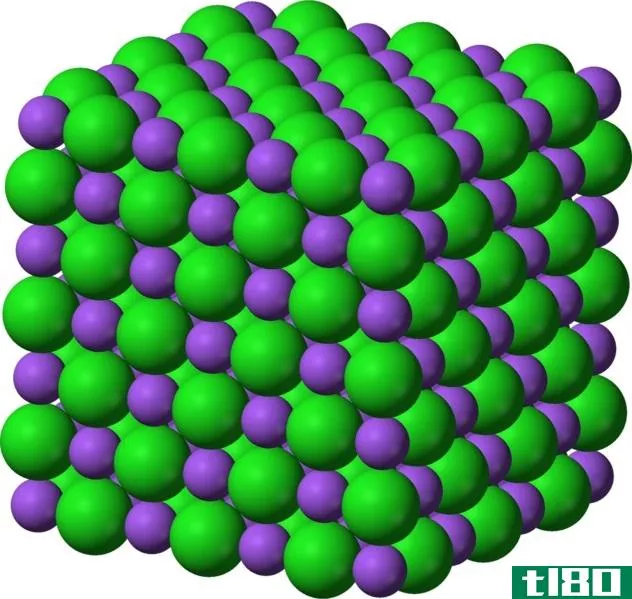
离子化合物的例子是Na++Cl–a NaCl
Sodium(metal) has only one valence electron and Chlorine (non-metal) has seven valence electr***. 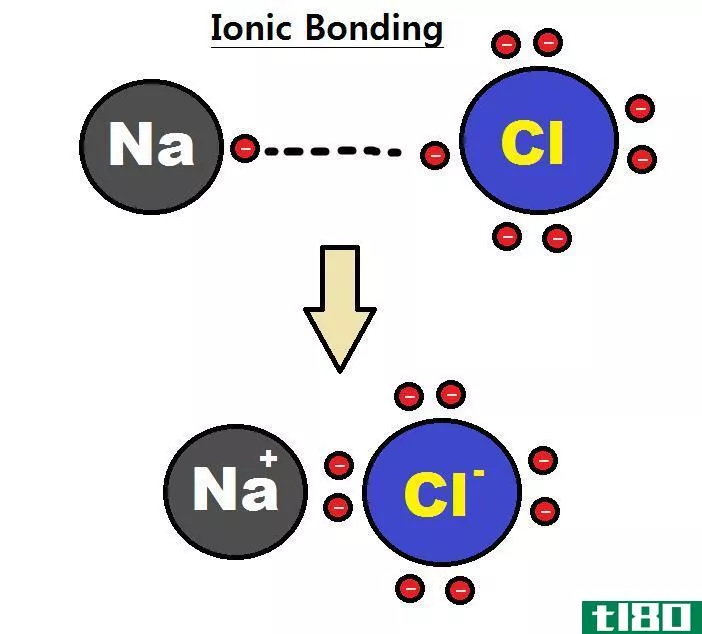
什么是共价化合物(covalent compounds)?
共价化合物是由两个或多个原子共享电子而形成的,以满足“八位体规则”。这种键合类型常见于非金属化合物中,同一化合物的原子或附近元素的周期性两张桌子具有几乎相同电负性值的原子不会从价壳层交换(捐赠/接收)电子。相反,它们共享电子以实现八位元组态。
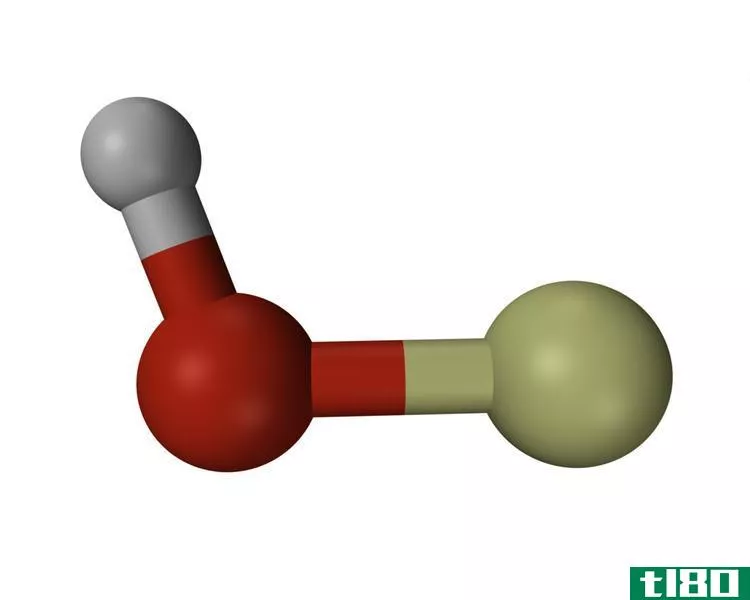
共价化合物的例子有甲烷(CH4)、一氧化碳(CO)、一溴化碘(IBr)
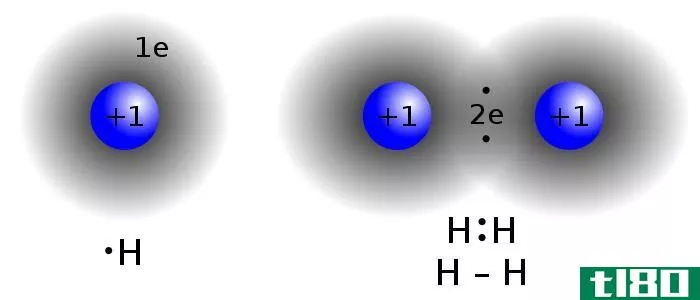
共价键合
离子型(ionic)和共价化合物(covalent compounds)的区别
离子化合物和共价化合物的定义
离子化合物:离子化合物是由离子键以晶格结构结合在一起的阳离子和阴离子的化合物。
共价化合物:共价化合物是原子间共享一个或多个电子,特别是成对电子而形成的化学键。
离子和共价化合物的性质
物理性质
离子化合物:
所有离子化合物在室温下都以固体形式存在。
离子化合物具有稳定的晶体结构。因此,它们具有较高的熔点和沸点。正负离子之间的吸引力非常强。
| 离子化合物 | 外观 | 熔点 |
| 氯化钠-氯化钠 | 白色结晶固体 | 801摄氏度 |
| KCl–氯化钾 | 白色或无色玻璃状晶体 | 770摄氏度 |
| 氯化镁-氯化镁 | 白色或无色晶体固体 | 1412摄氏度 |
共价化合物:
共价化合物以所有三种形式存在:室温下的固体、液体和气体。
与离子化合物相比,它们的熔点和沸点相对较低。
| 共价化合物 | 外观 | 熔点 |
| 氯化氢 | 无色气体 | -114.2摄氏度 |
| CH4-甲烷 | 无色气体 | -182摄氏度 |
| 四氯化碳 | 无色液体 | -23摄氏度 |
电导率
离子化合物:固体离子化合物没有自由电子,因此它们不以固体形式导电。但是,当离子化合物溶解在水中时,它们会形成导电的溶液。换句话说,离子化合物的水溶液是良好的导电体。
共价化合物:无论是纯共价化合物还是水中的溶解形式都不导电。因此,共价化合物在所有相中都是不良导体。
溶解度
离子化合物:大多数离子化合物溶于水,但不溶于非极性溶剂。
共价化合物:大多数共价化合物溶于非极性溶剂,但不溶于水。
硬度
离子化合物:离子固体是硬而易碎的化合物。
Image Courtesy: “Covalent bond hydrogen” by Jacek FH – Own work. (CC BY-SA 3.0) via Comm*** “IonicBondingRH11” by Rhannosh – Own work. (CC BY-SA 3.0) via Wikimedia Comm***