关键区别-氧化数法与半反应法
氧化数法和半反应法是平衡氧化还原反应化学方程式的两种方法。氧化还原反应是由两个平行的化学反应组成的化学反应:氧化反应和还原反应。这些被称为氧化还原反应的半反应。因此,氧化还原反应发生在反应混合物中,其中一种物质经历氧化,另一种物质(或同一种物质)经历还原。氧化和还原改变化学元素的氧化数或氧化状态。无论是氧化数的变化,还是氧化还原反应中发生的半反应,都可以用来平衡氧化还原反应的整体化学方程式。氧化数法与半反应法的关键区别在于,氧化数法是利用反应混合物中化学物种氧化数的变化,而半反应法是用两个平行的半反应平衡后再加成的方法。
目录
1. 概述和主要区别
2. 什么是氧化数法
3. 什么是半反应法
4. 并列比较-氧化数法与半反应法的表格形式
5. 摘要
什么是氧化数法(oxidation number method)?
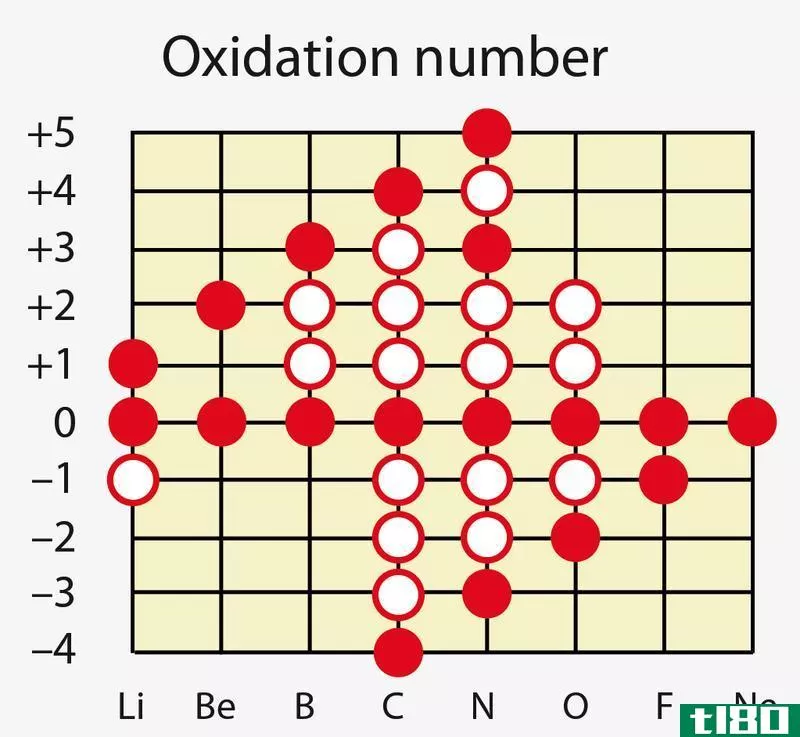
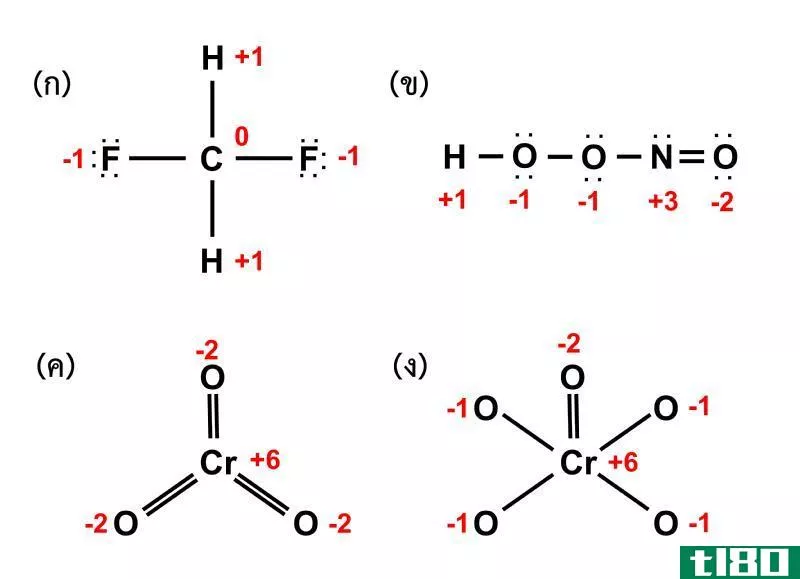
氧化数法是利用反应混合物中化学物种的氧化数来平衡氧化还原反应的化学方程式的方法。化学元素的氧化数就是该元素的氧化程度。氧化数有时称为氧化状态,它可以是正值,也可以是负值,也可以是零。当一个原子的氧化数增加时,我们称之为该原子已氧化;相反,当氧化数减少时,该原子就减少了。
例:锌(Zn)与盐酸(HCl)反应生成氯化锌(ZnCl2)和氢气(H2)。该反应是一个氧化还原反应,锌氧化,氢原子还原,氯的氧化数不变。锌原子被氧化成Zn2+,而H+离子被还原成H2。
Zn+HCl→ZnCl2+H2

图01:锌与盐酸的反应
氧化数法可用于平衡上述方程。首先,应该指出所有原子的氧化数。
锌=0
H在HCl中=+1
Znin ZnCl2=+2
H2中的H=0
然后确定这些氧化值发生的变化。锌被氧化成Zn2+,而H+被还原成H2。在认识到这些变化后,应指出每个原子氧化数的增加或减少。我们把这个因子称为“ON因子”(每个原子的增加或减少)。确定ON因子后,氧化原子应乘以还原原子的ON因子,反之亦然。
关于系数Zn=2
系数H=1
相乘时,{znx1}+{hclx2}→{zncl2x1}+{H2}
得到了平衡的氧化还原反应:Zn+2HCl→ZnCl2+H2
什么是半反应法(half reaction method)?
半反应法是一种利用两个平行的半反应来平衡氧化还原反应的方法:氧化半反应和还原半反应。在氧化还原反应中,一种反应物起氧化剂的作用,氧化另一种反应物,同时使自身还原。
例:在锌和盐酸的反应中,锌是还原剂,盐酸中的氢是氧化剂。那么平衡的两个半反应可以写成:
氧化:Zn→Zn+2+2e
还原:2HCl+2e→H2+2Cl–
然后我们可以简单地加上半反应,得到平衡的氧化还原反应。但在加入它们之前,应检查两边的电子数是否相等(只有这样,两边的电子才能被抵消,得到网络方程)。如果电子不相等,则整个方程(半反应)应乘以一个适当的值,直到它等于另一半反应中的电子数。
平衡氧化还原反应:Zn+2HCl→ZnCl2+H2
氧化数法(oxidation number method)和半反应法(half reaction method)的区别
| 氧化数法与半反应法 | |
| 氧化数法是利用反应混合物中化学物种的氧化数来平衡氧化还原反应的化学方程式的方法。 | 半反应法是一种利用两个平行的半反应来平衡氧化还原反应的方法:氧化半反应和还原半反应 |
| 方法 | |
| 氧化数法利用反应物和产物中每个原子氧化数的变化。 | 半反应法采用氧化还原反应的氧化还原反应。 |
总结 - 氧化数法(oxidation number method) vs. 半反应法(half reaction method)
氧化还原反应是一种常见的反应类型,其中一种反应物起氧化剂的作用,而另一种反应物起还原剂的作用。平衡氧化还原反应有两种主要方法:氧化数法和半反应法。二者氧化反应数之和为二者之和的氧化反应数之和为二者之数之二的氧化反应之数之二之二之数之差之氧化反应法,采用二者之二之数之差之氧化反应法。
引用
1.“平衡氧化还原反应。”平衡氧化还原反应,离子电子法,氧化数法|【电子邮件保护】2.“氧化数法平衡氧化还原反应方程式。”用于pH计算、浓度转换溶液制备和化学方程式平衡的化学计算器软件。此处提供
2.“氧化数法平衡氧化还原反应方程式”,用于pH计算、浓度转换溶液制备和化学方程式平衡的化学计算器软件。