离子电子法和氧化数法的关键区别在于,在离子电子法中,反应是根据离子的电荷来平衡的,而在氧化数法中,反应是根据氧化剂和还原剂的氧化数的变化来平衡的。
离子电子法和氧化数法是平衡化学方程式的重要方法。对于一个特定的化学反应,给出了一个平衡的化学方程式,它可以帮助我们确定反应物中有多少反应物产生特定量的产物,或反应物的量,以获得所需量的产物。
目录
1. 概述和关键区别
2. 什么是离子电子法
3. 氧化数法是什么
4. 并排比较——离子电子法与氧化数法的表格形式
5. 摘要
什么是离子电子法(ion electron method)?
离子电子法是一种利用离子半反应确定反应物与产物之间化学计量关系的分析技术。给定某一特定化学反应的化学方程式,就可以确定该化学反应的两个半反应,并平衡每一个半反应中的电子数和离子数,得到完全平衡的方程式。
图01:化学反应
让我们考虑一个例子来理解这个方法。
高锰酸盐离子与亚铁离子的反应如下:
MnO4–+Fe2+⟶Mn2++Fe3++4H2O
两个半反应是高锰酸盐离子转化为锰离子和亚铁离子转化为铁离子。这两个半反应的离子形式如下:
MnO4–⟶Mn2+
Fe2+⟶Fe3+
此后,我们必须平衡每个半反应中氧原子的数量。在亚铁转化为铁离子的半反应中,没有氧原子。因此,我们必须平衡另一半反应中的氧气。
MnO4–⟶Mn2++4O2-
这四个氧原子来自水分子(不是分子氧,因为在这个反应中没有气体产生)。那么正确的半反应是:
MnO4–⟶Mn2++4H2O
在上面的方程中,左边没有氢原子,但是右边有八个氢原子,所以我们必须在左边加8个氢原子(氢离子的形式)。
MnO4–+8H+⟶Mn2++4H2O
在上面的方程中,左侧的离子电荷不等于右侧的离子电荷。因此,我们可以在其中一个侧面加上电子来平衡离子电荷。左边的电荷是+7,右边是+2。在这里,我们要在左边加五个电子。一半的反应是,
MnO4–+8H++5e–⟶Mn2++4H2O
当平衡亚铁转化为铁离子的半反应时,离子电荷从+2转化为+3;这里我们需要在右侧添加一个电子,如下所示,以平衡离子电荷。
Fe2+⟶Fe3++e–
此后,我们可以通过平衡电子数将两个方程相加。我们要把亚铁转化为铁的半反应乘以5,得到五个电子,然后把这个修正的半反应方程式加到高锰酸盐转化为锰(II)离子的半反应中,两边的五个电子就抵消了。以下反应是这种添加的结果。
MnO4–+8H++5Fe2++5e–⟶Mn2++4H2O+5Fe3++5e–
MnO4–+8H++5Fe2+⟶Mn2++4H2O+5Fe3+
什么是氧化数法(oxidation number method)?
氧化数法是一种分析技术,利用反应物从反应物到产物时化学元素氧化的变化来确定反应物与产物之间的化学计量关系。在氧化还原反应中,有两个半反应:氧化反应和还原反应。与上述相同的例子,高锰酸盐与亚铁离子的反应,氧化反应是亚铁离子转化为铁离子,还原反应是高锰酸盐离子转化为锰(Ⅱ)离子。
氧化:Fe2+⟶Fe3+
还原:MnO4–⟶Mn2+
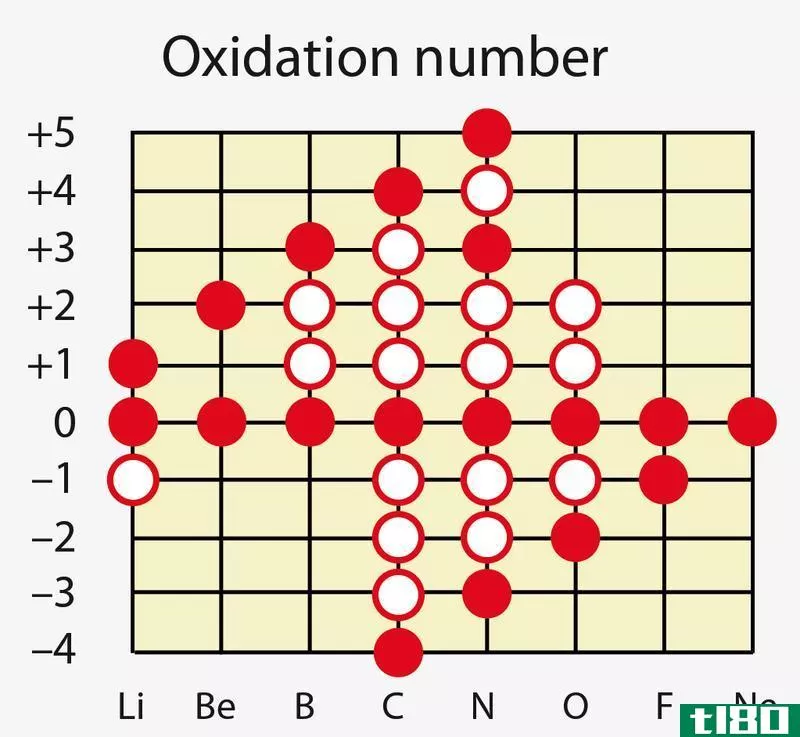
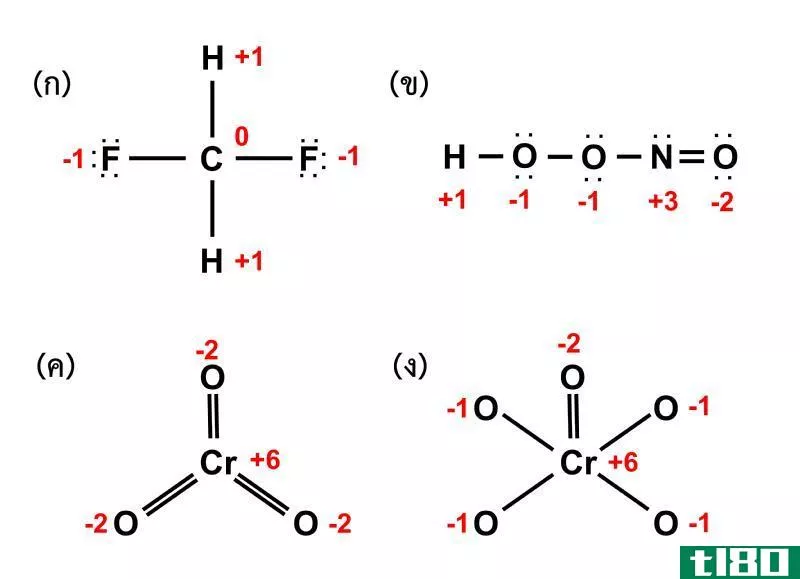
当平衡这类反应时,首先我们需要确定化学元素氧化状态的变化。在氧化反应中,亚铁离子的+2转化为+3的铁离子。在还原反应中,锰的+7转化为+2。因此,我们可以通过乘以另一半反应中氧化态的增量/减量来平衡这些氧化态。在上述示例中,氧化反应的氧化状态变化为1,还原反应的氧化状态变化为5。然后,氧化反应乘以5,还原反应乘以1。
5Fe2+⟶5Fe3+
MnO4–⟶Mn2+
然后,我们可以把这两个半反应相加,得到完整的反应,然后利用水分子和氢离子来平衡其他元素(氧原子),以平衡两边的离子电荷。
MnO4–+8H++5Fe2+⟶Mn2++4H2O+5Fe3+
离子电子法(ion electron method)和氧化数法(oxidation number method)的区别
离子电子法和氧化数法是平衡化学方程式的重要方法。离子电子法和氧化数法的关键区别在于,在离子电子法中,反应是根据离子的电荷来平衡的,而在氧化数法中,反应的平衡取决于氧化剂和还原剂氧化数的变化。
下面的信息图总结了离子电子法和氧化数法的区别。

总结 - 离子电子法(ion electron method) vs. 氧化数法(oxidation number method)
离子电子法和氧化数法的关键区别在于,在离子电子法中,反应是根据离子的电荷来平衡的,而在氧化数法中,反应的平衡取决于氧化剂和还原剂氧化数的变化。
引用
1“平衡方程式。”