价态和氧化数之间的关键区别在于,价态是一个原子为稳定所能失去、获得或共享的最大电子数,而氧化数是一个原子为了与另一个原子形成键而可以失去或获得的电子数。
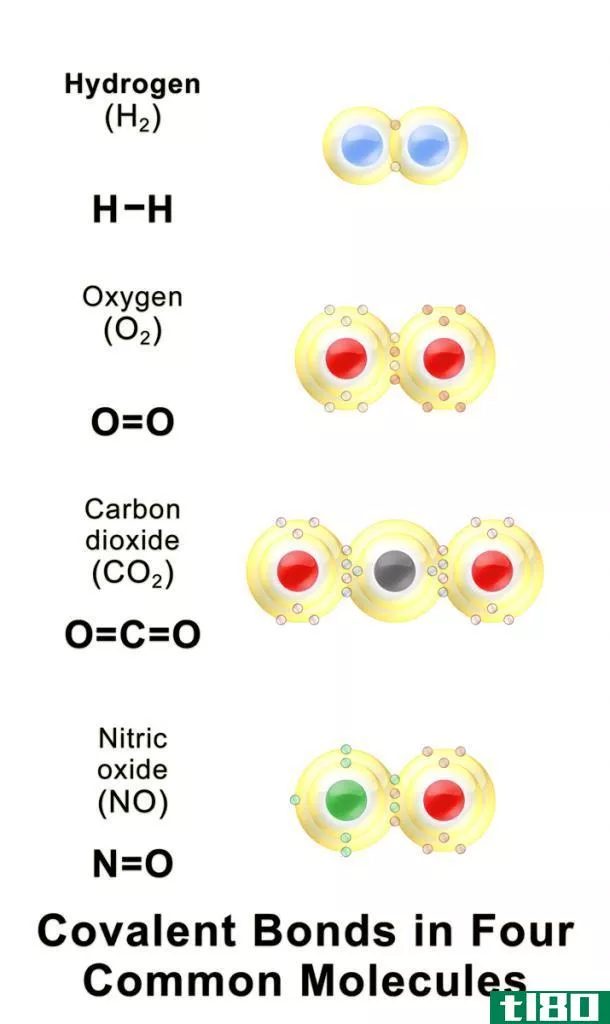
氧化数和价电子与原子的价电子有关。价电子是占据原子最外层轨道的电子。这些电子对原子核的吸引力很弱;因此,原子可以很容易地移除或与其他原子共享这些电子。这种电子的丢失、获得或共享导致一个特定的原子具有氧化数和价态,最终在两个原子之间形成化学键。
目录
1. 概述和主要区别
2. 什么是价
3. 氧化数是多少
4. 并列比较-以表格形式表示的价态与氧化数
5. 摘要
什么是价(valency)?
价态是一个原子失去、获得或分享以稳定的最大电子数。对于金属和非金属,八位元规则描述了原子最稳定的形式。在这里,如果一个原子最外层的壳层的数目被完全填满(需要八个电子来完成),那么这个电子组态是稳定的。换言之,如果s和p子轨道完全填充,具有ns2np6构型,则原子是稳定的。
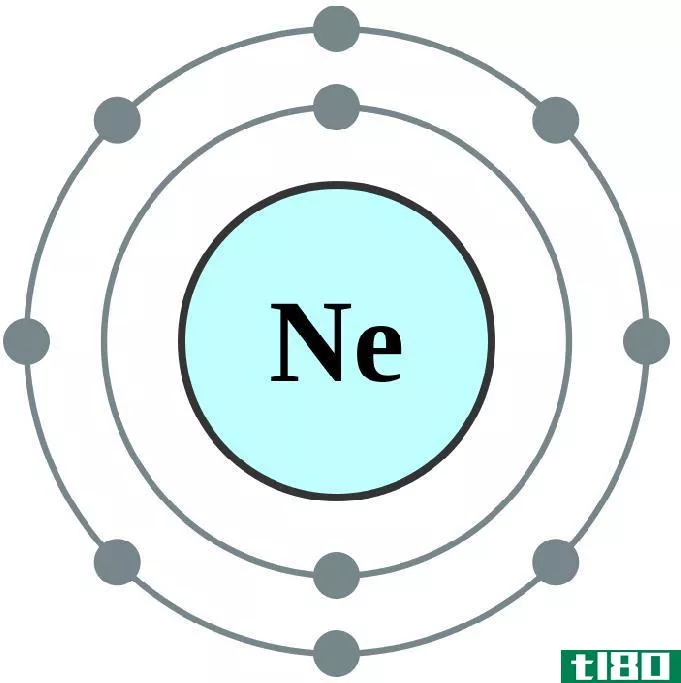
很自然,惰性气体原子有这种电子构型。因此,其他元素需要丢失、获得或共享电子来遵守八位元规则。在这种稳定过程中,一个原子需要失去、获得或分享的最大电子数就是该原子的价态。
例如,让我们考虑一下硅。硅的电子组态为1S22S2P63S2**2。最外层的壳层是n=3,它有4个电子。因此,它应该再获得四个电子来完成八位元。一般来说,硅可以与其他元素共享4个电子来完成八位体。因此,硅的价态是4。
对于不同的化学元素,其价态是不同的。这是因为电子是根据轨道的能级填充到轨道上的。然而,大多数过渡金属具有相同的价态,通常为2。但是,有些元素可以有不同的价态,因为原子可以通过去除电子而稳定在不同的电子构型中。
例如,在铁(Fe)中,电子组态为[Ar]3d64s2。因此,铁的价态是2(4s2中有2个电子)。但有时,铁的价变成3。这是因为3d5电子组态比3d6更稳定。因此,再去掉一个电子和4s电子,铁就更稳定了。
什么是氧化值(oxidation number)?
氧化数是一个原子为了与另一个原子形成键而损失或获得的电子数。有时,我们交替使用氧化状态和氧化数这两个术语,但它们略有不同。
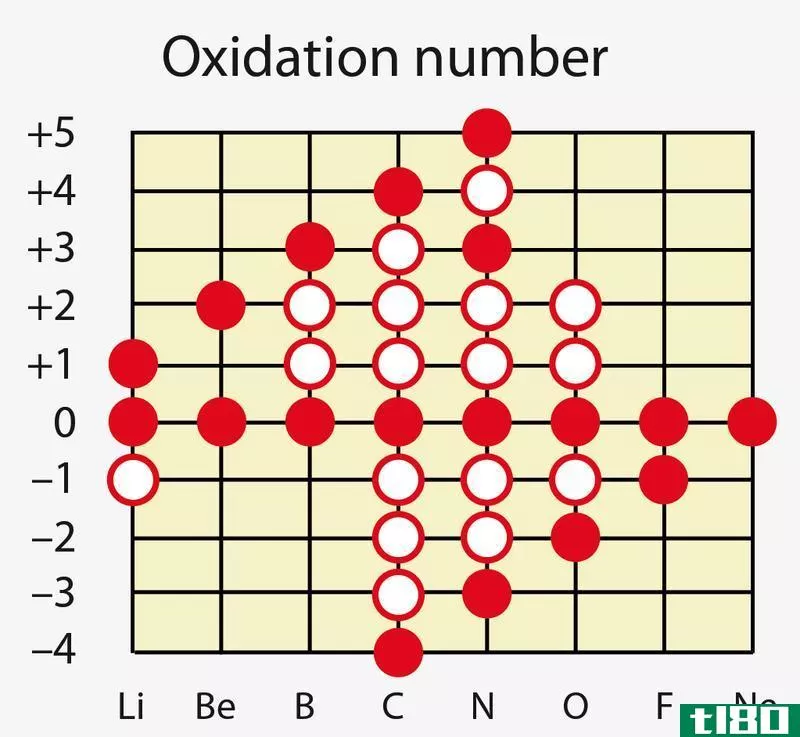
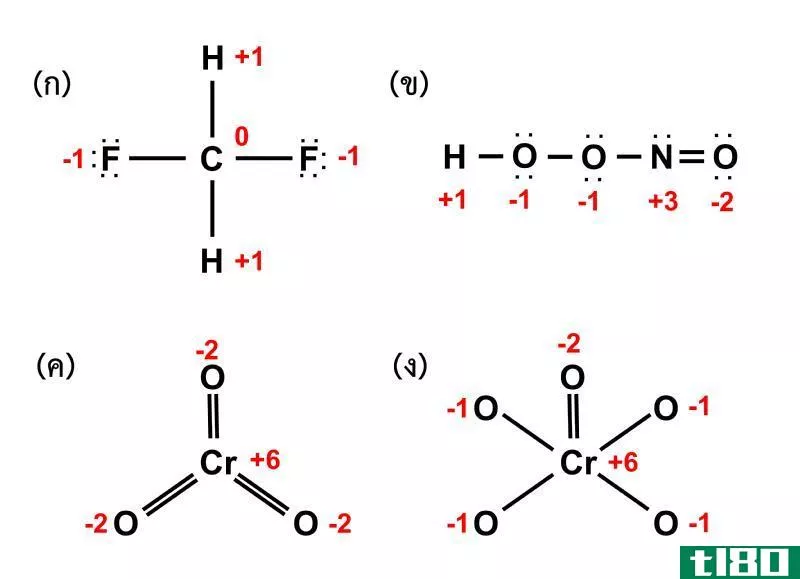
图01:一些化学元素可以显示不同的氧化数
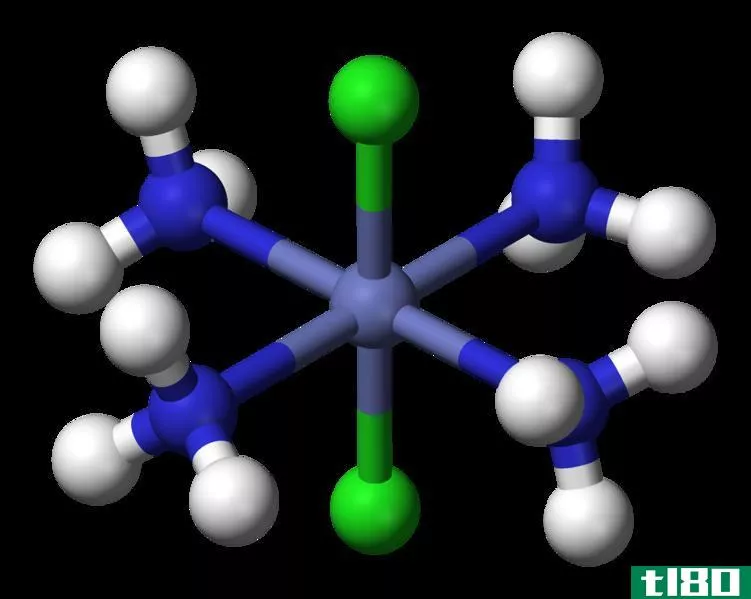
大多数情况下,氧化数一词用于配位络合物。在配位络合物中,氧化数是配位化合物中心原子的电荷,如果该原子周围的所有键都是离子键。配位配合物几乎总是由中心的过渡金属原子组成。这种金属原子周围有化学基团,我们称之为配体。这些配体有单独的电子对,可以与金属原子共享形成配位键。
配位键形成后,类似于共价键。这是因为配位键中的两个原子共享一对电子,就像共价键一样。然而,考虑到配位键是离子键,我们必须计算中心金属原子的氧化数。
价(valency)和氧化值(oxidation number)的区别
氧化数和价电子与原子的价电子有关。价态和氧化数之间的关键区别在于,价态是一个原子为稳定所能失去、获得或共享的最大电子数,而氧化数是一个原子为了与另一个原子形成键而可以失去或获得的电子数。此外,价一词适用于任何化学元素,但氧化数一词主要用于配位络合物。
下面的信息图总结了价态和氧化数之间的区别。

总结 - 价(valency) vs. 氧化值(oxidation number)
氧化数和价态都与原子的价电子有关。价态和氧化数之间的关键区别在于,价态是一个原子为稳定所能失去、获得或共享的最大电子数,而氧化数是一个原子为了与另一个原子形成键而可以失去或获得的电子数。
引用
1.“氧化数。”百科全书ædia Britannica,Inc.,百科全书ædia Britannica,Inc.,可在此处获得。