主要区别
真溶液与胶体溶液的主要区别在于,真溶液是均匀的单相体系,胶体溶液是非均匀的两相体系。
真正的解决方案(true soluti***) vs. 胶体溶液(colloidal soluti***)
真正的溶液是均匀的混合物,而胶体溶液是不均匀的混合物。真正的溶液是单相系统,而胶体溶液是两相系统。真正的溶液是溶质溶解在溶剂中,而胶体溶液是一个两相系统,其中一个相分散到另一个相。真实溶液由溶质和溶剂组成,而胶体溶液则由分散相和分散介质组成。真溶液外观透明,胶体溶液外观半透明。真正的溶液含有肉眼看不见的颗粒,而胶体溶液含有电子显微镜可见的颗粒。真溶液经过电解,而胶体溶液经过电泳。真溶液颜色是溶解在溶剂中的盐的颜色,而胶体溶液的颜色取决于胶体颗粒的大小。
比较图
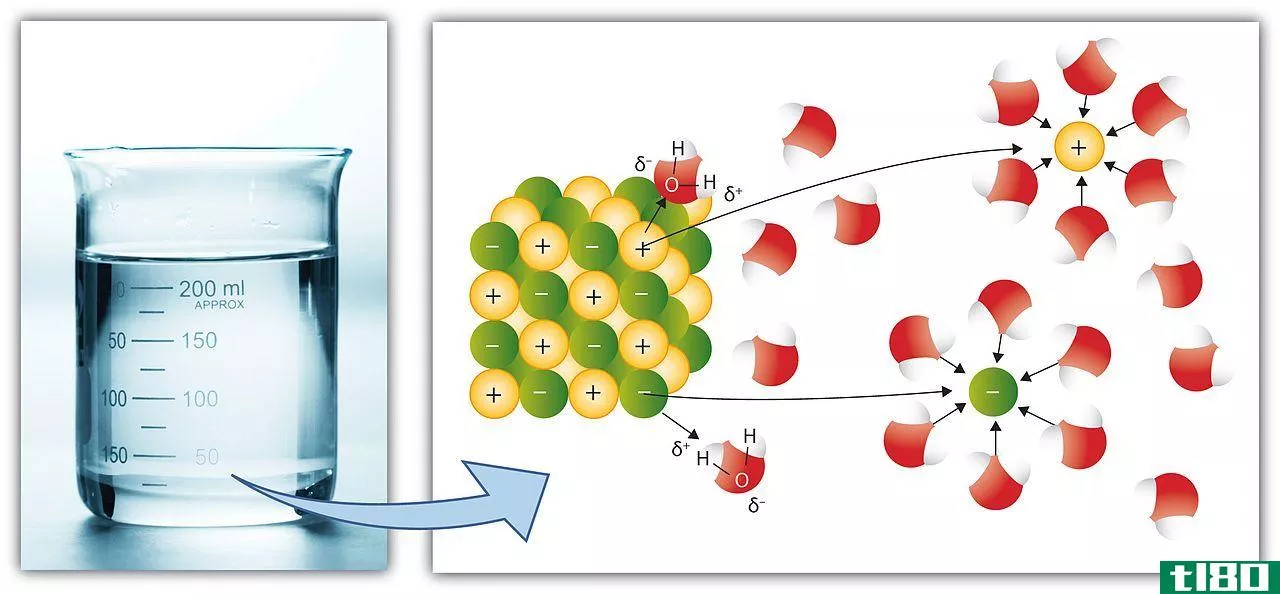
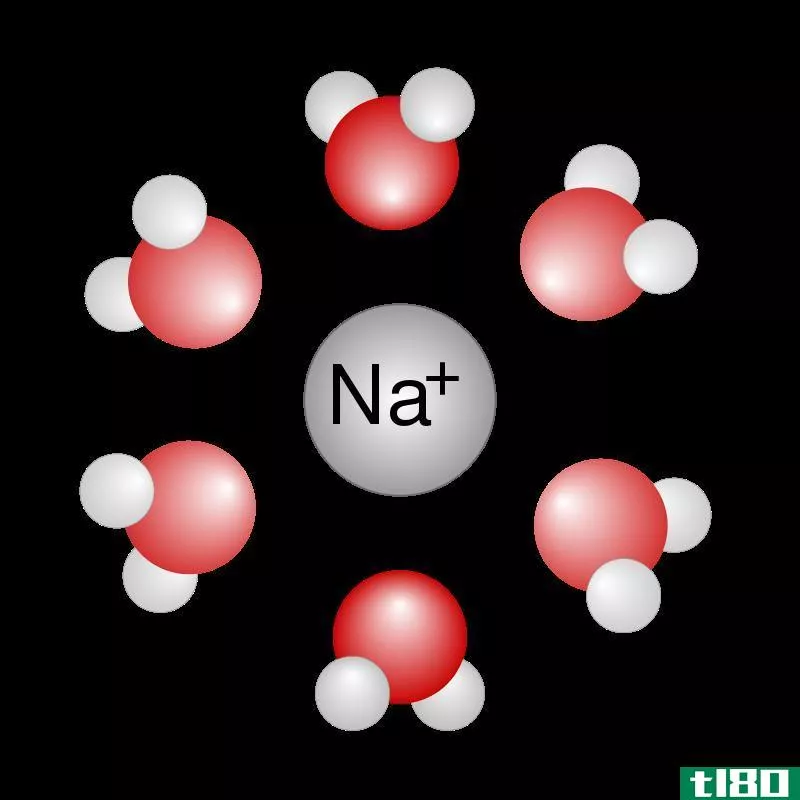
什么是真解(true solution)?
真正的解决方案是均质混合物。真正的解决方案是由两种或两种以上的成分组合而成。真正的溶液有溶质和溶剂。在真溶液的两种组分中,溶质含量较少,溶剂含量较大,但在某些情况下,也有例外。真实溶液中的溶质可以是固体、液体或气体,溶剂也是如此。当真溶液的两个组分结合时,两个组分的溶解环境都发生了变化。溶质分子从相似的分子中分离出来,然后溶剂分子围绕在它们周围。溶剂分子也能与其他类似分子充分分离,从而创造出一个容纳溶质分子的空间。只有当溶质和溶剂中的分子间力被溶剂溶质中的分子间力克服时,溶质才溶解在溶液中。如果溶质是极性的,则分子间作用力更大,如果溶质分子间作用力大于溶质极性分子中的分子间作用力,则溶质会溶解在溶剂中。这意味着溶剂也应该是极性的。真正的溶液是在溶解度原理的基础上形成的。真溶液的强度是以摩尔浓度、摩尔浓度、当量浓度或溶解在特定质量或体积溶剂中的溶质的质量或体积为基础来表示的。真解的强度可以用百分数表示。
例子
糖溶液
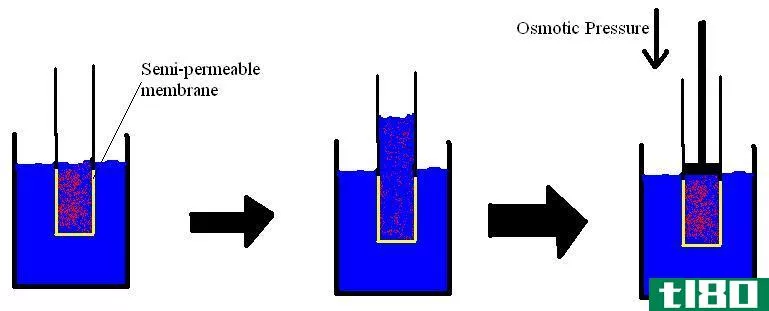
什么是胶体溶液(colloidal solution)?
胶体溶液是一种物质以粒子的形式分散在另一种物质中的体系。分散的物质形成分散相,分散的物质构成分散介质。胶体溶液是根据两种物质的物理状态来分类的,即分散和分散两种物质。只有当两种物质之间有相当大的接触时,一种物质才会分散到另一种物质中。胶体溶液有两种类型的疏水胶体溶液和亲干胶体溶液,但用疏水性和亲水性这两个通用术语代替。在亲水介质中分散的胶体粒子具有亲和力。疏水胶体溶液是指分散粒子对分散介质没有或很少亲和力的溶液。由于分散粒子对分散介质的亲和力,亲水胶体溶液具有热力学稳定性。因此,当分散粒子加入水中时,会自发形成亲水胶体溶液。当分散粒子加入水中时,亲水胶体溶液表现出自发聚结。胶体溶液粒子间的相互作用是由范德瓦尔斯力、熵力、空间力、排除体积力和静电相互作用等力引起的。胶体溶液有两种制备方法。胶体尺寸是通过喷射、研磨和剪切式振动或高剪切混合的应用来实现的。溶解的小分子可以通过氧化还原反应、沉淀和冷凝等过程凝聚成较大的胶体颗粒。
例子
溶于水的淀粉
主要区别
- 真溶液为单相体系,胶体溶液为两相体系。
- 真正的溶液特性是均质混合物;另一方面,胶体溶液特性是非均匀混合物。
- 真溶液有溶质和溶剂,而胶体溶液有分散和分散介质。
- 真实溶液的溶质粒径小于1nm,而胶体溶液的分散相粒径在1-1000nm之间。
- 真溶液呈透明状,胶体溶液呈半透明状。
- 真实溶液具有电解性质,而胶体溶液不具有这种性质。
- 真正的溶液粒子肉眼看不见,而胶体溶液粒子在电子显微镜下是可见的。
结论
以上讨论的结论是,真溶液和胶体溶液分别是均质和非均相混合物,在化学和药学中有着广泛的应用。